Ошибки при определении резус-фактора
Выделяют
следующие причины возникновения ошибок
при определении резус-фактора:
-
технические
погрешности. -
биологические
особенности испытуемой крови
Технические
погрешности.
-
неправильное
соотношение между сывороткой и
эритроцитами; -
преждевременная
оценка результатов; -
оценка результатов
по высыхающей капле; -
использование
неактивных, инфицированных, загнивших
и с истекшим сроком сывороток; -
определение
резус-фактора в гемолизированном и
длительно хранящемся образце крови.
Биологические
особенности испытуемой крови:
-
снижение
агглютинабельности резус-антигена при
некоторых заболеваниях печени, почек,
системы крови; -
неспецифическая
агглютинация испытуемых эритроцитов.
При
получении сомнительных результатов
необходимо повторить исследование,
используя более чувствительные методы.
КЛИНИЧЕСКОЕ
ЗНАЧЕНИЕ ГРУППОВОЙ
Дифференциации.Учение о совместимости
Группа
крови любого человека индивидуальна.
Выше указывалось о существовании
множества антигенных систем крови.
Любой эритроцитарный, лейкоцитарный,
тромбоцитарный или плазменный антиген
может быть причиной иммунологической
совместимости. Однако основную роль
при определении совместимости играют
антигены системы АВО и Rh-Нr.
Несовместимость
крови донора и реципиента наступает
при вливании крови, содержащей антигены,
на которые у реципиента в плазме имеются
антитела. В таких случаях возникает
агглютинация и гемолиз эритроцитов.
Совместимость по системе аво
В
1907 г. Grile,
а в 1908 г. Ottenberg
первыми выдвинули положение о переливании
крови с учетом групповой совместимости.
Они установили,
что при переливании крови только
одноименных групп, или в случае, когда
сыворотка реципиента не агглютинирует
эритроциты донора гемотрансфузия будет
успешной. В случае, когда сыворотка
реципиента агглютинирует эритроциты
донора, развиваются тяжелые осложнения,
обусловленные агглютинацией и гемолизом
эритроцитов. На основании этих наблюдений,
был сделан абсолютно правильный вывод:
можно переливать только биологически
совместимую кровь.
Оттенберг,
изучая проблемы совместимости,
сформулировал правило:
агглютинируются эритроциты переливаемой
крови, а не крови реципиента, так как
аггглютинины донорской крови разводятся
в крови реципиента, их
титр становится низким
и они не могут агглютинировать его
эритроциты
По
правилу Оттенберга можно переливать
кровь, эритроциты которой не агглютинируются
сывороткой реципиента, т. е можно
переливать не только однгуппную кровь,
но при совместимости кровь других групп.
Согласно
правилу Оттенберга кровь других групп
можно переливать по схеме.







Кровь
первой группы можно переливать людям
всех остальных групп, так как эритроциты
группы 0(I)
не содержат агглютиногенов А и В,поэтому
не могут дать агглютинацию ни с какими
сыворотками.
Сыворотка
группы AB(IV) не содержит никаких
агглютининов, поэтому эритроциты других
групп не будут агглютинироваться.
Поэтому больным с группой крови AB(IV)
можно переливать кровь любой группы.
Учитывая такую совместимость групп
крови, были введены понятия «универсальный
донор» и «универсальный реципиент».
Соответственно лица группы 0(I)
отнесены к «универсальным донорам», а
группы AB(IV) к «универсальным реципиентам».
Однако,
необходимо помнить, что при переливании
большого количества иногруппной
совместимой крови больным с массивной
кровопотерей агглютинины плазмы донора
не получают достаточной степени
разведения плазмой реципиента, и могут
агглютинировать эритроциты больного,
вызывая посттрансфузионный шок. Поэтому
правило Оттенберга можно применять при
трансфузии не более 1 литра крови.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
С детства практически каждый человек знает свою группу крови и резус-фактор. Эти данные пишутся на медицинской карточке каждого пациента, который проходит лечение в больнице или обращается в поликлинику за помощью. Считается, что группа крови и резус — это обусловленные генетически характеристики, которые формируются у плода еще в утробе матери и не могут быть изменены. Однако за последние несколько десятилетий было зафиксировано множество случаев «смены» то резуса, то группы крови у одного и того же человека в течение жизни. Может ли такое произойти на самом деле? Если да, то в чем же кроется причина? Разбирался во всех тонкостях этой проблемы MedAboutMe.

Что такое группа крови и резус-фактор?
Прежде чем говорить о возможности смены группы крови и резуса, следует разобраться в основных понятиях. Как известно, кровь человека состоит не только из жидкой части, но и из форменных элементов, среди которых важнейшую роль играют эритроциты. На своей поверхности эти клетки имеют специальные сигнальные молекулы — антигены (агглютиногены). Два основных антигена — это A и B: группы крови по системе ABO определяются именно благодаря наличию или отсутствию их в организме человека.
Иммунитет реагирует на наличие антигенов, вырабатывая против них специфические антитела, которые носят называния альфа и бета (агглютинины). Если представить это в упрощенной схеме, получается всего 4 возможных комбинации:
- оболочка эритроцитов не имеет ни A, ни B антигенов, но имеются альфа и бета антитела (первая группа крови);
- есть антиген A на поверхности эритроцитов, а также присутствуют антитела бета (вторая группа крови);
- есть антиген B на поверхности красных кровяных клеток, а также есть антитела альфа (третья группа крови);
- есть и A, и B антигены, но нет антител альфа и бета для них (четвертая группа).
В крови у одного и того же человека не могут находиться антиген A и антитело альфа (а также антиген B и антитело бета): это приведет к немедленному слипанию эритроцитов между собой и к гибели человека. С резус-фактором ситуация обстоит намного проще: он определяется по наличию или отсутствию на поверхности красных кровяных клеток антигена под названием Rh.
Почему же у одних людей есть антигены, а у других нет? Вопрос о том, каким образом в процессе эволюции сформировались группы крови и резус-фактор, до сих пор остается открытым. Часть ученых предполагает, что это может быть результатом древнейшего симбиоза каких-то микроорганизмов с клетками, которое закрепилось в популяции млекопитающих.
Факт!
Помимо традиционной системы ABO существуют и другие системы, которые используются гораздо реже. Примером могут служить системы Kell и MNS. Первая применяется в трансфузиологии, когда необходимо перелить кровь пациенту с аутоиммунной анемией и гемолитической болезнью новорожденных, а вторая — в работе судебно-медицинских экспертиз.
Могут ли анализы ошибаться?

Услышать истории о «магической» смене резус-фактора или группы крови можно довольно часто. На многих форумах люди делятся случаями, которые произошли с ними или их знакомыми и родственниками. Зачастую в таких историях группу крови и резус-фактор первый раз определяют в далеком детстве, после чего человек довольно продолжительное время не сдает никаких анализов. Как бы сильно не хотелось уверовать в собственную уникальность и исключительность, стоит помнить, что всегда есть место диагностической ошибке.
Группа крови определяется благодаря использованию специальных сывороток, которые содержат антитела альфа, бета и альфа+бета. Небольшую каплю сыворотки смешивают на специальном планшете с кровью человека, после чего внимательно наблюдают за склеиванием (агглютинацией) эритроцитов. Первая группа крови не дает реакцию агглютинации ни с одной из сывороток, четвертая — дает со всеми, вторая — с сывороткой, где есть антитела альфа, третья — где имеются антитела бета.
В настоящее время для достоверного определения группы крови и резус-фактора исследование проводится несколько раз, при этом используются качественные и свежие реактивы. А была ли такая возможность у какой-нибудь небольшой сельской больницы еще 30-40 лет назад? Плохое качество реагентов, использование просроченных материалов, несоблюдение температурного режима и преждевременная оценка результатов — все это может стать вполне банальными причинами «изменения» группы крови и резуса. Также не стоит забывать и о человеческом факторе: неправильное нанесение личных данных пациента на планшет, где проводится реакция, или перепутанные анализы отнюдь не являются редкостью.
Беременность и другие причины временного «изменения» группы крови

Если проанализировать большинство рассказов о смене резуса и группы крови, можно заметить, что именно беременность являлась ключевым моментом. Известно, что во время беременности женский организм претерпевает существенные изменения. В частности, увеличивается объём циркулирующей крови и количество эритроцитов, а количество агглютиногенов падает. Это приводит к тому, что при проведении исследования красные кровяные клетки в ряде случаев могут не склеиваться между собой. Таким образом ранее существовавшие вторая, третья и даже четвертая группы крови «превращаются» в первую. Но если пересдать анализ через несколько месяцев после родов, он будет гораздо более точным, и группа крови «восстановится».
Также причиной «изменения» группы крови может стать панагглютинация. При этом явлении кровь пациента вступает в реакцию со всеми диагностическими сыворотками, приводя к склеиванию эритроцитов. Это встречается у тяжелобольных пациентов при хронической почечной, печеночной недостаточности, гематологических и онкологических заболеваниях. Чтобы избавиться от явления панагглютинации, необходимо прогреть планшет в термостате, после чего будет получен верный результат.
Кто такие химеры и почему их кровь столь необычна?

Казалось бы, поменять группу крови или резус-фактор действительно невозможно. Однако существует поистине уникальное явление — химеризм. Чтобы разобраться в этом, MedAboutMe обратился к греческой мифологии. Химера — это существо, имеющее голову льва, тело козы и хвост змеи, которое обладало нечеловеческой силой и было предвестником несчастий. В биологии же химерами называют организмы, которые имеют генетически разнородный материал. Встречается ли такое среди людей?
Примерами естественного и природного химеризма могут быть близнецы. Считается, что во время нахождения в утробе матери плоды обмениваются тканями, а также кровью. При этом нормальная физиологическая реакция иммунитета (отторжение чужеродного материала) угнетается. Интересно, что нередко встречается так называемый феномен исчезнувшего близнеца, когда один плод в утробе матери «поглощает» другой, присваивая его клетки, которые продолжают развиваться в его организме. Таким образом у одного человека могут быть обнаружены сразу две группы крови или же два разных резус-фактора.
Случаи искусственного химеризма встречаются крайне редко. Это явление связано с пересадкой донорских органов или многократным переливанием чужеродной крови первой группы пациенту со второй, третьей или четвертой группой.

Факт!
Один из самых уникальных случаев за всю медицинскую практику произошел в Австралии. Девятилетней девочке по имени Деми Ли Бренанн понадобилась трансплантация печени. Хирургическое вмешательство прошло успешно, но после него в организме ребёнка начали происходить поистине «магические» процессы. Как говорят врачи, кровь девочки из первой группы с резус-отрицательным фактором стала резус-положительной. Анализы показали, что стволовые кровяные клетки донорской печени попали в костный мозг юной пациентки и взяли под контроль ее иммунную систему. Таким образом отпала и необходимость в приеме иммуносупрессивных препаратов: новый орган не воспринимался иммунитетом как нечто чужеродное.
Группы крови – вирусно-генетическое заболевание человека, обезьян и других животных / Тюняев А.А. // Вестник новых медицинских технологий – 2011 – №1
Причины ошибок при исследовании групповой принадлежности крови и меры их предупреждения / Лунина Г. В. // Проблемы науки – 2019 – №7
Ошибки первичного определения группы крови лечащим врачом / Жибурт Е. Б., Караваев А. В., Глазов К. Н. и др. // Вестник Национального медико-хирургического Центра им. Н.И. Пирогова – 2012 – №3
Ошибки при определении групп крови
Регистрационные удостоверения
Разновидности ошибок при определении групп крови: технические, вызванные применением некачественных реагентов, обусловленные биологическими особенностями анализируемых образцов.
Технические причины
- Некорректное расположение реагентов на планшете.
- Нарушение количественного отношения цоликлонов и эритроцитов.
- Недостаточная стерильность планшетов и пипеток.
- Неверная запись в историю болезни.
- Несоблюдение времени реакции агглютинации. В случае ожидания менее 5 минут реакция может не наступить при наличии слабых агглютиногенов. При передержанной реакции подсыхание капель с краев может симулировать ложноположительный результат.
- Температура воздуха свыше 25 °C. Рекомендуется использовать специальные реагенты с поправкой на температурные условия, опускать внешнюю часть планшета в холодную воду.
- Недостаточное или избыточное центрифугирование. В первом случае возможны ложноположительные результаты, во втором – ложноотрицательные.
Низкое качество реагентов
- Титр цоликлонов менее 1:32, использование просроченных реагентов вызывают позднюю или слабо выраженную реакцию.
- Загрязнение и недостаточная консервация цоликлонов и стандартных эритроцитов вызывает «бактериальную» агглютинацию.
Биологические особенности эритроцитов
- Слабые формы антигенов эритроцитов вызывают позднюю и слабо выраженную агглютинацию. Во избежание ошибок определения групп крови осуществляют повторное исследование с другой серией цоликлонов и увеличенным временем реакции, применяют моноклональные антитела Анти-Aсл., проводят типирование перекрестным способом со стандартными эритроцитами.
- «Панагглютинация» вызывает неспецифическую агглютинацию со всеми сыворотками. Онкологические и гематологические пациенты попадают в группу риска. Для устранения «аутоагглютинации» используют трехкратное отмывание эритроцитов. Планшет прогревают в течение 5 минут в термостате при 37 °C. В ряде случаев предварительно подогревают пробирку, реактивы, раствор NaCl.
- «Монетные столбики» эритроцитов. По окончании исследования в поле реакции рекомендуется добавить 1 – 2 капли 0,9 % раствора NaCl и покачать планшет.
- Неполная агглютинация. Частичная агглютинация эритроцитов может возникать после пересадки пациенту костного мозга или в первые месяцы после трансфузии крови 0(I). Для окончательного типирования антигенов по системам AB0 и Резус рекомендуется использование ID-гелевых карт.
Биологические особенности антител
- Выявление иммунных антител, возникших в результате предшествующей сенсибилизации. Больному с иммунными антителами требуется индивидуальный подбор донора.
- Возникновение «монетных столбиков». Сомнительный результат подтверждают со стандартными эритроцитами 0(I). Для распознавания истинной агглютинации добавляют изотонический раствор и покачивают планшет.
- Отсутствие Анти-A и Анти-B-антител. Встречается у младенцев и больных с угнетением гуморального иммунитета.
- Присутствие в сыворотке специфических и неспецифических холодовых антител. В случае наличия неспецифических агглютининов агглютинация пропадает во время проведения исследования при 37 °C. Взаимодействие сыворотки со стандартными эритроцитами 0(I) говорит о присутствии специфических холодовых антител. Специфичность антител определяется с помощью типированных по системам P и MNS эритроцитов.
Список литературы
- Рагимов, А.А. Трансфузионная иммунология/А.А. Рагимов, Н.Г. Дашкова. — М.: Медицинское информационное агентство, 2004. — 279 с.
- Шевченко, Ю.Л. Безопасное переливание крови/Ю.Л. Шевченко, Е.Б. Жибурт. — СПб.: Питер, 2000. — 308 с.
Патенты
Галерея 1

Планшет для типирования крови человека по антигенам эритроцитов
Регистрационное удостоверение на медицинское изделие. ТУ 22.29.29−001−06125010−2017. № РЗН 2018/6730 от 02 марта 2020 года

Планшет для типирования крови человека по антигенам эритроцитов
Приложение к регистрационному удостоверению на медицинское изделие. ТУ 22.29.29−001−06125010−2017. № РЗН 2018/6730 от 02 марта 2020 года

Набор реагентов для изосерологических исследований in vitro (Иммуногем-Сангвитест)
Регистрационное удостоверение на медицинское изделие. ТУ 21.20.23-002-06125010-2018. № РЗН 2019/8361 от 02 марта 2020 года

Набор реагентов для изосерологических исследований in vitro (Иммуногем-Сангвитест)
Приложение к регистрационному удостоверению на медицинское изделие. ТУ 21.20.23-002-06125010-2018. № РЗН 2019/8361 от 02 марта 2020 года
Галерея 2

Патент на промышленный образец 105908
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович, генеральный директор ООО

Патент на промышленный образец 109688
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович

Патент на промышленный образец 109689
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович
Выводы:
У детей вакцинированных эпидемическим паротитом по индивидуальному плану наблюдается вторичная иммунологическая недостаточность с угнетением клеточного звена и поликлональной активацией гуморального звена иммунитета.
Изучение иммунного статуса у детей, получавших вакцинацию по индивидуальному плану диктует необходимость разработки эффективных методов оздоровления с включением в комплекс лечения имунокоррегирующей терапии.
Список литературы
1. Зверевв В., Юминова Н.В. Эффективность вакцинации против кори и эпидемического паротита, Инф. бюл. Вакцинация 2000; 11 (5):10-1.
2. Назиров Ф.Г. Состояние и перспективы развития педиатрической службы в свете реализации государственных программ реформирования здравоохранения и «Здоровое поколение». Журн. Педиатрия №2-3. -2000. С. 8-11.
3. Семенов Б.Ф., Баранов А.А. Вакцинопрофилактика при нарушениях здоровья. М.Мсоюз педиатров России. 2001.
4. Флетчер Р., Флетчер С., Вангер Э. Клиническая эпидемиология (основы доказательной медицины), М., Медиа Сфера, 1998; 345.
5. ЯрцевМ.Н., ЯковлеваК.П. Физиология и патология иммунной системы. 2004; 2: 11-9.
6. Toscani L., et al: Comparison of the efficacy of various mumps vaccine strains: Buckley R.H. J Allergy ClinImmunol 2002; 109: 747-57.
ПРИЧИНЫ ОШИБОК ПРИ ИССЛЕДОВАНИИ ГРУППОВОЙ ПРИНАДЛЕЖНОСТИ КРОВИ И МЕРЫ ИХ ПРЕДУПРЕЖДЕНИЯ
Лунина Г.В.
Лунина Галина Владимировна — врач, клиническая лаборатория диагностики, Отдел контроля качества и клинической лабораторной диагностики, Центр крови Белгородской области г. Белгород ОЗК №3, г. Губкин
Ошибки при определении группы крови, возникают при нарушении техники выполнения исследования или в случае трудноопределимых групп крови.
1. Технические ошибки:
• ошибочный порядок расположения реагентов;
• использование сывороток с истёкшем сроком годности;
• использование инфицированных сывороток;
• использование сывороток с титром ниже 32;
• использование одной палочки при смешивании сывороток разных групп и крови;
• нарушение соотношения между стандартными сыворотками и исследуемых эритроцитов (эритроцитов должно быть в 5-10 раз меньше, чем сыворотки);
• нарушение соотношений между эритроцитами и моноклональными реагентами (цоликлоны) (2-3:10)
• не соблюдение температурного режима (не ниже 15°С и не выше 25°С);
• преждевременная оценка результатов (ранее 5 минут);
• за агглютинацию принимают монетные столбики, если не добавляется 0,9% раствор хлорида натрия;
• недостаточно высокое качество используемых для исследования реагентов.
2. Ошибки биологического характера:
• способность эритроцитов давать агглютинацию со всеми стандартными сыворотками;
• у людей с заболеванием крови, печени, почек, хроническими процессами возможен процесс агглютинации эритроцитов с собственной сывороткой (для исключения ошибки тарелку поставить в термостат при 37°С на 5-6 минут);
• полная панагглютинация- необходимо исследовать агглютинины А и В в слюне;
• феномен Томпсона — инфицированная кровь даёт неспецифическую агглютинацию;
• у новорожденных агглютиногены А и В не достаточно активны и поэтому исследования должны проводиться с сыворотками с высоким титром антител;
• слабые агглютиногены А2, А3;
3. Трудноопределяемые группы крови.
Антиген А нельзя считать однородным, существует два основных его подтипа: А! и А2. Эритроциты с подтипом агглютиногена А! встречают намного чаще, чем с подтипом А2 (88% и 12% соответственно). В соответствии с этим группа А(П) имеет две подгруппы: А(П) и А2(П), а группа АВ(1У) — АВ(1У) и А2В(1У) (Таблица 1.).
Таблица 1. Трудноопределяемые группы крови
Группа Подгруппа Агглютиногены в эритроцитах Агглютинины в сыворотке крови Распространённость
0аР нет нет а и в 33,5%
Ар (II) А1(П) А2(П) А1 В1 в (а2- крайне редко) Р(аг в 20% случаев) 32,1% 5,7%
Ва(Ш) нет В а 20,6%
АВо(^) АВ(1У) А2В(1У) А1 и В А2 и В нет (а2- крайне редко) нет(аг в 20% случаев) 6,8% 1,3%
Группы крови по системе АВ0
Агглютиноген А j и А2 отличаются друг от друга по свойствам.
• подтип А1 обладает большей адсорбционной возможностью по сравнению с агглютиногеном А2, он сильнее адсорбирует агглютинин а из сыворотки, поэтому его называют сильным, а подтип А2 — слабым.
• эритроциты с агглютиногеном А2 имеют более низкую агглютинабельность.
• подгруппы с агглютиногенами А1 и А2 обладают различными свойствами сывороток. Сыворотка подгрупп А2 (II) и А2В (IV) довольно часто содержит агглютинин, названный Ландштейнером и Левином экстраагглютинином aj, дающим агглютинацию только с эритроцитами А1 и не дающим агглютинации с эритроцитами А2. В то же время в сыворотке подгрупп A(II) и AB(IV) довольно редко, но встречается экстраагглютинин a2, не агглютинирующий эритроциты Aj, а дающий агглютинацию с эритроцитами А2.
Существуют варианты эритроцитов с ещё более слабовыраженными агглютинабельными свойствами, что связано с наличием в них подтипов А3, А4, Az и др. Несмотря на то, что эти слабые антигены встречают довольно редко, но они имеют определённое клиническое значение.
• групповой антиген В отличается большей однородностью. Описанные редкие его варианты (В2, В3, Bw и др.) существенного клинического значения не имеют;
• позже в первой группе крови 0(1) была найдена специфическая субстанция, также обозначенная символом «0». Фактор 0 — агглютиноген, присущий эритроцитам групп 0(I), A2(II), A2B(IV).
Для эритроцитов всех групп характерно наличие субстанции Н, её считают общим веществом-предшественником. Субстанцию Н чаще встречают у лиц с первой группой крови, в других же она содержится в незначительном количестве;
• в настоящее время известны так называемые кровяные химеры, обусловленные одновременным пребыванием в организме человека эритроцитов, принадлежащих двум фенотипам АВО. В естественных условиях явление кровяной химеры встречают у близнецов. Оно может также появиться при пересадке аллогенного костного мозга или переливании массивных объёмов крови. При определении группы крови и резус -принадлежности в условиях наличия кровяной химеры, как правило, получают искажённый результат (во всех сомнительных результатах направить образцы крови в специализированную лабораторию).
Список литературы
1. Приказ Минздрава России от 09.01.1998 № 2 «Об утверждении Инструкции по иммуносерологии».
2. Приказ Минздрава России от 25.11.2002 № 363 «Об утверждении Инструкции по применению компонентов крови».
3. Требования по проведению иммуногематологических исследований доноров и реципиентов на СПК и в ЛПУ. Методические указания № 2001/109. Минздрав России, НИИ гематологии и трансфузиологии, Санкт-Петербург, 2002.
4. Минеева Н.В. Группы крови человека. Основы иммуногемотологии. СПб., 2004. 188 с.
Библиографическое описание:
Тактаева, Е. В. Группа крови человека и проблемы при ее определении / Е. В. Тактаева. — Текст : непосредственный // Молодой ученый. — 2019. — № 2 (240). — С. 64-66. — URL: https://moluch.ru/archive/240/55598/ (дата обращения: 29.01.2023).
Группа крови — это генетически наследуемые признаки, не меняются в течение жизни в естественных условиях и описание индивидуальных антигенных характеристик эритроцитов, которые определяют с помощью методов идентификации специфических групп углеводов и белков, помещенных в мембраны эритроцитов человека или животного. Группа крови также характеризует системы эритроцитарных антигенов, или агглютиногенов (веществ, которые организм человека рассматривает как чужеродные, потенциально опасные, против которых начинает производить собственные антитела, см. агглютиноген), которые контролируются определенными локусами (конкретный участок в хромосоме), содержащие различное количество аллельных (варианты последовательности нуклеотидов ДНК в локусе) генов, таких, например., как A, B и 0 системе AB0. Наличие у людей разных Группа крови обусловлена генетическими факторами, которые содержатся в длинном плече 9-й хромосомы.
К началу 20-го века никто и не подозревал, что кровь может быть разной. Переворот в этой области знаний сделал австрийский врач Карл Ландштейнер, который обнаружил и исследовал три антигены А, В и С. В 1901 году он поставил необычный эксперимент: он принимал сыворотки крови одних людей и смешивал с эритроцитами других, а именно взяв кровь себе и пяти своих сотрудников, отделив сыворотку от эритроцитов с помощью центрифуги и смешал отдельные образцы эритроцитов с сывороткой крови разных лиц и собственной. Некоторые сыворотки склеивали эритроциты, а некоторые — нет. И в зависимости от наличия или отсутствия этой реакции (агглютинации) были обнаружены группы крови.
В совместной работе с Л. Янским по наличию или отсутствию агглютинации Ландштейнер разделил все образцы крови на три группы: А, В и 0. Два года спустя ученики Ландштейнера, А. Штурли и А. Декастелло, открыли четвертую группу крови — АВ. Общепринятым является буквенно-цифровое обозначение Группы крови: первая — 0 (I), вторая группа — А (II), третья группа — В (iii), четвертая группа — АВ (IV). В среднеевропейской популяции по системе AB0 около 43 % людей имеют первую группу крови, 42 % — вторую, 11 % — третьего и около 4 % — четвертую. Группа крови по системе АВ0 отличают по наличию антигенов (агглютиногенов) на эритроцитах и антител (агглютининов) в сыворотке крови (табл. 1).
Эритроцит может обладать только антигеном А (II группа крови), только антигеном В (III группы крови) или и А, и В одновременно (IV группа крови). Если же на поверхности эритроцитов нет ни одного из этих антигенов, значит, он относится к клеткам I (0) группы крови.
Кровь всегда готова к тому, что у нее могут попасть посторонние эритроциты. Если у человека есть антиген А (II группа крови), то в плазме обязательно присутствуют антитела бета. Как только в организм попадает эритроцит, что несет на себе антиген В, антитела тут же прилепятся чужака, как метка. Это передаст иммунной системе сигнал об опасности. У обладателей антигена В (III группы крови) функцию антитела играют альфа распознают эритроциты с А-антигеном.
Таблица 1
Основные факторы, обусловливающие групповую принадлежность крови по системе АВ0
|
Группа крови |
Антигены (агглютиногены) |
Антитела (агглютинины) |
|
І |
0 |
α та β |
|
ІІ |
А |
β |
|
ІІІ |
В |
α |
|
ІV |
АВ |
Отсутствуют |
Антигены системы АВО развиваются на эритроцитах еще до рождения ребенка. Например, антиген А находится на эритроцитах 37 дневного плода. Но полное развитие антиген получает после рождения, через несколько месяцев. У взрослых людей кроме антигенов А, В еще имеется антиген Н. Он предшественник антигенов А, В, но может быть и на поверхности эритроцитов первой группы.
В 1911 г обнаружены две подгруппы антигена А, а именно А1 и А2. Между собой они могут отличаться как качественно, так и количественно. Качественно — это особенности в биохимической структуре сахаров. А количественно — это большее количество детерминант в антигене А1. Поэтому факту определены подгруппы А2 и А2В.
Распознать А2 подгруппу можно по сильной активности взаимодействия анти-Н с А2 клетками чем с А1.
Для клинической практики наибольшее значение имеют две классификации Группа крови человека: система AB0 и резус-система (Rhesus) — вследствие того, что эти системы обладают наибольшей антигенной силой. При каждом переливании крови от человека к человеку обязательно учитывают совместимость именно с этими двумя системами, поскольку в случае переливания человеку другой (несовместимой) группы крови происходит агглютинация (склеивание) и гемолиз (разрушение) эритроцитов, что может привести смерти.
Наследование различных групп крови АВО-системы определяется различным сочетанием трех аллелей одной аллеломорфных группы генов, которые обозначаются как JA, β и I ‘и расположены в девять паре хромосом.
Аллель JA определяет образование антигена А на поверхности эритроцитов и агглютинина β в плазме крови, аллель JB — образование антигена В на эритроцитах и агглютинина α в плазме и, в конце концов, за аллеля J отсутствуют антигены А, В на поверхности эритроцитов и содержатся агглютинины α и β в плазме.
Генетические исследования показали, что в этой системе существуют следующие соотношения между генотипом и его фенотипическим проявлением:
‒ генотипы JAJA и JAJ0 дают одинаковый фенотип А с антигеном А и агглютининов β;
‒ генотипы JBJB и JBJ ° обусловливают одинаковый фенотип В с антигеном В и агглютининов α;
‒ генотип JAJB определяет фенотип АВ с антигенами А и В, но без агглютининов α и β;
‒ генотип J ° J ° вызывает фенотип 0 без антигенов А и В, но с агглютининами α и β.
Гены JA и JB в отношении гена J ° ведут себя доминантно.
Группы крови человека можно определить стандартными эритроцитами, цоликлонами (моноклональные антитела) как на плоскости, так и гелевыми технологиями. При определении могут возникнуть ошибки. Технические (например, неправильная маркировка крови и реагентов, неправильное соотношение, срок годности и т. д.), невысокое качество реактивов. Но самое важное это ошибки, обусловленные индивидуальными особенностями антигенов эритроцитов АВО. Поскольку антигены имеют сложную химическую структуру — гликолипиды, гликопротеины, гликозидные остатки, прикрепленные к олигосахаридным цепочкам. Даже сами олигосахаридные цепочки различны у антигенов А и В. Поэтому важно применять широкий спектр антител для определения антигенов. Количество детерминант на эритроцитах различное. При большом их количестве реакция агглютинации сильнее. Окружающая среда может влиять на модификацию антигенов. Детерминанты ослабевают или утрачиваются у онкологически больных людей, лейкозами. Эти изменения мало изучены. Они играют роль в нарушении синтеза трансфераз, ответственных за формирование антигенных детерминант А и В. Так же изменения имеют место при вирусной и бактериальной природе. При таких случаях возможно приобретение, например, В -подобного антигена. Он образуется вследствие влияния микроорганизмов взамен антигена А на мембране эритроцитов. Микроорганизмы выделяют ацетилазы, которые воздействуют на антиген А и последний становится похожим на антиген В. И что интересно, приобретенный антиген В не агглютинирует собственными анти-В антителами. Часто ошибки происходят при не выявлении антигена А2 в группе крови А или в группе крови А2В. Существуют ошибки, связанные со специфической и неспецифической агглютинацией. Это может связано наличием аутоантител как на эритроцитах, так и в сыворотке аллоантител.
Литература:
- Лавряшина М. Б., Толочко Т. А., Волков А. Н. Аллоантигены крови человека: Учеб. пособ. — Кемерово, 2006; Практическая трансфузиология / Под ред. Г. И. Козинке. — М., 2005.
- Википедия — статья «Группа крови».
- Минеева Н. В. Группы крови человека. Основы иммуногематологии. Санкт-Петербург 2010 г. Издание 2-е.
Основные термины (генерируются автоматически): группа крови, антиген А, эритроцит, III, поверхность эритроцитов, агглютинин, антиген, антиген В, система, сыворотка крови.
Ошибки при определении групп крови
Регистрационные удостоверения
Разновидности ошибок при определении групп крови: технические, вызванные применением некачественных реагентов, обусловленные биологическими особенностями анализируемых образцов.
Технические причины
- Некорректное расположение реагентов на планшете.
- Нарушение количественного отношения цоликлонов и эритроцитов.
- Недостаточная стерильность планшетов и пипеток.
- Неверная запись в историю болезни.
- Несоблюдение времени реакции агглютинации. В случае ожидания менее 5 минут реакция может не наступить при наличии слабых агглютиногенов. При передержанной реакции подсыхание капель с краев может симулировать ложноположительный результат.
- Температура воздуха свыше 25 °C. Рекомендуется использовать специальные реагенты с поправкой на температурные условия, опускать внешнюю часть планшета в холодную воду.
- Недостаточное или избыточное центрифугирование. В первом случае возможны ложноположительные результаты, во втором – ложноотрицательные.
Низкое качество реагентов
- Титр цоликлонов менее 1:32, использование просроченных реагентов вызывают позднюю или слабо выраженную реакцию.
- Загрязнение и недостаточная консервация цоликлонов и стандартных эритроцитов вызывает «бактериальную» агглютинацию.
Биологические особенности эритроцитов
- Слабые формы антигенов эритроцитов вызывают позднюю и слабо выраженную агглютинацию. Во избежание ошибок определения групп крови осуществляют повторное исследование с другой серией цоликлонов и увеличенным временем реакции, применяют моноклональные антитела Анти-Aсл., проводят типирование перекрестным способом со стандартными эритроцитами.
- «Панагглютинация» вызывает неспецифическую агглютинацию со всеми сыворотками. Онкологические и гематологические пациенты попадают в группу риска. Для устранения «аутоагглютинации» используют трехкратное отмывание эритроцитов. Планшет прогревают в течение 5 минут в термостате при 37 °C. В ряде случаев предварительно подогревают пробирку, реактивы, раствор NaCl.
- «Монетные столбики» эритроцитов. По окончании исследования в поле реакции рекомендуется добавить 1 – 2 капли 0,9 % раствора NaCl и покачать планшет.
- Неполная агглютинация. Частичная агглютинация эритроцитов может возникать после пересадки пациенту костного мозга или в первые месяцы после трансфузии крови 0(I). Для окончательного типирования антигенов по системам AB0 и Резус рекомендуется использование ID-гелевых карт.
Биологические особенности антител
- Выявление иммунных антител, возникших в результате предшествующей сенсибилизации. Больному с иммунными антителами требуется индивидуальный подбор донора.
- Возникновение «монетных столбиков». Сомнительный результат подтверждают со стандартными эритроцитами 0(I). Для распознавания истинной агглютинации добавляют изотонический раствор и покачивают планшет.
- Отсутствие Анти-A и Анти-B-антител. Встречается у младенцев и больных с угнетением гуморального иммунитета.
- Присутствие в сыворотке специфических и неспецифических холодовых антител. В случае наличия неспецифических агглютининов агглютинация пропадает во время проведения исследования при 37 °C. Взаимодействие сыворотки со стандартными эритроцитами 0(I) говорит о присутствии специфических холодовых антител. Специфичность антител определяется с помощью типированных по системам P и MNS эритроцитов.
Список литературы
- Рагимов, А.А. Трансфузионная иммунология/А.А. Рагимов, Н.Г. Дашкова. — М.: Медицинское информационное агентство, 2004. — 279 с.
- Шевченко, Ю.Л. Безопасное переливание крови/Ю.Л. Шевченко, Е.Б. Жибурт. — СПб.: Питер, 2000. — 308 с.
Патенты
Галерея 1

Планшет для типирования крови человека по антигенам эритроцитов
Регистрационное удостоверение на медицинское изделие. ТУ 22.29.29−001−06125010−2017. № РЗН 2018/6730 от 02 марта 2020 года

Планшет для типирования крови человека по антигенам эритроцитов
Приложение к регистрационному удостоверению на медицинское изделие. ТУ 22.29.29−001−06125010−2017. № РЗН 2018/6730 от 02 марта 2020 года

Набор реагентов для изосерологических исследований in vitro (Иммуногем-Сангвитест)
Регистрационное удостоверение на медицинское изделие. ТУ 21.20.23-002-06125010-2018. № РЗН 2019/8361 от 02 марта 2020 года

Набор реагентов для изосерологических исследований in vitro (Иммуногем-Сангвитест)
Приложение к регистрационному удостоверению на медицинское изделие. ТУ 21.20.23-002-06125010-2018. № РЗН 2019/8361 от 02 марта 2020 года
Галерея 2

Патент на промышленный образец 105908
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович, генеральный директор ООО

Патент на промышленный образец 109688
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович

Патент на промышленный образец 109689
Планшет для типирования крови человека по антигенам эритроцитов. Патентообладатель, автор: Чмелев Вадим Мстиславович
- Что такое резус-фактор?
- Чем опасна беременность при отрицательном резус-факторе?
- Каким образом происходит резус-изоиммунизация?
- Каковы риски при первой беременности?
- Какие диагностические процедуры нужны беременной с резус-отрицательной кровью?
- Зачем определять резус-фактор у мужчин?
- Когда необходимо введение иммуноглобулина?
- В каких ситуациях необходима дополнительная профилактика резус-сенсибилизации?
Содержание:
Отрицательный резус-фактор при беременности может приводить к серьезным осложнениям со стороны развития малыша. Тем не менее вопрос резус-конфликта хорошо изучен, что позволяет не только своевременно диагностировать, но и успешно профилактировать неблагоприятные последствия.

О том, какие действия необходимо предпринять во время беременности, должна быть предупреждена каждая мама с отрицательной кровью.
Что такое резус-фактор?
Резус-фактор — это белок, располагающийся на поверхности эритроцитов. Люди, у которых он есть, обладают резус-положительной кровью, а у которых отсутствует — резус-отрицательной. Наличие белка — индивидуальная особенность организма, которая может наследоваться будущим поколением.
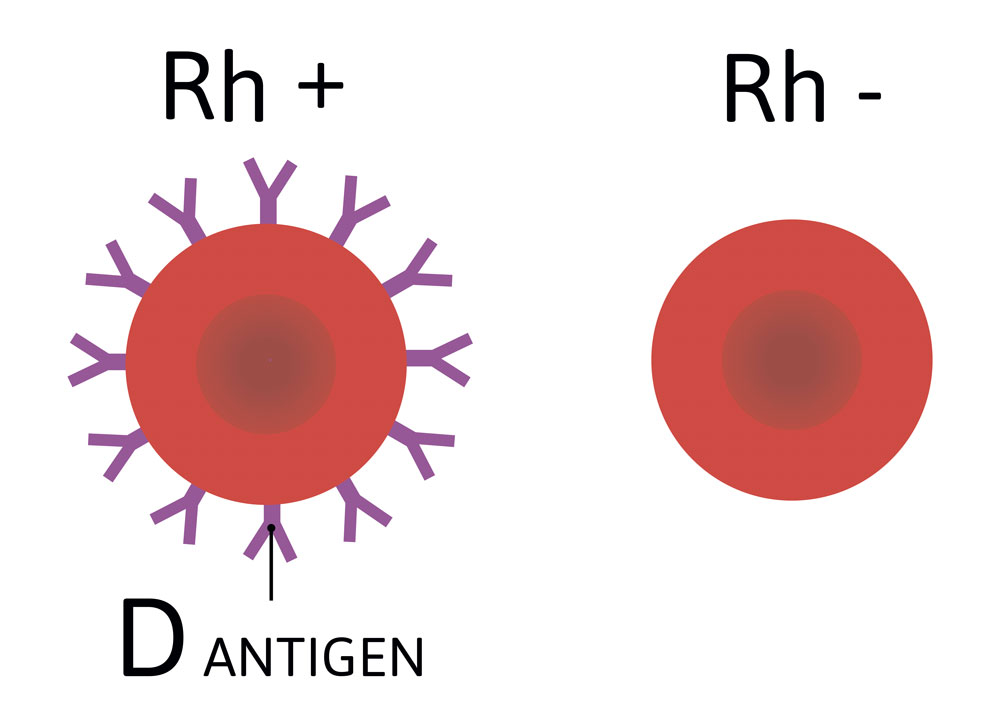
Данные о том, какой процент людей имеют резус-отрицательную кровь, противоречивы. Но нет сомнений в том, что он встречается гораздо реже положительной: от 8 до 25%, согласно различным статистическим анализам.
Особую роль резус-фактор играет во время беременности. Если у матери положительный резус, то ее кровь всегда будет совместима с кровью ребенка, если отрицательный — то шанс на успех лишь 50%.
Чем опасна беременность при отрицательном резус-факторе?
Если у мамы резус-отрицательная кровь, а будущему малышу передался положительный резус от отца, то может возникнуть несовместимость крови, которую называют резус-конфликт, или резус-сенсибилизация/изоиммунизация. Такое состояние закономерно приводит к развитию гемолитической болезни плода.
Каким образом происходит резус-изоиммунизация?
Во время беременности эритроциты плода проникают через плацентарный барьер в кровоток матери. Это происходит не у каждой женщины и вероятность проникновения зависит от срока.
Важно!
В течение 1-го триместра попадание эритроцитов из крови малыша в кровь мамы отмечается в 5-7% случаев, во 2-м триместре — в 15-16% и в 3-м триместре — у 29- 30% женщин.
Иммунитет беременной при попадании чужеродного белка отвечает выработкой специфических иммуноглобулинов. Сначала активируются IgM антитела. Так как они обладают высокой молекулярной массой, им не удается преододлеть плацентарный барьер. Но следующим этапом изоиммунизации становится образование IgG антител, которые проникают в кровоток плода спокойно и беспрепятственно. Материнские иммуноглобулины взаимодействуют с рецепторами лимфоцитов и макрофагов, что приводит к гемолизу эритроцитов будущего малыша.
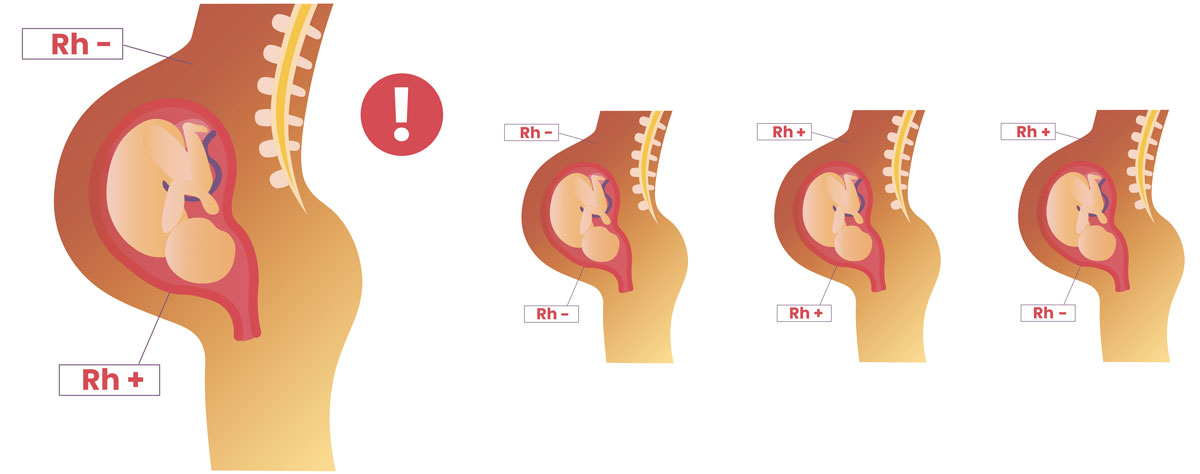
Распад эритроцитов приводит к анемии, и активизация очагов кроветворения вне костного мозга. Клетки печени перегружаются продуктами распада гемоглобина, нарушается ее способность синтезировать белок. Анемия прогрессирует, а значит, плод начинает страдать от недостатка кислорода в крови. У малыша развивается гипердинамический тип кровообращения с постепенным формированием сердечной недостаточности. Патологическая цепочка приводит к увеличению размеров печени, селезенки и формированию анасарки. При отсутствии проведения внутриутробного лечения малыш может погибнуть.
Важно!
Опасность резус-сенсибилизации в том, что у беременной отсутствуют специфические жалобы. Только при развитии тяжелой анемии и водянки плода мама отмечает снижение интенсивности шевелений. В этом случае слабая двигательная активность плода свидетельствует о развитии у него сердечной недостаточности.
Иногда резус-конфликт приводит к выкидышу, а после родов становится причиной гемолитической желтухи новорождённых. При этом в крови младенца разрушается значительное количество эритроцитов, кожа новорождённого желтеет, страдает головной мозг и может развиться водянка.
Важно!
Гемолитическая болезнь новорожденного в Российской Федерации диагностируется приблизительно у 0,6%-1% малышей.

Чем опасна беременность при отрицательном резус-факторе?
Во время первой беременности, как правило, резус-конфликт не дает выраженных клинических проявлений. Гемолитическая болезни плода (ГБП) встречается редко, так как попадание эритроцитов в кровоток матери происходит в основном на поздних сроках беременности или во время родов. Первичный иммунный ответ не успевает сформироваться и оказать негативное влияние на развитие малыша. Таким образом, резус-сенсибилизация чаще всего проявляется легкой анемией по причине позднего начала распада эритроцитов ребенка незадолго до родов или сразу после рождения.
Но вероятность ГБП при первой беременности повышается, если изоиммунизация женщина произошла ранее вследствие других причин. Например, при переливании компонентов резус-положительной крови в анамнезе.
Какие диагностические процедуры нужны беременной с резус-отрицательной кровью?
Если пара планирует беременность, то, как правило, во время прегравидарной подготовки женщина сдает анализ для уточнения группы крови и резус-фактора. Это позволяет заблаговременно информировать будущую маму о перечне необходимых мероприятий, которые ей предстоят во время вынашивания малыша.
Вне зависимости от того, какие обследования проходила женщина ранее, на первом визите в женскую консультацию ей определяют группу и резус-принадлежность крови.
Резус-отрицательная беременная получает направление на исследование антирезусных антител.
Если антитела отсутствуют, то для контроля данный анализ выполняется трехкратно за весь период вынашивания:
-
при постановке на учет;
-
в 18-20 недель беременности;
-
в 28 недель беременности.
Если у будущей мамы выявлены антирезусные антитела, её направляют на консультацию в перинатальный центр для составления индивидуального диагностического плана и дальнейшего наблюдения.
Зачем определять резус-фактор у мужчин?
Чтобы предусмотреть развитие иммунологического конфликта между мамой и малышом, уточняют принадлежность крови у папы.
Поэтому определять резус-фактор следует партнерам всех резус-отрицательных беременных.
Если у мужчины, как и у женщины, отрицательная кровь, то малыш с точностью унаследует резус от родителей. Так как в данном случае риск изоиммунизации сведен к нулю, определение антирезусных антител не проводится.
При резус-положительной принадлежности мужа спрогнозировать то, какая кровь будет у малыша невозможно без дополнительного анализа — вероятность 50/50. В этом случае обследование беременной проводится согласно плану, описанному выше.
Современная медицина сделала большой шаг вперед. Теперь в случае несовпадения резус-отрицательной крови у партнеров женщине предлагают определить резус-фактор малыша по циркулирующим в крови матери внеклеточным фрагментам плодовой ДНК. Целесообразно рекомендовать данный анализ совместно с первым пренатальным скринингом на сроке 12 недель беременности. Это неинвазивное безопасное дорогостоящее исследование, которое пока что не входит в систему обязательного медицинского страхования.
Обратите внимание!
Вышеуказанный метод диагностики имеет чувствительность и специфичность 98-100%.
Если у плода подтверждается отрицательный резус-фактор, то определение антирезусных антител в крови матери не проводится.
Таким образом, определение резус-принадлежности мужчины и будущего малыша позволяет избежать женщине лишних анализов и волнений относительно возможного конфликта.
Когда необходимо введение иммуноглобулина?
Введение антирезусного иммуноглобулина во время беременности и в послеродовом периоде — метод специфической профилактики, позволяющий предотвратить резус-конфликт.
Согласно клиническим рекомендациям МЗ РФ, если у беременной резус-отрицательной пациентки отсутствуют антирезусные антитела в 28 недель, ей рекомендовано ввести дозу иммуноглобулина человека антирезус Rho[D] в сроки не позднее 30 недель.
При резус-отрицательной принадлежности крови мужа или плода введение иммуноглобулина не требуется.
Если в результате диагностики у женщины до 28 недель беременности выявлены антирезусные антитела, ей необходимо:
-
расширенное обследование для определения степени тяжести резус-изоиммунизации;
-
назначение терапии;
-
динамическое наблюдение и контроль уровня антител;
-
экстренное родоразрешение при необходимости.

Обратите внимание!
Риск развития резус-сенсибилизации у отрицательной мамы, беременной положительным плодом, при отсутствии профилактики составляет около 16%. Своевременное введение иммуноглобулина снижает риск до 0,2%.
После родов у ребенка определяют группу крови и резус-фактор, на основании чего принимают решение о необходимости повторного введения иммуноглобулина. В случае резус-отрицательной принадлежности крови новорожденного проведение специфической профилактики не показано, так как потенциальный конфликт исключен.
При положительном резусе малыша рекомендовано внутримышечное введение иммуноглобулина в дозе 1500 ME (300 мкг). Профилактику проводят сразу после получения результатов исследования крови ребенка, предпочтительно в течение первых двух часов. В связи с отягчающими обстоятельствами можно иммунизировать маму позже, но для достижения желаемого эффекта не желательно превышать перерыв в 72 часа после родов.
Своевременная профилактика сохраняет отрицательный иммунный статус в отношении антирезусных антител, что позволяет женщине без опасений рожать в будущем. Отказ от введения иммуноглобулина повышает вероятность конфликта и ГБН с каждой последующей беременностью.

В каких ситуациях необходима дополнительная профилактика резус-сенсибилизации?
Заброс эритроцитов плода в кровоток матери происходит не только во время родов. Проведение инвазивных диагностических и лечебных вмешательств во время беременности повышают риск резус-иммунизации и требуют дополнительного введения иммуноглобулина.
К таким процедурам относятся:
-
биопсия ворсин хориона;
-
амниоцентез — пункция плодного пузыря;
-
кордоцентез — анализ пуповинной крови;
-
серкляж — наложение швов на шейку матки при истмико-цервикальной недостаточности;
-
редукция эмбриона(ов) при многоплодии;
-
повороты плода на головку при тазовом предлежании;
-
абдоминальная травма во время беременности;
-
дородовые кровотечения при угрозе прерывания беременности.
Помимо этого, профилактическое введение иммуноглобулина требуется при:
-
аборте;
-
самопроизвольном выкидыше;
-
неразвивающейся беременности;
-
антенатальной гибели плода;
-
внематочной беременности;
-
пузырном заносе.
На сегодняшний день выработан последовательный алгоритм ведения беременных с резус-отрицательной кровью. Своевременная диагностика, лечение и профилактика резус-конфликта позволяют женщине без осложнений выносить и родить здорового малыша не только в первую, но и в последующие беременности.
Надеемся, эта статья была вам полезна. Чтобы получать подобные материалы, подпишитесь на нашу рассылку. Она будет снабжать вас полезной и актуальной информацией не только во время беременности, но и в первые, самые сложные месяцы материнства.
Источники:
-
Неонатология. Клинические рекомендации / под ред. Н.Н. Володин, Д.Н. Дегтярев, Д.С. Крючко. М., ГЭОТАР-Медиа 2019. — С. 19-35.
-
Клинические рекомендации МЗ РФ «Резус-изоиммунизация. Гемолитическая болезнь плода», 2020 г.
-
Резус-сенсибилизация. Гемолитическая болезнь плода. Клинические рекомендации (протокол). М., 2017. 16 с.
-
White J, Qureshi H, Massey E, Needs M, Byrne G, Daniels G, et al. Guideline for blood grouping and red cell antibody testing in pregnancy. Transfus Med. 2016 Aug;26(4):246—63.
-
Клинические рекомендации МЗ РФ «Нормальная беременность», 2020 г.
-
American Academy of Pediatrics and the American College of Obstetricians and Gynecologists. Guidelines for perinatal care. 8th ed. Elk Grove Village, IL; Washington, DC; 2017.
Ошибки при определении резус-фактора
Выделяют
следующие причины возникновения ошибок
при определении резус-фактора:
-
технические
погрешности. -
биологические
особенности испытуемой крови
Технические
погрешности.
-
неправильное
соотношение между сывороткой и
эритроцитами; -
преждевременная
оценка результатов; -
оценка результатов
по высыхающей капле; -
использование
неактивных, инфицированных, загнивших
и с истекшим сроком сывороток; -
определение
резус-фактора в гемолизированном и
длительно хранящемся образце крови.
Биологические
особенности испытуемой крови:
-
снижение
агглютинабельности резус-антигена при
некоторых заболеваниях печени, почек,
системы крови; -
неспецифическая
агглютинация испытуемых эритроцитов.
При
получении сомнительных результатов
необходимо повторить исследование,
используя более чувствительные методы.
КЛИНИЧЕСКОЕ
ЗНАЧЕНИЕ ГРУППОВОЙ
Дифференциации.Учение о совместимости
Группа
крови любого человека индивидуальна.
Выше указывалось о существовании
множества антигенных систем крови.
Любой эритроцитарный, лейкоцитарный,
тромбоцитарный или плазменный антиген
может быть причиной иммунологической
совместимости. Однако основную роль
при определении совместимости играют
антигены системы АВО и Rh-Нr.
Несовместимость
крови донора и реципиента наступает
при вливании крови, содержащей антигены,
на которые у реципиента в плазме имеются
антитела. В таких случаях возникает
агглютинация и гемолиз эритроцитов.
Совместимость по системе аво
В
1907 г. Grile,
а в 1908 г. Ottenberg
первыми выдвинули положение о переливании
крови с учетом групповой совместимости.
Они установили,
что при переливании крови только
одноименных групп, или в случае, когда
сыворотка реципиента не агглютинирует
эритроциты донора гемотрансфузия будет
успешной. В случае, когда сыворотка
реципиента агглютинирует эритроциты
донора, развиваются тяжелые осложнения,
обусловленные агглютинацией и гемолизом
эритроцитов. На основании этих наблюдений,
был сделан абсолютно правильный вывод:
можно переливать только биологически
совместимую кровь.
Оттенберг,
изучая проблемы совместимости,
сформулировал правило:
агглютинируются эритроциты переливаемой
крови, а не крови реципиента, так как
аггглютинины донорской крови разводятся
в крови реципиента, их
титр становится низким
и они не могут агглютинировать его
эритроциты
По
правилу Оттенберга можно переливать
кровь, эритроциты которой не агглютинируются
сывороткой реципиента, т. е можно
переливать не только однгуппную кровь,
но при совместимости кровь других групп.
Согласно
правилу Оттенберга кровь других групп
можно переливать по схеме.







Кровь
первой группы можно переливать людям
всех остальных групп, так как эритроциты
группы 0(I)
не содержат агглютиногенов А и В,поэтому
не могут дать агглютинацию ни с какими
сыворотками.
Сыворотка
группы AB(IV) не содержит никаких
агглютининов, поэтому эритроциты других
групп не будут агглютинироваться.
Поэтому больным с группой крови AB(IV)
можно переливать кровь любой группы.
Учитывая такую совместимость групп
крови, были введены понятия «универсальный
донор» и «универсальный реципиент».
Соответственно лица группы 0(I)
отнесены к «универсальным донорам», а
группы AB(IV) к «универсальным реципиентам».
Однако,
необходимо помнить, что при переливании
большого количества иногруппной
совместимой крови больным с массивной
кровопотерей агглютинины плазмы донора
не получают достаточной степени
разведения плазмой реципиента, и могут
агглютинировать эритроциты больного,
вызывая посттрансфузионный шок. Поэтому
правило Оттенберга можно применять при
трансфузии не более 1 литра крови.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
При беременности может возникать иммунологическая несовместимости крови матери и плода по резус-фактору, реже по системе АВ0 и еще реже по некоторым другим факторам крови. В результате такой несовместимости возникает гемолитическая болезнь плода и новорожденного. В каких случаях необходимо делать укол антирезусного иммуноглобулина? На вопросы о резус-факторе и иммунологическом конфликте отвечают врачи медицинских клиник «Арт-Мед».
У внука (13,5 лет) при прохождении плановой медицинской комиссии обнаружили 0 (нулевой) резус фактор, группа крови 4. У матери группа 4, резус положительный. При этом нам просто сообщили об этом. Зная, что случай уникальный, необходимо ли нам предпринимать какие-то меры по формированию запаса крови для экстраординарных случаев? Нужно ли куда-то обращаться для наблюдения и прочее?
Вам необходимо обратиться в учреждение «Национальный научно-практический центр детской гематологии, онкологии и иммунологии им. Дмитрия Рогачева» г. Москва, ГСП-7, 117997, ул. Саморы Машела, д.1. Телефон: +7 495 287 65 70, факс: +7 495 664 70 90, электронная почта: info@fnkc.ru
У меня отрицательный резус фактор, у мужа положительный. Есть двое детей 2007 и 2011 года рождения. Оба ребенка с положительным результат фактором, антитела во время беременностей не появлялись, после родов оба раза ставили иммуноглобулин. Летом случилась замершая беременность, внутренний диаметр плодного яйца, когда началось кровотечение, по УЗИ был 3,4 мм на восьмой акушерской неделе. Провели чистку, иммуноглобулин не вводили, врач сказал, что на таком сроке не нужно. В январе по анализу крови антитела к резус фактору не обнаружены. Говорит ли это о том, что сенсабилизация не произошла? Можно ли планировать беременность? Какова вероятность резус конфликта?
Если нет антител, то сенсибилизация не произошла. Вероятность резус-конфликта примерно 5%.
Беременность вторая, первая закончилась выкидышем на 6-ой неделе (после чистки иммуноглобулин не вводили). У меня резус отрицательный, у супруга — положительный. С настоящей беременностью лежала в стационаре на сроке 6-8 недель, там мне ввели иммуноглобулин, но в выписных документах об этом ничего не написали. В ЖК анализов на антитела не делали, поверив мне на слово, что был введен иммуноглобулин и результат будет недостоверным, если анализ сделать. Сейчас срок 26 недель, перед тем как вводить мне иммуноглобулин на 28-й неделе, врач отправила сдавать анализ на антитела, по результатам которого она хочет узнать вводили мне в стационаре иммуноглобулин или нет? Какой будет результат анализа, если все — таки мне препарат в стационаре вводили? И как доктор определит титры появились в результате введения препарата или же эти титры появились в результате развивающегося резус-конфликта?
В Вашем случае, лучше всего, попытаться получить письменное подтверждение из стационара, где Вам ввели иммуноглобулин в сроке 6-8 недель. Вероятно, доктор хотела бы определить величину титра антител.
5-6 акушерских недель беременности, первые роды 12 лет назад, естественные, антител во время беременности не было, ребенок с положительным резус-фактором, иммуноглобулин не вводился. После замершей беременности в декабре прошлого года на сроке 5-6 недель сделали укол иммуноглобулина (перед уколом антител не было). Сейчас пришли анализы на антитела: титр 1: 16(1:32). Как на таком сроке они могли появиться? Если на УЗИ еще эмбриона не видно, кровеносная система еще толком не сформирована? Могли антитела остаться в таком количестве после укола иммуноглобулина полгода назад? И чем это грозит на таком сроке, беременность может замереть из-за этого? Когда антитела могут начать уничтожать эритроциты ребенка? Естественно, буду постоянно контролировать уровень антител в динамике. Что еще можно сейчас сделать? У мужа положительный резус 2 группа, у меня — отрицательный 1 группа.
Наличие в анамнезе женщины с резус-отрицательной кровью гемотрансфузии без учёта резус-принадлежности её крови, самопроизвольного прерывания беременности, антенатальной смерти плода в предыдущих беременностях или рождения ребёнка с ГБН являются прогностически неблагоприятными и указывают на повышенный риск заболевания плода при данной беременности. У пациенток с резус-отрицательной кровью необходимо с ранних сроков (6–12 недель) или при первом обращении исследовать кровь на наличие антиэритроцитарных АТ и определять их титр в динамике (1 раз в месяц на протяжении всей беременности). Титр АТ соответствует наибольшему разведению сыворотки, при котором в ней ещё возможна реакция агглютинации «Аг-АТ» (титр АТ может быть равен 1:2, 1:4, 1:8, 1:16 и т.д.). Абсолютная величина титра АТ в крови матери при определении степени тяжести заболевания плода не имеет решающего значения для прогноза развития заболевания у плода/новорождённого (возможно рождение детей с резус-отрицательной кровью у резус-сенсибилизированных женщин). Титр АТ в течение беременности может нарастать, оставаться без изменений, снижаться, а иногда наблюдается скачкообразное изменение титра (чередующиеся повышение и понижение), что имеет относительное значение.
Третья беременность, 20 недель. Обе беременности протекали без каких-либо патологий, титров не было. Первый родился естественным путем, второй — кесарево сечение. После родов вводили иммуноглобулин (во время беременности не вводили). В эту беременность риск резус-конфликта довольно высок, на данный момент антител в крови не обнаружено. Врач в ЖК предлагает сдать тест на определение резус-принадлежности плода и уже исходя из результатов, оценивать необходимость введения иммуноглобулина на 28 неделе. Насколько информативен этот тест (читала, что он не дает 100% результат)? Или мне стоит в любом случае сделать укол в 28 недель? Детей потом еще планирую, у меня резус отрицательный (2-), у мужа — положительный (3+), у первых двух детей — 4+.
Тест, к сожалению, не обладает 100% точностью. Вам необходимо в 28 недель сдать кровь на антирезусные антитела, при их отсутствии ввести дозу антирезусного иммуноглобулина.
Планируем беременность, было два аборта, первый — мини, второй — медикаментозный на ранних сроках беременности, у меня 3 отрицательная группа крови, у мужа — 3 положительная. Какие анализы сдать перед беременностью? Какова вероятность резус конфликта? Если будет резус конфликт, какова вероятность, что ребенок будет полноценный?
Перед планированием беременности необходимо пройти полный комплекс: осмотр и обследование, включая консультации смежных специалистов (терапевт, ЛОР, стоматолог). Вероятность возникновения конфликта по среднестатистическим данным составляет 10%. Если Вы будете наблюдаться и выполнять все рекомендации врача – все будет хорошо.
Мы планируем через полгода эко, 11 лет назад была беременность, которая закончилась медикаментозным абортом на сроке 5 акушерских недель, иммуноглобулин не вводили, сказали, что срок очень маленький и не нужно этого делать. Стали планировать беременность, но в течение 8 лет не получалось, прошла кучу обследований и лечений, 2 гистеросальпинографии и 1 лапароскопию, далее 1 неудачное эко и сейчас было удачное крио. Беременность 4 недели с подсадки и 6 акушерских недель, началось кровотечение, его остановили, но через 3 дня случился выкидыш и чистка. Через 12 часов ввели антирезусный иммуноглобулин, но при этом анализ на присутствие моих антител у меня не брали. Не будет ли хуже от этого укола? Если вдруг антитела были и как это может отразиться на следующих беременностях? Какими должны быть мои действия? У меня 2 отрицательная группа крови, у мужа — 1 положительная. Мне 33 года.
От введения иммуноглобулина после прерванной беременности вреда не будет. Вам необходимо сдать антирезусные антитела через 2 месяца.
13 недель беременности, в анамнезе первая беременность замершая в 7.5 недель, укол иммуноглобулина не вводили, вторая беременность через 2 года — на сроке 5 недель лежала на сохранении, врачи ввели мне укол, объяснили тем, что первая беременность была замершая, а я слышала о том, что его на более поздних сроках вводят. В ЖК врач сказала, что обнаружены антитела, собиралась выписать направление в центр планирования, но тоже была удивлена, что так рано мне ввели иммуноглобулин, сказала поэтому и антитела, направление не дала, ничего не объяснила. Что мне теперь делать и почему мне не дали направление на повторный анализ? Все ли в порядке и какие риски? У меня 2 отрицательная кровь, у мужа — 1 положительная.
На Вашем сроке необходимо сдать кровь на антирезусные антитела. При благоприятном течении беременности и при отсутствии эпизодов кровотечения одну дозу иммуноглобулина Вам необходимо ввести в 28 недель, а затем повторить введение в первые 72 часа после родов при положительном резусе у новорожденного.
Планирую беременность, первая — аборт,вторая — внематочная,третья -замершая, первые 2 раза иммуноглобулин не вводили,после замершей попросила мне ввести,антител не было, вторая и третья беременность от мужа, у него положительный резус, у меня — отрицательный. Была ли польза от введённого иммуноглобулина? Не навредит ли он следующей беременности,так как первые 2 раза не вводили препарат?
Если беременность замерла на сроке более 10 недель, введение иммуноглобулина в Вашем случае обязательно. При последующих беременностях необходимо контролировать уровень антител и вводить в регламентированные сроки антирезусный иммуноглобулин.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, и приводимая ниже информация носит исключительно справочный характер.
Резус-принадлежность: показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
Синонимы
: резус-принадлежность, резус-фактор крови, резус, Rh, Rh type, Rh typing, Rh-factor, rhesus factor.
Показания для назначения исследования
Примерно у 85% населения земного шара эритроциты (красные клетки крови) несут антиген, называемый резус-фактором (Rh); о таких людях говорят, что они резус-положительны (Rh+). Остальная часть населения лишена этого антигена, то есть они – резус-отрицательны (Rh-).
Исследование резус-принадлежности (резус-фактора) назначают перед госпитализацией (обследование потенциальных реципиентов (реципиент – человек, которому переливают донорскую кровь)).
Оценка резус-принадлежности при беременности или подготовке к беременности необходима для предотвращения резус-конфликта и развития тяжелых осложнений новорожденных.
Подготовка к процедуре
Подготовка к процедуре включает общие правила, которые необходимо выполнять перед сдачей большинства анализов крови.
- Предпочтительно выдержать 4 часа после последнего приема пищи.
- Накануне избегать пищевых перегрузок.
- Исключить прием алкоголя накануне исследования.
- Не курить минимально в течение 1 часа до исследования.
- Исключить физические и эмоциональные перегрузки накануне исследования.
Срок исполнения
1 рабочий день (указанный срок не включает день взятия биоматериала).
Что может повлиять на результаты
При соблюдении правил подготовки к исследованию результат будет корректным.
Резус-принадлежность (Rh-factor, Rh)
Для исследования берется кровь из вены.
Сдать анализ на резус-фактор можно в ближайшем медицинском офисе ИНВИТРО. Список офисов, где принимается биоматериал для лабораторного исследования, представлен в разделе «Адреса».
Референсные значения
Результат выдается в форме:
- RHD+ПОЛ;
- RHD+ПОЛ с дополнительным комментарием — «Выявлен слабый резус-антиген. При гемотрансфузии рекомендовано использовать резус-отрицательные эритроциты»;
- RHD-ОТР.
Эритроциты (красные клетки крови) несут на своей поверхности различные белки (антигены). Эти антигены наследуются от родителей.
Выявлено около 236 эритроцитарных антигенов (большинство из них встречаются редко). Они объединены в системы группы крови. Одна из таких систем, которая имеет огромное практическое значение – это система резус-фактора. Среди антигенов системы Резус наибольшее значение имеет антиген D (RhD). Именно антиген D подразумевается под термином резус-фактор. По наличию или отсутствию антигена D люди делятся на резус-положительных и резус-отрицательных.
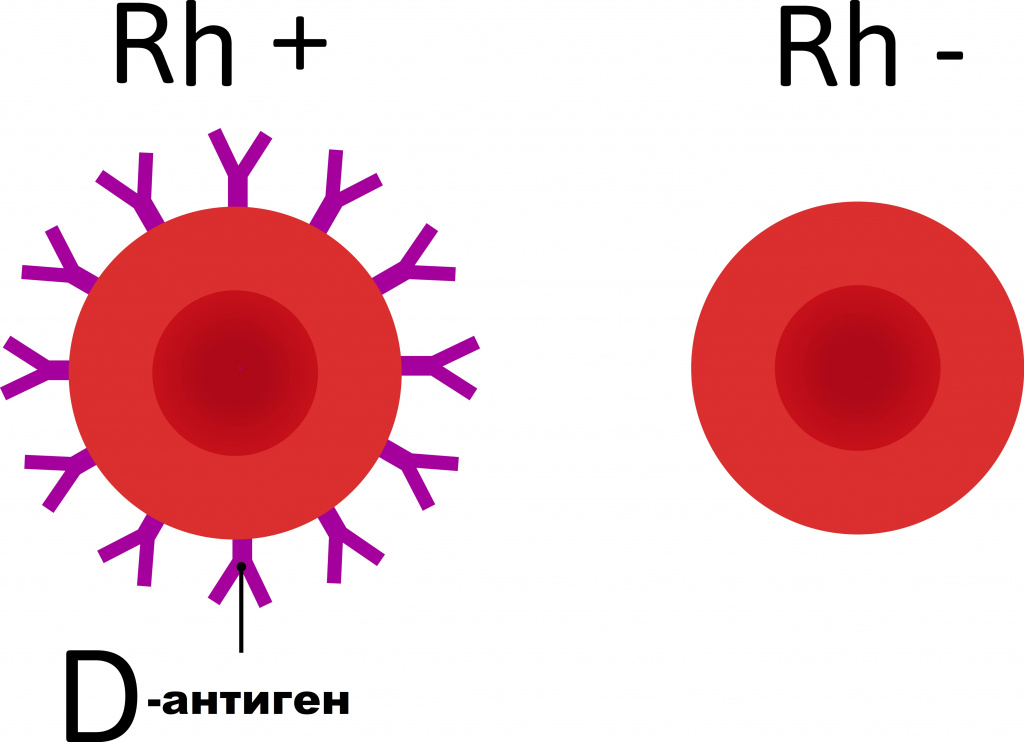
Антиген D (резус-фактор) обладает выраженными иммуногенными свойствами (способность вызывать образование антител).
Резус-конфликт (несовпадение по резус-принадлежности реципиента и донора, матери и плода) в 95% случаев является причиной гемолитической болезни новорожденных, а также частой причиной тяжелых осложнений, возникающие после переливания крови (посттрансфузионные осложнения).
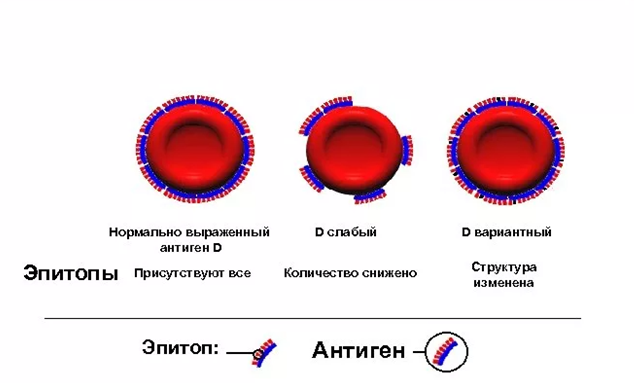
При определении резус-принадлежности различают несколько вариантов антигена D, что может приводить к затруднению его определения. Чаще всего эритроциты резус-положительного человека несут на себе все виды антигена D (нормально выраженный D антиген). У некоторых людей на эритроцитах представлены нормальные виды антигена, но снижено их количество на поверхности клетки – этот вариант называют D слабый. Если эритроциты несут не все виды антигена D (отличаются качественно), то такой вариант обозначают как D вариантный.
Исследование крови на резус-принадлежность является важным этапом предоперационной подготовки пациента, когда есть вероятность, что потребуется переливание донорской крови (гемотрансфузия). Если человеку (реципиенту) с резус-отрицательной кровью перельют резус-положительную кровь, иммунная система реципиента распознает этот антиген как чужеродный и запустит выработку антител к нему (как правило, образуется небольшое количество антител, но остаются так называемые клетки памяти (В-лимфоциты), которые помнят об антигене D). При повторном контакте с чужими эритроцитарными антигенами сразу образуется большое количество антител, и донорские эритроциты начинают массивно разрушаться. Это приводит к посттрансфузионным осложнениям — гемолитической анемии (снижению гемоглобина, способного переносить кислород к тканям и органам за счет разрушения эритроцитов), острой почечной недостаточности, желтухе, посттрансфузионному шоку.
Вторая возможная ситуация возникновения резус-конфликта – беременность, когда резус-отрицательная мать (на ее эритроцитах нет антигена D) беременна резус-положительным ребенком (на эритроцитах плода присутствует резус-фактор). На поздних сроках беременности фрагменты резус-положительных эритроцитов плода могут проникать в кровь матери, где будут восприняты как чужеродный антиген и вызовут реакцию иммунной системы – выработку антител к резус-фактору. Эти антитела в свою очередь способны проникать через плаценту в организм ребенка и разрушать его эритроциты. При первой резус-положительной беременности в организме матери обычно не успевает образовываться достаточно большого количества антител, и у плода не возникает серьезных осложнений. Однако у последующих резус-положительных плодов может наблюдаться хронический распад эритроцитов. Обычно, если не происходит выкидыша, такие дети рождаются недоношенными, страдают анемией (малокровием) и желтухой. Это состояние называют гемолитической болезнью новорожденных (гемолиз – разрушение эритроцитов). Оно может привести к гибели ребенка.
Таким образом, заблаговременное обследование матери и плода на резус-принадлежность позволяет предотвратить резус-конфликт и гибель новорожденного.
Источники:
- Минеева Н.В. Группы крови человека. Основы иммуногематологии. — СПб. 2004. 188 с.
- Дуткевич И.Г. Практическое руководство по клинической иммуногематологии (групповые антигены и антитела крови человека, группы крови и их клиническое значение, методики иммуногематологических исследований). — Санкт-Петербург : СпецЛит, 2018. 159 с.
- Connie M. Westhoff. The Structure and Function of the Rh antigen Complex. Semin Hematol. 2007 January ; 44(1): 42–50.
- Pegoraro V, Urbinati D, Visser GHA, Di Renzo GC, Zipursky A, Stotler BA, et al. (2020) Hemolytic disease of the fetus and newborn due to Rh(D) incompatibility: A preventable disease that still produces significant morbidity and mortality in children. PLoS ONE 15(7): e0235807.
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Для корректной оценки результатов ваших анализов в динамике предпочтительно делать исследования в одной и той же лаборатории, так как в разных лабораториях для выполнения одноименных анализов могут применяться разные методы исследования и единицы измерения.


