Актуальность
Часто у лечащего врача возникают претензии к лабораторным анализам, т. е. происходит не совпадение клинической картины с лабораторными показателями. Нарушение преаналитики является одной из самых частых причин этой проблемы. Данная статья поможет разобраться с этой нелепой, но весьма серьезной задачей.
Что такое преаналитика? Преаналитика – это все процедуры, выполняемые до начала проведения лабораторных исследований, которые непосредственно влияют на результат лабораторного анализа.
Оптимально проведенная преаналитическая подготовка является основным условием точной и полной лабораторной диагностики.
Зачем нужно врачам знать преаналитику? При нарушении преаналитического этапа врачи собственноручно готовят предпосылки для заведомо ложных результатов лабораторного анализа.
Статистика
Затраты времени на этапах лабораторного исследования:
Преаналитическии этап вне лаборатории – 20,20%
Преаналитическии этап в лаборатории – 37,10%
Аналитическии этап – 25,10%
Постаналитическии этап – 13,60%
Отправка результатов – 4%
Анализ ошибок показывает, что около 40% ошибок совершается на преаналитическом этапе при выполнении исследований в плановом порядке и около 60% ошибок происходит на преаналитическом этапе при неотложных анализах. (M.Plebani, P.Carraro, 1997).
Из чего состоит преналитическии этап вне лаборатории?
— Назначение анализов
— Подготовка пациента (психологическая и физическая)
— Заполнение направления.
— Взятие биоматериала.
— Хранение и доставка биоматериала.
На каждом из выше указанных составных может быть допущена ошибка.
Общие правила при подготовке к исследованию крови:
1. Кровь сдается в утренние часы натощак (или в дневные и вечерние часы, спустя 4-5 часов после последнего приема пищи). За 1-2 дня до исследования исключить из рациона продукты с высоким содержанием жиров.
2. Показатели крови могут существенно меняться в течение дня, поэтому рекомендуется все анализы сдавать в утренние часы.
3. Накануне исследования (в течение 24 часов) исключить алкоголь, интенсивные физические нагрузки, прием лекарственных препаратов (по согласованию с врачом).
4. За 1-2 часа до сдачи крови воздержаться от курения, не употреблять сок, чай, кофе, можно пить негазированную воду. Исключить физическое напряжение (бег, быстрый подъем по лестнице), эмоциональное возбуждение. За 15 минут до сдачи крови рекомендуется отдохнуть, успокоиться.
5. Не следует сдавать кровь для лабораторного исследования сразу после физиотерапевтических процедур, инструментального обследования, рентгенологического и ультразвукового исследований, массажа и других медицинских процедур.
6. При контроле лабораторных показателей в динамике рекомендуется проводить повторные исследования в одинаковых условиях – в одной лаборатории, сдавать кровь в одинаковое время суток и пр.
7. Кровь для исследований нужно сдавать до начала приема лекарственных препаратов или не ранее, чем через 10 — 14 дней после их отмены. Для оценки контроля эффективности лечения любыми препаратами нужно проводить исследование спустя 7 – 14 дней после последнего приема препарата. Если Вы принимаете лекарства, обязательно предупредите об этом лечащего врача.
Общие правила применимы ко всем анализам, но для некоторых исследований требуется специальная подготовка и дополнительные ограничения.
Влияние некоторых факторов на результат анализов.
Психический стресс
Степень влияния психического стресса (страх перед взятием крови, предоперационный стресс и т.д.) на лабораторные результаты часто недооценивается. Между тем, под его влиянием может наблюдаться увеличение секреции гормонов (альдостерона, ангиотензина, катехоламинов, кортизола, пролактина, ренина, соматотропина, ТСГ, вазопрессина) и повышение концентрации альбумина, фибриногена, глюкозы, инсулина, лактата и холестерина.
Наложение жгута
Что происходит, когда жгут накладывается на весь период времени при взятии пробы? При использовании давления ниже уровня систолического, внутри капилляров поддерживается эффективное фильтрационное давление. Как следствие, жидкость и низкомолекулярные соединения перемещаются из внутрисосудистого пространства в интерстициальное. Макромолекулы, вещества, связанные с белками и клетки крови не проникают через стенку капилляров, таким образом, их концентрация заметно возрастает, тогда как концентрации низкомолекулярных веществ не изменяются.
Длительность наложения жгута и изменения уровней исследуемых параметров
Сравнение: через 1 мин. через 3 мин.
Параметры Отклонение в %
Билирубин +8
Холестерин +5
Креатинин -9
Креатинкиназа -4
Железо +7
Глюкоза -9
γ-Глютамилтрансфераза -10
Калий +5
Положение тела
Изменение положения тела – из горизонтального в вертикальное – приводит к увеличению уровня ряда показателей.
Параметры Увеличение в %
Гематокрит 13
Эритроциты 15
Холестерин высокой плотности 10
Альдостерон 15
Ренин 60
Взятие пробы из катетера
Если пробы берут из венозных или артериальных инфузионных катетеров, канюлю следует промыть изотоническим солевым раствором в объеме, соизмеримом с объемом катетера. Прежде чем взять пробу, выбросить первые 5 мл крови, полученной из катетера. Взятиепроб для исследований свертывающей системы из катетеров, обработанных гепарином, неприемлемо. Для гепарин-зависимых методов (тромбиновое время, АЧТВ) рекомендуется
предварительно отбросить объем крови, вдвое превышающий объем катетера; первая порция взятой затем крови может быть использована для выполнения исследований, не относящихся к системе гемостаза; последующая порция цитратной крови может использоваться только для определения нечувствительных к присутствию гепарина аналитов: протромбинового времени, рептилазного времени, фибриногена по Clauss, АТ III, мономеров фибрина. Важно, чтобы перед взятием крови в пробирку с раствором цитрата натрия не было длительной паузы, в течение которой кровь в катетере может «застаиваться».
Высота над уровнем моря
Содержание некоторых компонентов крови подвержено значительным изменениям в зависимости от высоты над уровнем моря. С увеличением высоты значительное повышение наблюдается в отношении, например реактивного белка (до 65% на высоте 3600 м), гематокрита и гемоглобина (до 8% на высоте 1400 м) и мочевой кислоты. Адаптация к высоте занимает недели, а возвращение к значениям на уровне моря происходит в течение нескольких дней. Значительное снижение величин с ростом высоты над уровнем моря обнаружено в отношении мочевого креатинина, клиренса креатинина, эстриола (до 50% на высоте 4200 м), осмоляльности сыворотки, ренина плазмы и трансферрина сыворотки.
1 Мошкин А., Долгов В. Обеспечение качества в клинической лабораторной диагностике.. — М.: 2004. – С. 26-43.
2 Преаналитический этап. Пробоподготовка. West Medica
3 Преаналитика: практические советы и методы. SARSTEDT AG & Co.
Түйін: преаналитикалық кезенде көптеген факторлар зертханалық зертудің нәтижесіне әсер ететің зертхана дәрігерлері жақсы түсінеді. Ал клиникалық дәрігердің көбісі бұл жағдайдың маңызың ескермейді. Осы салалардың әсерінен зертханалық зертудің нәтижесін дәрігерлер дұрыс талдамауына және дұрыс ем шара жасамауына алып келеді.
Resume: physicians of Clinical Laboratory Diagnostics had recognized that, in the preanalytical phase, many factors can affect to the results of laboratory tests. Most of physicians don’t know of their influence. Ignorance of this factors may lead to misinterpretation of the result and take on a patient the wrong action.
Согласно данным ВОЗ, удельный вес лабораторных анализов составляет 75–80 % от общего числа диагностических исследований, выполняемых в медорганизациях.
Служба значительно эволюционировала: если раньше лаборатория была придатком в поиске факторов риска, постановке диагноза, назначении лечения, то сегодня она является объединяющим механизмом на всех этапах взаимодействия врача и пациента. Централизация лабораторных исследований — мировая тенденция реформирования клинической лабдиагностики. Особое значение имеет преаналитический этап клинических лабораторных исследований.
Лабораторная диагностика
Важная составляющая
Основной целью централизации лабораторных исследований является повышение эффективности лечебно-диагностического процесса за счет расширения объема лабораторной, диагностически значимой информации, которая поступает лечащим врачам из централизованной лаборатории.
Согласно постановлению коллегии Минздрава от 25.07.2018 № 14.4 «О совершенствовании работы службы лабораторной диагностики», централизация лабораторий, направленная на увеличение доступности лабораторных исследований, определена основным стратегическим моментом развития службы клинической лабораторной диагностики страны.
Важнейшей составляющей централизации является процесс взаимодействия с внешним заказчиком (медучреждением) на преаналитическом этапе оказания лабораторных услуг. Преаналитический этап включает прием пациента врачом, назначение лабораторных исследований, заполнение бланка направления, получение пациентом инструкций об особенностях подготовки к сдаче анализов или сбору биологического материала, взятие проб, доставку материала в лабораторию.
При централизации для лаборатории существенно увеличивается число пунктов сбора проб биологического материала, значительно расширяется спектр заказываемых тестов, изменяется структура проб биологического материала, ритм и временной период их поступления в лабораторию.
Взаимодействие централизованной лаборатории с заказчиком на преаналитическом этапе предполагает обучение врачей, медсестер, курьеров, обеспечение их инструкциями по подготовке пациентов к лабораторным исследованиям, правилам взятия, сбора и подготовки проб к транспортировке, организацию логистики доставки. Порядок организации взятия проб биологического материала и доставки его в централизованную лабораторию является одним из важнейших моментов обеспечения правильного взаимодействия лаборатории и учреждения здравоохранения.
Централизация лабораторных исследований предусматривает особые требования к организации преаналитического этапа, строгое выполнение которых позволит обеспечить получение качественных результатов. Любые неточности на этапе назначения лабораторных исследований будут существенным образом снижать эффективность лечебно-диагностического процесса.
Большинство ошибок в процессе лабораторного анализа — от назначения теста до интерпретации результатов — происходит до того, как образец попал в лабораторию, т. е. вне прямого контроля лаборатории. По данным различных исследований, на преаналитический этап приходится от 46 % до 68 % всех лабораторных ошибок.
Наиболее частые ошибки преаналитического этапа:
- отсутствие образца или перечня назначенных исследований;
- ошибки идентификации образца (этикетка,сопроводительный документ);
- гемолиз in vitro (в пробирке);
- сгустки в образце крови/плазмы;
- неправильная пробирка/контейнер;
- недостаточное количество образца (объем пробы);
- неправильное соотношение кровь/антикоагулянт;
- недостаточное перемешивание образца после взятия;
- неадекватные условия хранения и транспортировки;
- неправильный режим центрифугирования (время/скорость).
Рекомендации
При определении приемлемости выявленных ошибок рекомендуется использовать целевые уровни индикаторов качества преаналитического этапа, установленные Международной федерацией клинической химии и лабораторной медицины (IFCC). Ошибки преаналитического этапа могут существенно исказить состав или свойства биологического материала и таким образом существенно снизить диагностическую ценность результата лабораторного исследования. Частота таких ошибок зависит от уровня технологической дисциплины в направляющей организации здравоохранения, качества администрирования этого этапа.
Основные причины большого количества ошибок:
- отсутствие стандартов качества выполнения процедур преаналитического этапа;
- неиспользование для взятия и сбора биоматериала одноразовых безопасных приспособлений по причине существующего ложного представления об их высокой стоимости;
- недостаточные знания и качество обучения среднего медперсонала правилам и технике выполнения процедур преаналитического этапа.
Прогресс лабораторных технологий, оснащение медицинской лаборатории современными автоматическими анализаторами позволили получать существенно более точные результаты анализов. Новые автоматические анализаторы весьма чувствительны к качеству исследуемого биоматериала, что предъявляет более высокие требования к условиям взятия, хранения и срокам доставки проб.
Согласно приказу Минздрава от 18.04.2019 № 466 «О совершенствовании деятельности службы лабораторной диагностики Республики Беларусь», обеспечение качества преаналитического этапа лабораторных исследований является зоной ответственности клинических специалистов. В стандарте СТБ ISO 15189-2015 «Медицинские лаборатории. Требования к качеству и компетенции» требуется установление индикаторов качества с целью мониторинга и оценки работы по всем критическим аспектам преаналитического этапа. Их внедрение в лабораторную практику и систематический сбор данных позволят обеспечить надежность результатов лабораторного тестирования.
Внутренний стандарт
Клинико-диагностическая лаборатория (КДЛ) РНПЦ РМиЭЧ является многопрофильной, с 2016 года выполняет централизованные исследования для взрослых и детей Новобелицкого и Советского районов Гомеля. Заказчиками являются 10 поликлиник. Исследования включают широкий спектр биохимических (специфических белков и метаболитов), иммунохимических (гормоны, онкомаркеры, витамины и др.), коагулологических (коагулограмма, агрегатограмма, факторы свертывания и антикоагулянты, D-димеры и др.) лабораторных тестов.
Разработан внутренний стандарт, который был включен в текст совместного приказа РНПЦ РМиЭЧ и ГУЗО Гомельского облисполкома (№ 117 и № 167 от 05.02.2019) «О централизации лабораторных исследований». Определена схема проведения централизованных лабораторных исследований.
Для обеспечения доступности для врачей-клиницистов информации о полном спектре выполняемых тестов сотрудниками лаборатории разработаны бланки направлений.
Для обеспечения контроля качества выполнения централизованных исследований лаборатория постоянно анализирует результаты применения основных индикаторов качества преаналитического этапа:
- ошибки идентификации и транскрипции тестов;
- несоответствие направления установленной форме;
- неверный тип, недостаточный объем образца;
- повреждение образца/направления в ходе транспортировки;
- образец, направление для образца не получены;
- сгусток в образце.
По результатам анализа, проведенного КДЛ РНПЦ РМиЭЧ, несоответствия в целом выявляются для 1,3 % доставленных образцов сыворотки/плазмы. Среди индикаторов с наибольшей частотой встречаются ошибки транскрипции тестов, составляющие 1 %:
- отсутствие отметок о необходимых тестах;
- нечеткий запрос на исследование;
- незаполненные/не полностью заполненные паспортные данные пациента (не обозначен пол, возраст, не указан диагноз, отсутствует печать врача).
Реже определяются ошибки идентификации пробы — нарушение маркировки, в т. ч. расхождения между нумерацией направления и пробы. В 0,34 % случаев пробы не доставлялись в лабораторию, в 0,3 % — для проб отсутствовали направления на исследования. Несмотря на то что выбраковка по причине гемолиза определена на этапе взятия крови и первичной пробоподготовки, в лабораторию в 0,31 % случаев доставляются гемолизированные образцы. В 0,5–1 % случаев в пробах сыворотки встречаются нити фибрина, сгустки, осадок эритроцитов. Регистрируются случаи доставки количества сыворотки, недостаточного для выполнения назначенных тестов. Такие несоответствия являлись результатом неполного соблюдения поликлиниками правил пробоподготовки: выдержки необходимого времени сворачивания крови, соблюдения режима центрифугирования крови и пипетирования сыворотки.
Для образцов сыворотки с выявленными ошибками транскрипции тестов лаборатория выясняет необходимую информацию по телефону, после чего образцы, как правило, принимаются в работу. Указанные действия позволили минимизировать потери образцов по причине нарушений правил преаналитики. Выбраковка с оформлением акта отказа в приеме биологического материала с объяснением причин проводится для гемолизированных образцов либо для случаев, когда доставляется только проба сыворотки без направления и наоборот. Пробы сыворотки со сгустками, эритроцитами подвергаются повторному центрифугированию, после чего выполняются исследования.
Лабораторная практика традиционно делится на три этапа: преаналитический, аналитический и постаналитический.
Преаналитическая фаза включает в себя правильный отбор образцов, предоставление информации о пациенте, сбор и маркировку образцов, обработку образцов, сортировку, титрование и центрифугирование. Любой из этих шагов может быть пропущен, что приведет к неточным результатам, которые приписываются преаналитической фазе.
Преаналитические ошибки при исследовани общего анализа крови чаще всего вызваны неверным пониманием запроса на анализ, неправильной маркировкой, контаминацией места отбора, гемолизом, сгустками, недостаточным количеством образцов, проблемами хранения и несоответствующей пропорцией крови к антикоагулянту или неправильным выбором антикоагулянта.
Общая частота неточностей в лабораторных работах, согласно G. Lippi et.al. (2010), варьируется от 0,1% до 3,0%. Считается, что преаналитические ошибки составляют от 46% до 68,2% ошибочных диагнозов, в то время как аналитические ошибки, которые были в центре внимания более ранних исследований, составляют лишь около 10% всех ошибочных диагнозов (Hammerling J., 2013). Кроме того, преаналитические ошибки составляют от 18,5% до 47% всех лабораторных ошибок.
Наиболее распространенными преаналитическими ошибками являются отсутствие медицинской информации, неподходящие контейнеры и потерянные образцы.
Несмотря на то, что существуют международные стандарты отбора проб крови и стандартизации процесса тестирования, соблюдение руководящих принципов здесь крайне низкое, особенно тогда, когда лабораторный персонал не привлекается, а медсестры или врачи выполняют забор крови, частота преаналитических ошибок становится очень высокой.
Кроме того, критерии отбраковки образцов различаются в разных лабораториях. Не хватает профессиональных данных по отчетности, анализу первопричин и стратегиям предотвращения лабораторных ошибок (Lima-Oliveira G, et.al., 2012).
Наиболее распространенной преаналитической ошибкой являются изменения условий хранения из-за задержки при транспортировке, на которые приходится 19,45%, за которыми следуют пробы, забракованные из-за неверных медицинских записей- 19,16%. Общее количество забракованных разбавленных проб составляет 16,35%, а количество забракованных проб из-за неправильных пробирок составляет 16,01%). Отклоняется гемолизированных образцов — 15,13%. Немеченые образцы отклоняются в количестве 10,01%, а образцы со сгустками составляют 3,88% от общего числа забракованных образцов (Toor N., et. al., 2023)
Низкая удовлетворенность пациентов напрямую связана с лабораторными ошибками и высокими затратами как для пациентов, так и для системы лабораторных услуг.
Негативное влияние лабораторных ошибок на лечение пациентов не ограничивается тем фактом, что они увеличивают время обработки, требуют дополнительных заборов крови и приводят к неточным диагнозам и неподходящим лекарствам; они также наносят ущерб репутации лаборатории и подрывают доверие пациентов к диагностическим услугам. Было подсчитано, что лабораторная ошибка оказывает негативное влияние на результаты лечения пациентов до 24,4% (Lippi G., et.al., 2006).
Этот процесс приводит к увеличению финансовой нагрузки на систему здравоохранения. Согласно исследованию S. Green (2013), расходы на преаналитические ошибки составляют от 0,23% до 1,2% всего операционного бюджета больниц.
Сбор крови
Количество и концентрация дикалийэтилендиаминтетрауксусной кислоты (EDTA) в пробирке для сбора крови требуют, чтобы кровь собиралась до определенной отметки на пробирке. Если собрано слишком мало крови, разбавление образца может привести и к изменению параметров. Относительный избыток EDTA в таких случаях также влияет на морфологию клеток крови.
Транспортировка крови
Транспортировка образца должна исключать высокую температуру. Фрагментация эритроцитов при этом является признаком избыточного тепла. Ложно высокое количество лейкоцитов (WBC) при высокой температуре встречается чаще, чем ложно низкое. Известно, что в определенных ситуациях гематологические анализаторы обеспечивают ложное PLT, когда истинное количество тромбоцитов является адекватным.
Физиологические и физические факторы, влияющие на показатели общего анализа крови
Несколько физиологических и физических факторов могут повлиять на результаты CBC и затруднить установление референтных значений. Физиологические факторы включают возраст, этническую принадлежность, пол, сезон, время суток, питание, болезни, стресс, травмы др.
К важным физическим факторам относятся место забора крови, наличие и тип антикоагулянта, а также обработка и подготовка образцов (Dyer D.Cervasio S.,2008). Любая интерпретация результатов должна учитывать эти факторы.
Преаналитические ошибки результатов общего анализа крови
Потеря образца
Отсутствие полноценного запроса на анализ
Неправильная маркировка (19,16% преаналитических ошибок)
Сбор крови
Контаминация места, в котором производится забор крови
Недостаточное количество образца крови
Неправильный выбор антикоагулянта, относительный избыток или дефицит EDTA (16,45% преаналитических ошибок)
Неправильные пробирки (16,01%)
Гемолиз in vitro (15,13% преаналитических ошибок)
Наличие сгустков крови (3,88% преаналитических ошибок)
Транспортировка
Задержка транспортировки (19, 45% преаналитических ошибок)
Неподходящие контейнеры
Высокая температура окружающей среды при транспортировке
<RBC (фрагментация эритроцитов)
WBC >
Неправильное хранение
Высокая температура окружающей среды при хранении
<RBC (фрагментация эритроцитов)
WBC >
Первоначальное замораживание с последующим охлаждением
Нарушение срока хранения образца крови при определенной температуре
Хранение крови
Отложенный анализ проб по организационным, техническим причинам или проверке сомнительных результатов, которые необходимо уточнить — не редкость в клинической практике. Кроме того, реорганизация лабораторных служб по всему миру влечет за собой объединение небольших лабораторий в более крупные, что особенно важно в эпоху новых инициатив в области общественного здравоохранения. Большое количество образцов отправляется из периферийных центров в централизованную лабораторию на большие расстояния, тем самым происходит задержка на 12-24 часа или даже более. Более того, в выходные дни этот интервал может превышать 36 часов. Это важно уситывать в связи с тем, что CBC является наиболее часто проводимым лабораторным тестом, дающим основную и ценную информацию не только для облегчения диагностики и направления дальнейшего тестирования, но и для мониторинга состояния пациента, включая оценку эффективности терапии.
В большинстве случаев мы не можем сразу провести анализ, поэтому информацией о том, как долго мы можем хранить образцы для получения надежных результатов, должны владеть как сотрудники лаборатории, так и врачи.
В литературе большинства производителей автоматических анализаторов часто упоминается, что образцы крови, хранящиеся либо при комнатной температуре, либо при 4 ± 2°C (в холодильнике) до 24 часов, как правило, дают надежные результаты для общего анализа крови и автоматизированного дифференциального подсчета лейкоцитов. Однако, хранение при комнатной температуре может вызвать изменения этилендиаминтетраацетата (EDTA) и количественное влияние хранения на кровь, поскольку известно, что клеточные элементы обладают ограниченной стабильностью в EDTA. В то же время, было отмечено, что хранение в холодильнике крови с антикоагулянтом EDTA улучшает стабильность общего анализа крови (Gulati G., et.al., 2002).
В соответствии с рекомендациями Международного комитета по гематологической стандартизации, максимальные интервалы хранения для общего и лейкоцитарного подсчета с автоматическим дифференциальным подсчетом стабильны при 4°C в течение как минимум 24 ч или даже до 72 ч, при этом существенные различия зависят от типа автоматизированного анализатора клеток крови.
Для CBC образцы можно надежно хранить в течение 24 часов. Для более длительного хранения лучшим выбором будет охлаждение (при 4 °C). Интересно, что в некоторые моменты времени (1, 2 и 4 часа) PLT немного ниже. Хранение при 4 °C показало гораздо большую стабильность. За исключением 8 часов, до 3 дней статистических изменений не было. Преимущества холодильной камеры (4 ° C) очевидны для длительного хранения. Стоит отметить, что хранение образцов более 12 часов для метаболической панели может привести к ненадежным результатам. Разные авторы сообщают, что некоторые анализы крови стабильны до 72 часов после сбора, если хранить их при 4 ° C в холодильнике.
Повреждение эритроцитов при хранении тесно связано с их внутренним энергетическим метаболизмом. Поскольку в эритроцитах нет митохондрий, полностью зависящих от гликолиза для получения энергии, молочная кислота, образующаяся в процессе гликолиза, будет снижать внутреннее значение рН клеток, тем самым снижая уровень метаболизма клеток и уменьшая производство АТP, что приводит к снижению уровня фосфорилирования фосфопротеинов и утрате деформируемости клеточной мембраны. Снижение уровня АТP в свою очередь уменьшает синтез 2,3-дифосфоглицериновой кислоты, а уменьшение значения рН и концентрации 2-магне3-дифосфоглицериновой кислоты сдвигает кривую кислородной диссоциации гемоглобина влево. АТP также является агонистом NO-синтазы. NO и гемоглобин в эритроцитах объединяются с образованием SNOHb и Hb(Fe~II) NO, которые участвуют в транспорте и метаболизме NO. Уменьшение АТP также влияет на ионный насос на клеточной мембране, что приводит к увеличению уровня К + в депонированной крови (Li L., et.al., 2022).
Некоторые параметры, связанные с эритроцитами, такие как RBC, HB и MCHC менее стабильны при хранении при 4 °C, на что может повлиять первоначальное замораживание с последующим охлаждением (Lombardi G., et al., 2011). RDW значительно увеличивается после 24-часового хранения при комнатной температуре. Возможной причиной этого изменения может быть повышенный MCV (de Baca M., et.al., 2006).
По данным D. Gunawardena et.al. (2017) среди параметров CBC лейкоциты (WBC), эритроциты (RBC), HB, MCH, нейтрофилы и лимфоциты стабильны при всех температурах (4 ± 2°С, 23 ± 2°С и 31 ± 2°С.) до 48 часов. Моноциты, эозинофилы, MCH, HCT и SV-RDW показали статистически значимые изменения при 23 ± 2°C и 31 ± 2°C. Значительное снижение количества тромбоцитов (PLT) и увеличение MPV и количества базофилов наблюдались при всех исследуемых температурах вплоть до 48 часов.
Увеличение MPV наблюдается при всех температурах, причем этот показатель не считается очень стабильным для образцов крови, хранящихся в течение длительного времени. Его значения изменяются в первый период времени (1 час) и не имеют различий для температуры хранения (Wu D-W., et.al., 2017). Четыре дня при 4 °C изменяют морфологию, движение и агрегацию тромбоцитов (Mahmoodi M., et al., 2006). MPV может иметь отношение к изменениям формы тромбоцитов, связанным со временем и формой, от дисковидной до сферической и набухания. Возможно, что тробмоциты, которые показывают повышение MPV, не будут подсчитаны машиной как тромбоциты, а будут помечены отдельно, что приведет к снижению PLT. Это говорит о том, что лучше всего оценивать PLT в течение 6 часов после забора крови.
Во всех случаях результаты CBC обычно более стабильны, чем различные биохимические, например, метаболические панели и предоставляют надежные результаты даже через 24 часов хранения.
Эритроциты, хранящиеся с добавлением прогестерона, имеют более высокие уровни АТP, меньший спонтанный лизис, более высокую осмотическую резистентность и более высокое поглощение метиленового синего в течение времени хранения, чем клетки, хранение которых происходит без добавления прогестерона. Этот гормон, по-видимому, находится в устойчивом равновесии между плазмой и эритроцитами в течении 42 дней хранения, и его количество в плазме почти вдвое больше, чем в клетках. После повторных промываний солевым раствором около 10% прогестерона остается прикрепленным к эритроцитам. Специфическая связь прогестерона с популяциями эритроцитов различной плотности показывает, что высокая удельная активность достигается в популяциях клеток низкой плотности (молодые клетки) в течение всего времени хранения (DeVenuto F., S M Wilson S.,1976).
.
Трансфузиология
Во время хранения компонентов крови ex vivo биореактивные вещества, накопленные в среде хранения и вызвавшие изменения в эритроцитах, предоставили постоянные доказательства непрерывных изменений, приводящих к дисфункции эритроцитов и способны оказывать неблагоприятное воздействие на переливаемого хозяина (Gacko M., et.al., 2004). Удаление лейкоцитов и тромбоцитов как источника свободных радикалов в компонентах эритроцитов влияет на защиту оксидоредуктивного баланса в компонентах эритроцитов во время хранения.
Лейкоредуцирование или лейко-истощение относится к снижению количества лейкоцитов менее чем 5 × 10 6 остаточных донорских лейкоцитов в конечном продукте крови при сохранении 85% жизнеспособного исходного RBC. Наличие лейкоцитов в компонентах крови является причиной нескольких осложнений.
Лейкоредуцирование предотвращает фебрильные реакции, накопление цитокинов / хемокинов, избегая фебрильной негемолитической реакции трансфузии (FNHTR), уменьшая передачу цитомегаловируса и невосприимчивость к переливанию тромбоцитов (в концентратах тромбоцитов).
Несмотря на использование аддитивных растворов, изменения морфологии и метаболизма эритроцитов ожидаются при хранении пакетов с кровью с лейко-редукцией и без нее. Хранение эритроцитов вызывает некоторые сложные структурные и биохимические изменения, которые называются поражением хранения эритроцитов (RCSL)
Биохимические изменения включают снижение активности фермента глюкозо-6-фосфатдегидрогеназы (G6PD) в качестве антиоксидантного фермента, увеличение везикуляции эритроцитов, потеря мембран эритроцитов, лизис мембран эритроцитов, снижение уровня 2,3-дифосфоглицерата (2,3- DPG), аденозинтрифосфат (АТФ) и снижение уровня глутатионредуктазы (GSH). Эти процессы сопровождаются снижением рН, увеличением активности фермента ЛДГ и концентрацией лактата.
Эти изменения приводят к снижению функции и выживаемости эритроцитов после переливания. G6PD является важным ферментом в метаболизме эритроцитов и ключевым ферментом окислительного пентозофосфатного пути (PPP). В PPP никотинамид-аденин-динуклеотид-фосфат (NADP) превращается в его восстановленную форму, NADPH, которая необходима для GSH-опосредованной защиты от окислительного стресса поддерживая целостность эритроцитов.
Также наблюдаются некоторые биохимические изменения концентратов эритроцитов при анаэробном гликолизе. В частности, наблюдается увеличение уровней калия (K +) и лактата и одновременное снижение уровней pH, глюкозы и натрия (Na +). Время хранения не влияет на уровни кальция (Ca ++) в концентратах RBC.
Активность ферментов лактатдегидрогеназы и К + в эритроцитах значительно выше (в 20-160 раз), чем в плазме, и можно ожидать, что гемолиз приведет к увеличению этих аналитов.
Cтатистически значимое увеличение активности лактат дегидрогеназы было показано в течение периода хранения в нефильтрованных эритроцитах. Активность фермента LDH в нефильтрованном эритроците по сравнению с LR-RBC увеличилась с 14-го дня хранения и была статистически признана значимой. Такие показатели, как MCV, MCH и MCHC, меньше всего влияли на хранение. Другие авторы обнаружили, что MCV увеличился, а MCHC значительно снизился в течение периода хранения, которые оценивались каждую неделю. (Grezelbash B., et.al., 2018).
J. Latham et al. (1982) наблюдали увеличение концентрации не только лактата, лактатдегидрогеназы, но и гемоглобина во время хранения. Консистенция свободного Hb и скорость гемолиза также были выше в нефильтрованном RBC по сравнению с LR-RBC во время хранения. Эти наблюдения указывают на возможное вовлечение лейкоцитов в большее повреждение эритроцитарной мембраны и благоприятное влияние лейкоредуцирования на качество сохраняемых единиц эритроцитов. Эти различия могут быть связаны с биологически активными веществами, такими как цитокины и гистамин, которые высвобождаются из лейкоцитов во время хранения, что оказывает непосредственное воздействие на мембрану эритроцитов и приводит к некоторым структурным и биохимическим изменениям.
Согласно предложению Castro O., et.al. (2003), общая концентрация гемоглобина, лактатдегидрогеназа и концентрация лактата являются маркерами гемолиза.
Sonker А. et.al. (2014) также сообщили, что лейко-фильтрованный RBC показывает меньшее повышение K +, LDH и гемолиза к концу периода хранения по сравнению с их нефильтрованными единицами. Присутствие лейкоцитов может быть причиной усиленного окислительного стресса. Эти авторы отметили, что активность ферментов LDH, гемолиз и повреждение клеточных мембран (калий, LDH, свободный гемоглобин) усиливаются в компонентах крови с высоким содержанием лимфоцитов.
Дельта – проверки
Преаналитические ошибки, которые могут повлиять на результаты CBC, включают смешивание образцов, неправильное получение образца и нарушение целостности образца между моментом, когда образец был получен и когда он был доставлен в лаборатории.
Дельта-проверки — процесс маркировки различий в конкретных аналитах между последовательными анализами, являются одним из способов выявления таких проблем. Такие проверки эффективны при обнаружении некоторых вариантов преаналитических ошибок.
Среди обычно оцениваемых показателей CBC средний объем клеток, или MCV, и средняя концентрация клеточного гемоглобина, или MCHC, пригодны для дельта -проверок лучше всего. И тот, и другой показатель чрезвычайно стабильны в течении короткого срока — 24 часа. Например, суточный биологический коэффициент вариации MCV у здоровых людей составляет всего 0,5%. Даже в ситуациях быстрого изменения других параметров эритроцитов, таких как острое кровоизлияние, MCV и MCHC не будут значительно изменяться в течение суток, поскольку ответ ретикулоцитов на острую кровопотерю не начинается в течение первых двух-трех дней. За исключением переливания эритроцитов и редко острого внутрисосудистого гемолиза, нет неотложных ситуаций в состоянии пациента, которые бы значительно изменили эти показатели в краткосрочной перспективе. В случае острого гемолиза с гемоглобинемией, MCHC может быть изменен, в отличие от MCV, который будет оставаться стабильным.
Из других проблем, связанных с анализом образца, гемолиз образца также поддается обнаружению с помощью дельта-проверок на основе MCHC. В этом сценарии RBC уменьшается, без изменений в HB и MCV, что приводит к увеличению MCHC.
Загрязнение образцов внутривенной жидкостью и изменения количества клеток из-за свертывания образцов теоретически могут быть обнаружены дельта-проверками HB и HCT, а также изменениями значений RBC, WBC и PLT. Однако нецелесообразно использовать дельта-проверки любого из этих показателей для обнаружения такого образца, поскольку быстрые изменения любого из них являются обычными у госпитализированных пациентов, причем, частота ложноположительных результатов будет здесь неприемлемо высокой. Тем не менее, внутривенное загрязнение приводит к пропорциональному снижению всех этих показателей.
Следует также отметить, что выполнение дельта-проверок на MCHC имеет дополнительное преимущество для обнаружения неисправности анализатора, поскольку MCHC рассчитывается на основе трех параметров эритроцитов RBC, HB и MCV, которые измеряются непосредственно на большинстве гематологических анализаторов. Следовательно, проблемы в любом из этих измерений будут влиять на MCHC. Выбор пределов достоверности для дельта-проверок зависит от ряда факторов, в том числе от желаемого баланса чувствительности и специфичности и оцениваемой популяции пациентов. Статистический подход к дельта-проверкам может быть достигнут путем получения пар точек данных пациентов из репрезентативной популяции. Пределы, охватывающие желаемую долю населения (например, 95% или 99%), могут быть легко выбраны (Savage R., 2006).
Температура хранения
Гемоглобин, количество эритроцитов, количество лейкоцитов, средний корпускулярный гемоглобин остаются стабильными в течение по меньшей мере 24 часов при температуре 33 ° C. Гематокрит, средний корпускулярный объем и количество тромбоцитов стабильны в течение менее четырех часов при 33 ° C. Все вышеперечисленные параметры стабильны при 22 ° С и 4 ° С. Дифференциальная оценка HCT, MCV, PLT показала нестабильность в течение четырех часов при температуре 33 ° C.
Некоторые параметры, связанные с эритроцитами, такие как RBC, HB и MCHC, менее стабильны при хранении при 4 ° C, поскольку на них может повлиять первоначальное замораживание с последующим охлаждением Изменение HCT и MCHC, несомненно, является следствием изменения MCV, поскольку эти параметры частично получены из последнего показателя.
Гемолиз in vitro
Термин «гемолиз» происходит от латинского слова hemo (кровь) и лизиса (взломать) и означает разрушение клеток крови. Лаборанты обычно ограничивают значение понятия «гемолиз» эритроцитами (процесс, называемый эритролизом), которые составляют наибольший процент эритроцитов крови и игнорируют состояние других клеток крови. В связи с этим подходом методы оценки гемолиза зависят «исключительно» от измеренного количества свободного гемоглобина (fHB), выделившегося из разрушенных эритроцитов. Напротив, небольшое количество авторов описывают «гемолиз» как разрушение всех типов клеток крови, а именно панцитолиз и заявляют, что лейкоциты и тромбоциты также могут поддвергаться гемолизу. Стоит отметить, что лейкоциты могут способствовать повышению уровня калия в состоянии лизиса.
Гемолиз может происходить in vivo, при патологических состояниях или in vitro в связи с преаналитическими ошибками.
Гемолиз in vitro в преаналитической фазе является основной проблемой, с которой сталкиваются клинические лаборатории. Определяемый как разрыв мембраны эритроцита с экстравазацией гемоглобина и других внутриклеточных компонентов в окружающую плазму, гемолиз можно обнаружить визуально во время лабораторной оценки из-за изменения окраски плазмы от розового до красного после центрифугирования образца.
Гемолиз in vitro обычно возникает в результате неадекватного забора крови, включая такие факторы, как использование игл малого диаметра, попадание остатков спирта с кожи в образец, трудности с поиском венозного доступа, маленькие и хрупкие вены, которые легко травмируются, и попытки неудовлетворительной пункции. Кроме того, неправильное обращение с образцами, такое как недостаточное заполнение пробирки для сбора, приводящее к избытку антикоагулянта, сильное встряхивание образца, воздействие чрезмерно высоких или низких температур и центрифугирование на очень высокой скорости в течение длительного периода времени, также являются факторами, которые могут нарушить структурная целостность клеток крови (Lippi G., et.al., 2008).
Факторы, способствующие гемолизу in vitro вследствие неадекватного забора крови
Использование игл малого размера
Попадание остатков спирта с кожи в образец
Трудности с поиском венозного доступа
Маленькие и хрупкие вены, которые легко травмируются
Неоднократные попытки плохой пункции
Было показано, что с течением времени количество эритроцитов значительно снижается из-за гемолиза. Повышенная проницаемость клеток будет определяться увеличением MCV — индекса, отражающего набухание эритроцитов. Изменение HCT и MCHC явно является следствием изменения MCV, поскольку эти параметры частично получены из MCV (Buoro S., et al., 2016).
В работе G. de Longe et.al. (2018) образцы с высокой степенью гемолиза превышали спецификации качества для желаемой систематической ошибки, демонстрируя снижение эритроцитов (4,7%), гематокрита (6,6%), MCV (0,6%) и увеличение параметров: RDW (1,3%), MCH (1,5%), MCHC (2,5%) и количество тромбоцитов (36,7%). В то время как образцы с легкой степенью гемолиза имели умеренное увеличение MCH (0,6%), MCHC (0,7%) и количества тромбоцитов (1,4%). Авторами было замечено, что RCB имел погрешность -6,4% (от -22,8% до 10,0%), а HCT — погрешность -8,3% (от -25,7% до 9,2%), превышающую допустимые нормы ±1,7% для проб с высокой степенью гемолиза. Так, эти показатели могут быть занижены до 22,8% для эритроцитов и до 25,7% для HCT или завышены до 10,0% и 9,2% соответственно.
Стоит отметить, что принцип измерения MCV сильно различается в зависимости от используемого гематологического анализатора. с помощью метода импеданса образцы с высокой степенью гемолиза могут демонстрировать умеренное изменение MCV (увеличение на 0,6%) с последующим увеличением RDW на 1,3%, что представляет собой широкий разброс примерно в 12%, оценивая пределы согласия и их доверительные интервалы.
Гемолиз образца крови, взятого для CBC
Высокая степень гемолиза
Снижение RBC (4,7%), HCT (6,6%), MCV (0,6%)
Увеличение RDW (1,3%), MCH (1,5%), MCHC (2,5%)
Отсутствии изменений HB
Увеличение PLT (36,7%)
Низкая степень гемолиза
Увеличение MCH (0,6%), MCHC (0,7%), PLT (1,4%)
Сравнение образцов с разной степенью гемолиза показало снижение количества эритроцитов и гематокрита и увеличение средней концентрации корпускулярного гемоглобина и количества тромбоцитов в образцах с высокой степенью гемолиза. Согласно принятой клинической точке зрения, образцы с высокой степенью гемолиза превышают желаемую погрешность, демонстрируя снижение RBC, HCT и MCV, а также увеличение RDW, MCH, MCHC, PLT. Однако образцы с легкой степенью гемолиза показали лишь незначительное увеличение среднего корпускулярного гемоглобина, средней концентрации корпускулярного гемоглобина и количества тромбоцитов. (de Jonge G., et.al.,2018).
Выяснение интерференционных механизмов гемолиза необходимо для более точного решения проблемы гемолиза in vitro. Гемолизированные образцы влияют на результаты испытаний по нескольким механизмам, таким как: композиционные помехи (из-за разницы между внутриклеточной и внеклеточной концентрацией аналитов), помехи сигнала в инструментальных измерениях и химической помехи в аналитических реакциях. Эти интерференционные механизмы могут сосуществовать в различных сочетаниях. Отказ от результатов анализа гемолизированных образцов может привести к задержке в диагностике, что угрожает безопасности пациента, а запрос дополнительного образца увеличивает рабочую нагрузку лаборанта и стоимость исследования.
Вполне возможно, что клеточный дебрис и строма, образующиеся в результате распада эритроцитов, могут вызывать существенные аналитические помехи в подсчете тромбоцитов
Согласно данным ВОЗ, удельный вес лабораторных анализов составляет 75–80 % от общего числа диагностических исследований, выполняемых в медорганизациях.
Служба значительно эволюционировала: если раньше лаборатория была придатком в поиске факторов риска, постановке диагноза, назначении лечения, то сегодня она является объединяющим механизмом на всех этапах взаимодействия врача и пациента. Централизация лабораторных исследований — мировая тенденция реформирования клинической лабдиагностики. Особое значение имеет преаналитический этап клинических лабораторных исследований.
Лабораторная диагностика
Важная составляющая
Основной целью централизации лабораторных исследований является повышение эффективности лечебно-диагностического процесса за счет расширения объема лабораторной, диагностически значимой информации, которая поступает лечащим врачам из централизованной лаборатории.
Согласно постановлению коллегии Минздрава от 25.07.2018 № 14.4 «О совершенствовании работы службы лабораторной диагностики», централизация лабораторий, направленная на увеличение доступности лабораторных исследований, определена основным стратегическим моментом развития службы клинической лабораторной диагностики страны.
Важнейшей составляющей централизации является процесс взаимодействия с внешним заказчиком (медучреждением) на преаналитическом этапе оказания лабораторных услуг. Преаналитический этап включает прием пациента врачом, назначение лабораторных исследований, заполнение бланка направления, получение пациентом инструкций об особенностях подготовки к сдаче анализов или сбору биологического материала, взятие проб, доставку материала в лабораторию.
При централизации для лаборатории существенно увеличивается число пунктов сбора проб биологического материала, значительно расширяется спектр заказываемых тестов, изменяется структура проб биологического материала, ритм и временной период их поступления в лабораторию.
Взаимодействие централизованной лаборатории с заказчиком на преаналитическом этапе предполагает обучение врачей, медсестер, курьеров, обеспечение их инструкциями по подготовке пациентов к лабораторным исследованиям, правилам взятия, сбора и подготовки проб к транспортировке, организацию логистики доставки. Порядок организации взятия проб биологического материала и доставки его в централизованную лабораторию является одним из важнейших моментов обеспечения правильного взаимодействия лаборатории и учреждения здравоохранения.
Централизация лабораторных исследований предусматривает особые требования к организации преаналитического этапа, строгое выполнение которых позволит обеспечить получение качественных результатов. Любые неточности на этапе назначения лабораторных исследований будут существенным образом снижать эффективность лечебно-диагностического процесса.
Большинство ошибок в процессе лабораторного анализа — от назначения теста до интерпретации результатов — происходит до того, как образец попал в лабораторию, т. е. вне прямого контроля лаборатории. По данным различных исследований, на преаналитический этап приходится от 46 % до 68 % всех лабораторных ошибок.
Наиболее частые ошибки преаналитического этапа:
- отсутствие образца или перечня назначенных исследований;
- ошибки идентификации образца (этикетка,сопроводительный документ);
- гемолиз in vitro (в пробирке);
- сгустки в образце крови/плазмы;
- неправильная пробирка/контейнер;
- недостаточное количество образца (объем пробы);
- неправильное соотношение кровь/антикоагулянт;
- недостаточное перемешивание образца после взятия;
- неадекватные условия хранения и транспортировки;
- неправильный режим центрифугирования (время/скорость).
Рекомендации
При определении приемлемости выявленных ошибок рекомендуется использовать целевые уровни индикаторов качества преаналитического этапа, установленные Международной федерацией клинической химии и лабораторной медицины (IFCC). Ошибки преаналитического этапа могут существенно исказить состав или свойства биологического материала и таким образом существенно снизить диагностическую ценность результата лабораторного исследования. Частота таких ошибок зависит от уровня технологической дисциплины в направляющей организации здравоохранения, качества администрирования этого этапа.
Основные причины большого количества ошибок:
- отсутствие стандартов качества выполнения процедур преаналитического этапа;
- неиспользование для взятия и сбора биоматериала одноразовых безопасных приспособлений по причине существующего ложного представления об их высокой стоимости;
- недостаточные знания и качество обучения среднего медперсонала правилам и технике выполнения процедур преаналитического этапа.
Прогресс лабораторных технологий, оснащение медицинской лаборатории современными автоматическими анализаторами позволили получать существенно более точные результаты анализов. Новые автоматические анализаторы весьма чувствительны к качеству исследуемого биоматериала, что предъявляет более высокие требования к условиям взятия, хранения и срокам доставки проб.
Согласно приказу Минздрава от 18.04.2019 № 466 «О совершенствовании деятельности службы лабораторной диагностики Республики Беларусь», обеспечение качества преаналитического этапа лабораторных исследований является зоной ответственности клинических специалистов. В стандарте СТБ ISO 15189-2015 «Медицинские лаборатории. Требования к качеству и компетенции» требуется установление индикаторов качества с целью мониторинга и оценки работы по всем критическим аспектам преаналитического этапа. Их внедрение в лабораторную практику и систематический сбор данных позволят обеспечить надежность результатов лабораторного тестирования.
Внутренний стандарт
Клинико-диагностическая лаборатория (КДЛ) РНПЦ РМиЭЧ является многопрофильной, с 2016 года выполняет централизованные исследования для взрослых и детей Новобелицкого и Советского районов Гомеля. Заказчиками являются 10 поликлиник. Исследования включают широкий спектр биохимических (специфических белков и метаболитов), иммунохимических (гормоны, онкомаркеры, витамины и др.), коагулологических (коагулограмма, агрегатограмма, факторы свертывания и антикоагулянты, D-димеры и др.) лабораторных тестов.
Разработан внутренний стандарт, который был включен в текст совместного приказа РНПЦ РМиЭЧ и ГУЗО Гомельского облисполкома (№ 117 и № 167 от 05.02.2019) «О централизации лабораторных исследований». Определена схема проведения централизованных лабораторных исследований.
Для обеспечения доступности для врачей-клиницистов информации о полном спектре выполняемых тестов сотрудниками лаборатории разработаны бланки направлений.
Для обеспечения контроля качества выполнения централизованных исследований лаборатория постоянно анализирует результаты применения основных индикаторов качества преаналитического этапа:
- ошибки идентификации и транскрипции тестов;
- несоответствие направления установленной форме;
- неверный тип, недостаточный объем образца;
- повреждение образца/направления в ходе транспортировки;
- образец, направление для образца не получены;
- сгусток в образце.
По результатам анализа, проведенного КДЛ РНПЦ РМиЭЧ, несоответствия в целом выявляются для 1,3 % доставленных образцов сыворотки/плазмы. Среди индикаторов с наибольшей частотой встречаются ошибки транскрипции тестов, составляющие 1 %:
- отсутствие отметок о необходимых тестах;
- нечеткий запрос на исследование;
- незаполненные/не полностью заполненные паспортные данные пациента (не обозначен пол, возраст, не указан диагноз, отсутствует печать врача).
Реже определяются ошибки идентификации пробы — нарушение маркировки, в т. ч. расхождения между нумерацией направления и пробы. В 0,34 % случаев пробы не доставлялись в лабораторию, в 0,3 % — для проб отсутствовали направления на исследования. Несмотря на то что выбраковка по причине гемолиза определена на этапе взятия крови и первичной пробоподготовки, в лабораторию в 0,31 % случаев доставляются гемолизированные образцы. В 0,5–1 % случаев в пробах сыворотки встречаются нити фибрина, сгустки, осадок эритроцитов. Регистрируются случаи доставки количества сыворотки, недостаточного для выполнения назначенных тестов. Такие несоответствия являлись результатом неполного соблюдения поликлиниками правил пробоподготовки: выдержки необходимого времени сворачивания крови, соблюдения режима центрифугирования крови и пипетирования сыворотки.
Для образцов сыворотки с выявленными ошибками транскрипции тестов лаборатория выясняет необходимую информацию по телефону, после чего образцы, как правило, принимаются в работу. Указанные действия позволили минимизировать потери образцов по причине нарушений правил преаналитики. Выбраковка с оформлением акта отказа в приеме биологического материала с объяснением причин проводится для гемолизированных образцов либо для случаев, когда доставляется только проба сыворотки без направления и наоборот. Пробы сыворотки со сгустками, эритроцитами подвергаются повторному центрифугированию, после чего выполняются исследования.
Что такое преаналитический этап лабораторных исследований?
Это этап, предшествующий непосредственному выполнению лабораторного исследования пробы пациента, который включает в себя:
- Подготовку пациента к выполнению исследований.
- Забор биоматериала (кровь, моча и т.д.).
- Хранение и транспортировку биоматериала в лабораторию.
Согласно данным статистики по разным источникам, до 70% процентов ошибок в результатах лабораторных исследованийявляются следствием нарушений правил работы именно на преаналитическом этапе. Современное оборудование, используемое в лабораториях, полностью автоматизировано, что исключает влияние человеческого фактора на процесс выполнения исследований. В связи с этим на аналитический этап лабораторных исследований (непосредственно исследование биоматериала в лаборатории) приходится лишь малая доля ошибок в исследованиях.
Так как цель каждого пациента, заказывающего лабораторные исследования – получить точные результаты этих исследований от лаборатории, и, соответственно, правильный диагноз от врача, то в работе лаборатории необходимо обратить особое внимание именно на преаналитический этап исследований.
Перед тем как идти в лабораторию, обязательно обратитесь к ееконсультантам и уточните, какой подготовки требует те анализы, которые Вам необходимы. Тщательно соблюдайте все рекомендации, которые получите у консультантов, и не забывайте, что на этом этапе качество проводимых исследованийнаходится непосредственно в Ваших руках.
Забор материала должен производиться специально обученной процедурной медсестрой с соблюдением всех правил и норм, предъявляемых современными стандартами. Взятый на исследование биоматериал должен быть правильно промаркирован и в кратчайшие сроки доставлен в лабораторию, при этом должны соблюдаться все необходимые правила хранения и транспортировки (такие как температурный режим, влажность и т.д.).
Сроки транспортировки биоматериала– это очень важный критерий при выборе лаборатории. Ведь, как известно, некоторые исследования очень «капризны», и сроки стабильности определяемых в биоматериале показателей невелики. Например, при исследовании свертывающей системы крови, некоторых электролитов (K, Na, Cl), а также некоторых гормонов, биоматериал должен быть доставлен в лабораторию, и его исследование должно быть выполнено в кратчайшие сроки с момента забора, иначе диагностическая точность полученных результатов сводится к нулю.
Только в сети КДЛ «ОЛИМП» лаборатории расположены вгородах республиканского значения (Астана и Алматы), а также вкаждом областном центре, что позволяет обеспечить транспортировку биоматериала из процедурного кабинета в лабораторию вкратчайшие сроки, и тем самым обеспечитьмаксимальную точность результата исследования. Кроме этого, в наших лабораториях вероятность ошибки на преаналитическом этапе сводится к минимуму, благодаря работе тщательно обученного персонала,применению современныходноразовых систем забора крови и других биоматериалов,штрих-кодированию проб сразу по месту забора, а также выполнениювсех современных требований к забору на основе международных принятых стандартов и рекомендаций.
Перед тем как заказать у нас исследования,Вы можете позвонить в наш контакт-центр по номеру 59-79-69 ( для г. Астана и регионов) или 259-79-69(для г. Алматы) и получить консультацию по всем интересующим Вас вопросам. Вы получите информацию о том, как необходимо подготовиться к сдаче каждого анализа, а также сведения о ближайших процедурных кабинетах и времени их работы.
Также Вы всегда можете зайти на наш сайт kdlolymp.kz и ознакомиться с режимом работы процедурных кабинетов в разделе «Где сдать?»
О том, как правильно подготовиться к сдаче анализов читайте здесь.
Кроме того, рекомендуем Вам ознакомиться с видеоинструкциями от нашей лаборатории по подготовке к сдаче анализов:
Как подготовиться к анализам крови:
Как подготовиться к анализам мочи:
Научный редактор
докт. мед. наук, доц. А.Ф. Завалко
Ежедневно в Москве проводятся сотни тысяч лабораторных исследований. В структуре Департамента здравоохранения города Москвы (ДЗМ) насчитывается 235 лабораторий, в которые поступают на анализ пробы из всех городских поликлиник и стационаров. Тысячи врачей получают результаты исследований как в бумажном, так и в электронном виде. В работу Московской лабораторной службы заложена многоступенчатая система контроля качества, практически исключающая вероятность ошибки. Однако зачастую пациенты приходят к выводу, что «в лаборатории что-то перепутали» и «анализы с ошибками». Попробуем разобраться, как анализы москвичей защищены от ошибок и на каком этапе может произойти сбой.
Какой путь проходит каждый анализ
Этап №1 – сбор или взятие биоматериала. К самостоятельно собранному биоматериалу относятся кал, моча и мокрота. Их пациент собирает сам, соблюдая при этом все правила и требования (в противном случае неправильный сбор материала может послужить причиной ошибки в результатах анализов).
Кровь берется у пациента в условиях поликлиники, стационара или на дому лаборантом или медицинской сестрой, при этом соблюдаются определенный порядок и правила, нарушение которых тоже ведет к ошибке в анализе.
Для анализа используется кровь из вены или из пальца. Анализ из венозной крови считается более точным.
Чтобы сдать более сложные биоматериалы, такие как ликвор и выпотную жидкость, пациент должен на короткий срок поступить в стационар.
Этап №2 – транспортировка. Только некоторые, самые простые анализы выполняются в лабораториях при поликлиниках. Большинство же взятых на анализ биоматериалов отправляются в окружные лаборатории.
Этап №3 – анализ. Пробы исследуются на специальных анализаторах, результаты готовы чаще всего в течение 24 часов после доставки проб
в лабораторию (за исключением особых трудоемких анализов, подготовка результатов которых может занять 10–14 суток).
Этап № 4 – получение результатов лечащим врачом (в
бумажной или электронной форме). В первом случае результаты на бумажном носителе привозят в поликлинику, где их отдают врачу, назначившему исследование, во втором – после подписания полученных результатов в лаборатории он автоматически поступают в электронную карту пациента и становятся доступны для просмотра любым врачом. На 2022 год информатизация клинико-лабораторной службы в большей части завершена, поэтому большинство заключений поступает в электронную медицинскую карту пациента и в ЕМИАС, где они становятся доступны для врача.
Полученные результаты анализов врач использует для подтверждения диагноза и назначения пациенту лечения.
Этап №5 – пациент на приеме у врача может ознакомиться с результатами исследования и получить надлежащую помощь. Пациент также может ознакомиться с результатами исследования в своей электронной медицинской карте через портал mos.ru и затем получить назначения врача.
Итак, отследив путь проб, которые собираются для анализа, мы можем сказать: вероятность ошибки есть на каждом из этапов.
Как исследование вашего биоматериала защищено от возможных ошибок
Лабораторный этап исследования – самый защищенный от ошибок. При доставке биоматериала они принимаются специалистом лаборатории (биоматериал может быть не принят, если лаборант заметит нарушение правил маркировки, транспортировки и т.д.). Затем биоматериал оказывается в ведении специалиста, который проверяет работу аппаратуры, контролирует автоматизированные процессы и, в целом, почти не прикасается к пробиркам.
В клинико-диагностических лабораториях системы ДЗМ действует отработанная система контроля качества и исключения ошибок. Анализ проб проводится только при помощи автоматических высокотехнологичных анализаторов, которые проходят систематическую проверку, – в начале каждого рабочего дня и перед каждой загрузкой приборов. Все реагенты и расходные материалы проверятся анализатором на пригодность к работе. При наличии малейшего подозрения на ошибку анализатор останавливает работу.
Всю информацию анализатор передает в базу данных лабораторной информационной системы. Если, несмотря на все меры предосторожности, специалист лаборатории замечает в базе сомнительные результаты, он проводит повторный анализ имеющейся пробы.
На каком этапе возможны ошибки
Согласно статистике, в настоящее время не менее 65 % всех ошибок, связанных с лабораторными исследованиями, происходит на долабораторном этапе. Какими они бывают?
-
Пациент не был надлежащим образом подготовлен к сдаче биоматериала. Например, курил, не соблюдал диету, сдавал кровь не натощак и т. д. Все эти условия отражаются на результатах исследования.
-
Погрешности сбора и хранения биоматериала. Например: немедицинский контейнер, нестерильная тара (для определенных анализов, например, бактериальный посев), слишком длительная транспортировка, неверный температурный режим в холодильнике, где хранились пробы, нарушения условий при перевозке и т. д.
-
Была допущена ошибка при оформлении проб или сопроводительных бумаг. Например: несоответствие номера пробы и номера направления, фамилии на пробе и на направлении, опечатка в фамилии, отсутствие фамилии врача или неточное указание медицинской организации, в которую следует доставить результаты, несовпадение номера страхового полиса с фамилией пациента и т. д.
Точность и педантичность при оформлении проб и документов для проведения исследования – задача сотрудников медицинской организации, которая заказывает анализ.
Что обычно настораживает пациента
Разница в результатах. Например, вы сдали анализы вчера и сегодня, и в показателях есть разница. Или – вы сдали биоматериал в городской лаборатории и в коммерческой лаборатории, и результаты снова разнятся.
Подобные отличия не говорят об ошибке: человеческий организм – это живая система, в ней постоянно происходят изменения. Если пациент болен – заболевание развивается, меняется состав крови.
Лабораторный показатель не должен быть стабилен даже в течение дня, не говоря уже о разнице в 1–2 дня. Лаборатории тоже не работают одинаково: разные приборы, разные реагенты, разные технологии выполнения одних и тех же тестов, у всех свой протокол, поэтому результаты анализов в разных лабораториях отличаются в рамках допустимого значения.
Как сократить вероятность ошибки в лабораторных исследованиях:
Внимательно отнеситесь к правилам подготовки к анализу, соблюдайте все предписания.
-
Правильно собирайте биоматериал, используйте только специальные медицинские контейнеры (при назначении определенных анализов – только стерильные).
-
Если вам выдали направление в бумажном виде, тщательно проверяйте записи на анализ: как написаны ваша фамилия и имя, возраст, номер страхового полиса. Эти ошибки в настоящий момент тоже встречаются редко, однако не лишним будет проявить бдительность.
-
Если вы сдаете повторный анализ в частной лаборатории, учтите, что точное совпадение результатов – скорее неадекватная ситуация. Хороший результат работы обеих лабораторий – небольшие отклонения в рамках допустимого диапазона значений.
-
Не пытайтесь самостоятельно прочесть результат анализа. Если у врача будут трудности с интерпретацией результатов, он всегда может обратиться за консультацией к специалисту лаборатории. Диагноз может поставить только ваш лечащий врач.
-
Никогда не просите медицинского работника трактовать результаты анализа по телефону или поставить диагноз только по одному результату анализа: это просто невозможно.
Следует помнить, что на основании анализов выставлять диагноз неверно! Клинический диагноз выставляется врачом с опорой на клинику, результаты инструментальных исследований и результаты лабораторных исследований.
Никогда не ставьте себе сами диагнозы, не пытайтесь делать выводы только по результатам лабораторных заключений. Позвольте врачу сделать свое дело и диагностировать заболевание в соответствии со всеми принятыми правилами.
Будьте здоровы!
Список литературы:
-
Ибрагимова Э.И., Аимбетова Г.Е., Байсугурова В.Ю. [и др.]. Ошибки в лабораторной медицине: обзор литературы // Наука о жизни и здоровье. 2020. № 1. С. 103–110. DOI:10.24411/1995-5871-2020-10072.
-
Бражникова О.В., Гавеля Н.В., Майкова И.Д. Типичные ошибки на преаналитическом этапе проведения лабораторных исследований // Педиатрия. Приложение к журналу Consilium Medicum. 2017. №. 4. С. 84–90.
Сайт издательства «Медиа Сфера»
содержит материалы, предназначенные исключительно для работников здравоохранения. Закрывая это сообщение, Вы подтверждаете, что являетесь дипломированным медицинским работником или студентом медицинского образовательного учреждения.

Анализ ошибок преаналитического этапа в централизованной лаборатории второго уровня
Журнал:
Лабораторная служба. 2016;5(3): 26‑26
Как цитировать:
Шатненко О.А.
Анализ ошибок преаналитического этапа в централизованной лаборатории второго уровня. Лабораторная служба.
2016;5(3):26‑26.
Shatnenko OA. Analysis of pre-analytical phase errors in a second level centralized laboratory. Laboratory Service. 2016;5(3):26‑26. (In Russ.).

?>
Читать метаданные
Централизованная клинико-диагностическая лаборатория (ЦКДЛ) городской поликлиники №195 представляет, в соответствии с Приказом Департамента здравоохранения Москвы №1051 от 12.12.2014, одну из 10 централизованных лабораторий города Москвы и ее главной задачей является обеспечение населения Западного округа Москвы лабораторными исследованиями, входящими в Реестр обязательного медицинского страхования. Ежедневно в ЦКДЛ обследуется: в клиническом отделении от 400 до 700 пациентов, в биохимическом — от 1,5 до 2,5 тыс. по 50 и 60 параметрам лабораторных исследований соответственно. Таким образом, ежедневно в лаборатории производится от 70 до 90 тыс. исследований. Получение качественных результатов лабораторных анализов это единый цикл, состоящий из трех этапов: преаналитический, аналитический и постаналитический. Для того чтобы повысить качество лабораторных исследований необходимо улучшить все этапы этого процесса. Известно, что на преаналитический этап приходится от 46 до 68% всех ошибок. В результате пациенты не получают адекватного назначения и 19% пациентов дообследуют, что экономически не выгодно. Выработка и соблюдение строгих требований к организации преаналитического этапа сводит к минимуму ошибки, при выполнении лабораторных исследований. Для выполнения этих условий необходим анализ наиболее часто встречающих ошибок. Существующая в нашей ЦКДЛ ЛИС, позволяет вести журнал анализа систематических ошибок преаналитического этапа. В 2015 г. в ОЦКДЛ выполнено 5 435 188 исследований, из 555 589 заказов них было допущено 18 700 преаналитических ошибок, что соответствует 3,4%. Наиболее типичные ошибки, встречающиеся в условиях нашей ЦКДЛ: — 2042 заказов не указан диагноз; — 1861 заказа назначения отмечены разными чернилами; — 1772 пациентов были неполные данные демографии; — сгустки в пробе с К3 ЭДТА зафиксированы в 1421 пробе; — 1008 не было назначений на бланке; — было доставлено 14 проб с отсутствием маркировки; — 96 проб были доставлены без направления; — 293 проб с Na цитратом было нарушено соотношение цитрат-кровь; — 504 направлений были доставлены без пробы. Полученные данные показывают, что необходим постоянный мониторинг за процессом выполнения требований преаналитического этапа. Для улучшения качества преаналитического этапа необходимо: — Совершенствование стандартных операционных процедур; — Проведение обучающих тренингов клинического и лабораторного персонала; — Проведение внешнего и внутреннего аудитов. Все это позволяет повысить эффективность, доступность и качество современной лабораторной медицины.
Авторы:
Шатненко О.А.
ГБУЗ ГП №195 ДЗМ, Москва, Россия
М.О. Егорова
д-р мед. наук, проф. кафедры КЛД ГОУ ВО Российский национальный исследовательский медицинский университет имени Н.И. Пирогова Минздрава России, руководитель отдела развития технологий и обучения Компании «ОМБ»,
Т.П. Сапенко
канд. мед. наук, ведущий специалист отдела развития технологий и обучения Компании «ОМБ»,
Н.В. Патругина
специалист по продукции отдела развития технологий и обучения Компании «ОМБ»
В статье подробно рассмотрены факторы преаналитического этапа, оказывающие влияние на результат лабораторного исследования проб крови, о которых необходимо знать медицинским сестрам. К ним относятся: заполнение бланка-заявки, подготовка пациента к исследованиям, время суток и положение пациента при взятии проб, условия хранения и доставки пробы в лабораторию и многое другое. Представленный материал позволит учесть факторы преаналитического этапа и подготовить стандартные операционные процедуры взятия венозной крови, что повысит качество результатов лабораторных исследований. Клиническая лабораторная диагностика – постоянно развивающаяся область медицины, основная задача которой – получение объективных данных о состоянии здоровья пациента.
Клинические решения основаны на результатах лабораторных исследований, что определяет ответственность лаборатории в соблюдении технологии аналитического этапа. Значительную часть преаналитического этапа выполняют вне лаборатории, однако ошибки, возникающие в этот период, ведут к искажению результатов лабораторного исследования. Выбор необходимых для обследования пациента лабораторных тестов, соблюдение процедуры взятия крови, идентификации пациента и образца зависит от врача-клинициста и процедурной медицинской сестры. Стандартизация процедур преаналитического этапа – задача, решаемая совместно врачом-клиницистом, медицинской сестрой процедурного кабинета, лабораторией и поставщиком медицинской продукции для обеспечения преаналитического и аналитического этапов лабораторного исследования.
На преаналитический этап приходится не менее 50% общего числа лабораторных ошибок [2], которые могут привести к неправильной постановке диагноза и последующему назначению неадекватной терапии. Ценой такой ошибки может стать жизнь пациента.
Одной из основных задач преаналитического этапа является адекватный отбор проб крови и обеспечение стабильности (сохранности) образца.
Практика показывает, что именно стандартизация преаналитического этапа позволяет сократить ошибки диагностики. Важным условием стандартизации преаналитического этапа служит не только соблюдение протокола, но и использование сертифицированных и одноразовых расходных материалов для взятия крови.
Правила заполнения бланка направления
Первый шаг при инициации лабораторного обследования пациента – формирование направления. Бланк-направление в лабораторию для проведения исследований должен содержать информацию о пациенте (Ф. И. О., пол, возраст, домашний адрес, номер страхового полиса), об источнике получения крови (тип образца: венозная, артериальная, капиллярная). Необходимо также указать дату и время взятия крови и, конечно, перечень необходимых исследований.
Источник получения крови (как и возраст) определяет соответствующие референтные значения. Например, существуют различия между концентрацией глюкозы капиллярной и венозной крови. Капиллярная кровь – среда, содержащая интерстициальную жидкость и артериальную кровь, поэтому концентрация глюкозы в капиллярной крови (в среднем 5,4 ммоль/л) выше, чем в венозной (в среднем 4,1 ммоль/л).
Маркировка времени взятия крови на бланке позволяет оценить сохранность компонентов пробы крови до исследования. Наряду с традиционным периодом доставки крови, в течение часа после получения пробы, есть ряд исследований, которые необходимо выполнить в течение 10 мин после взятия крови. Для подобных исследований бланк-направление в лабораторию может иметь специальную пометку и указание способа доставки (вакуумная почта, например) и условий сохранности содержимого пробы. Например, пробы для исследования гемостаза, наиболее чувствительные к условиям хранения,
должна доставлять в лабораторию медицинская сестра клинического отделения. Дополнительно можно предусмотреть предварительное центрифугирование пробы (в случае использования пробирок с разделительным гелем). Это обеспечит последующую сохранность содержимого сыворотки или плазмы до 48 ч при необходимости длительной транспортировки.
Последний момент – перечень необходимых исследований.
Врач, направивший больного на обследование с рукописным бланком, может упустить необходимые и желаемые исследования. Использование лабораторной информационной системы упрощает заполнение бланка, позволяя сделать выбор из списка. Кроме того, по результатам считывания штрихкода в направлении можно получить всю информацию, заключенную в бланке, как о пациенте, так и о направившем его враче.
Факторы, влияющие на результат анализа
В утреннее и вечернее время содержание многих компонентов крови отличается. Суточные биоритмы определяют концентрацию и активность биологических процессов и, например, максимальную экскрецию с мочой фосфатов, катехоламинов, кортизола, альдостерона отмечают в вечерние часы, а натрия – в утренние. Содержание в сыворотке крови гормонов АКТГ, кортизола, адреналина, норадреналина, ренина максимально в утренние часы, тогда как тиреотропного, соматотропного гормона, железа, калия – в вечерние часы [7].
Взятие крови для исследования в утренние часы в одно и тоже время важно и с точки зрения последующего сравнения результатов исследования в динамике. Оценить, что послужило причиной изменения содержания компонента в крови – суточные колебания или влияние терапии, – сложно, если нет развернутой информации о времени исследования, условиях взятия крови, лекарственной терапии, составе пи-
тания, предшествующей физической нагрузке и других факторах. Поэтому по умолчанию кровь берут у пациента утром натощак [7], до любых физиотерапевтических процедур, рентгенодиагностики и УЗИ. Необходимо исключить прием алкоголя и курение за 24 ч до времени сдачи анализа. Курение и прием кофе влияют на результаты исследования многих компонентов (например, С-реактивный белок, билирубин и многие др.). [7, 9]
Физические нагрузки изменяют значения некоторых лабораторных показателей в крови: в первую очередь концентрацию лактата, креатинина, белков и активность ферментов.
После прекращения физической нагрузки длительно, в течение 24 ч и более, сохраняется повышенная активность креатинкиназы и ЛДГ. [9]
Лабораторное обследование выполняют, как правило, неоднократно. Врачу-клиницисту важно получить и увидеть эффект терапии в динамике. Поэтому необходимо выполнять
исследование каждый раз в одно и то же время (учитывая суточные колебания) и получать кровь пациента в одной и той же позиции (в положении лежа или сидя).
От положения тела зависит интенсивность диффузии жидкости в тканевое пространство. В положении сидя концентрация белка, кальция, гормонов, количество клеток в образце будет выше. В некоторых случаях отличия при исследовании проб одного и того же пациента, взятых при разных положениях тела, будут значительными (табл. 1)[3]. Чаще всего горизонтальное положение тела при венепункции предпочтительнее, т. к. при вертикальной позиции происходит отток жидкости из сосудов, изменяя концентрацию аналитов на 5–9% и более.[8]
Таблица 1
Изменение некоторых биохимических аналитов при смене положения пациента: из горизонтального в вертикальное
| Параметр | Увеличение, % |
| Гемоглобин | 5 |
| Лейкоциты | 7 |
| Гематокрит | 13 |
| Эритроциты | 15 |
| Кальций | 5 |
| АСТ активность | 6 |
| Tироксин | 7 |
| IgG | 7 |
| IgA | 8 |
| IgM | 6 |
| Белок | 9 |
| Tриглицериды | 9 |
| Холестерин ЛПВП | 10 |
| Aльдостерон | 15 |
| Эпинефрин | 48 |
| Ренин | 60 |
Фактором, существенно изменяющим или затрудняющим лабораторное исследование образца, служит липемия (хилез), возникающий физиологически в течение 12 ч после приема пищи. Липемия определяется как мутность, видимая невооруженным глазом, в жидкой надосадочной части исследуемых образцов; в крови возникает мутность за счет наличия хиломикронов, носителей экзогенных (пищевых) липидов. [5]
Традиционно используемое понятие «натощак» означает, что последний прием пищи был не позднее 12 ч до времени взятия крови. Отдельные пациенты, например страдающие сахарным диабетом, не могут выдержать столь длительный перерыв в еде. Минимально короткий возможный перерыв (при приеме нежирной пищи) составляет 4 ч. В таком случае можно полагать, что хиломикроны, поступающие из кишечника в кровь, будут уже метаболизированы.
Причин изменения состава образца крови, не связанных с патологическими состояниями пациента, может быть несколько. Нарушение времени последнего приема пищи, поглаживание руки пациента, наложение жгута на период более 1 мин, длительная «работа кулаком» для пациента с фиксированной жгутом веной приводят к гемолизу и гиперкалемии.
Спектральная интерференция (влияние на получаемый результат), вызываемая липемией, в корне отличается от интерференции, возникающей при гемолизе и иктеричности.
Липемия создает помехи за счет присутствия в образце жиросодержащих компонентов, которые, рассеивая свет, образуют молочный или мутный вид образца сыворотки/плазмы крови. Степень рассеяния света зависит от количества, размера и показателя преломления взвешенных частиц (хиломикроны и липопротеиды очень низкой плотности), которые образуют мутность и создают белую окраску сыворотки, называемую хилезом или липемией (рис. 1b).
Гемолиз
Одной из проблем, препятствующей исследованию образца, является гемолиз – нарушение целостности эритроцитов и последующее увеличение во внеклеточном пространстве концентрации внутриклеточных компонентов. Внутриклеточная концентрация некоторых клеточных компонентов в 10 раз выше их внеклеточной концентрации. Гемолиз, обнаруживаемый в плазме/сыворотке крови, служит причиной увеличения концентрации таких аналитов, как калий, лактатдегидрогеназа, аспартатаминотрансфераза, магний.
Спектральная интерференция гемолиза (рис. 1c) определяется выходом внутриэритроцитарного гемоглобина в сыворотку/плазму крови. Гемоглобин отличается высоким поглощением света при характерной для него длине волны.
Отмеченное увеличение или уменьшение результатов при гемолизе зависит от метода и концентрации аналита.
Наличие гемолиза распознают по появлению различной выраженности красноватого окрашивания плазмы или сыворотки крови после центрифугирования. Основные причины гемолиза указаны в табл. 2.
Кроме хилеза и гемолиза, наиболее частую интерференцию результатов исследования может повлечь повышенный уровень билирубина в крови пациента (гипербилирубинемия), обуславливающий иктеричность сыворотки (рис. 2).
Гемолиз в пробе (за исключением исследований, не чувствительных к гемолизу) служит критерием для отказа в принятии лабораторией биоматериала на исследования (ГОСТ Р 53079.4-2008. Технологии
лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 4. Правила ведения преаналитического этапа). [6]
Процедура взятия крови зависит не только от опыта и навыка процедурной сестры, но и от используемого расходного материала для венепункции и получения образца. Пациенты в отделении химиотерапии, пожилые больные требуют специальных приспособлений для комфортной венепункции, таких как игла-бабочка и иглы большего диаметра.
Условия, в которых будет получен адекватный результат, следует оговорить и сообщить пациенту, указав в направлении.
Так, чтобы исключить возможность ложноположительных результатов при исследовании PSA и его растворимой фракции, взятие крови следует проводить не ранее чем через 5 сут после таких манипуляций, как пальцевое ректальное исследование, массаж простаты, трансректальное ультразвуковое исследование (когда датчик вводят в прямую кишку) и после любых других механических воздействий на предстательную железу (клизма, тепловые процедуры и т. п.). Рекомендуют также избегать эякуляции за 2–3 дня до исследования, езды на велосипеде или на лошади, а также употребления алкоголя. [1]
Нельзя забывать, что принимаемые лекарства могут существенно менять состав исследуемого образца. Например, прием единичной дозы железосодержащего препарата накануне исследования может повысить концентрацию железа в исследуемой сыворотке пациента на 300–500 мкг/100 мл, и этот эффект часто маскирует дефицит железа. [4]
В таблице 3 отражены ограничения для некоторых лабораторных исследований. Каждый раз, внедряя новый лабораторный тест, лаборатория изучает инструкцию и сообщает условия взятия биоматериала врачам-клиницистам, медицинским сестрам, в направлении или памятке для пациента.
(Продолжение материала в мартовском номере издания. Следите за новостями!)
Список литературы
1. Говоров А.В. ПСА в деталях // Урология сегодня. 2011. № 6. С. 2–4.
2. Гудер В.Г., Нарайанан С., Виссер Г., Цавта Б. Проба: от пациента до лаборатории / Пер. с англ. Меньшикова В.В. Мюнхен: GIT VERLAG GmbH. 2003. 105 с.
3. Егорова М.О. Биохимическое обследование в клинической практике. М.: Практическая медицина. 2008. 144 с.
4. Тиц Н. Клиническое руководство по лабораторным тестам / Пер. с англ. под редакцией Меньшикова В.В. М.: Юнимед-пресс. 2003. 570 с.
5. Tомас Л., Гиньска E., Митчел C.A., Мэй К. Сывороточные индексы: сокращение ошибок в лабораторной медицине. Результат, которому можно доверять. ООО «РОШ Диагностика Рус». 2013. 12 с.
6. ГОСТ Р 53079.4-2008. Технологии лабораторные клинические. Обеспечение качества клинических лабораторных исследований. Часть 4. Правила ведения преаналитического этапа. 2009.
7. Справочное пособие. Обеспечение качества лабораторных исследований. Преаналитический этап / Под. ред. В.В. Меньшикова. М.: ЛАБИНФОРМ, 1999. 316 с.
8. Blick K.E., Liles S.M. Principles of Clinical Chemistry. NY.: Wiley and Sons. 1985. Р. 697.
9. McCall E., Tankersley M. Phlebotomy essentials. 3-rd edition. Lippincott Williams & Wilkins. 2003. Р. 306.
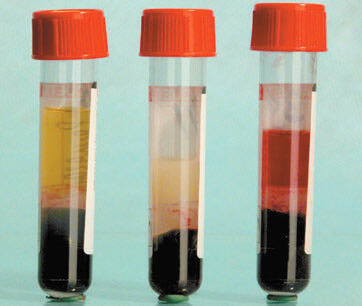
Рис. 1. Вид сыворотки крови после
центрифугирования:
а – сыворотка, пригодная для исследования;
b – образец хилезной сыворотки;
c – образец гемолизной сыворотки

Рис. 2. Вид пробы с различными компонентами
интерференции:
a – хилез;
b – лаковый гемолиз;
c – гипербилирубинемия 100 мкмоль/л;
d – билирубинемия 9 мкмоль/л;
e – билирубинемия 3 мкмоль/л
а b c а b c d e
Таблица 3
ПРИМЕРЫ ОГРАНИЧЕНИЙ (ИЛИ ИХ ОТСУТСТВИЯ) ДЛЯ НЕКОТОРЫХ ЛАБОРАТОРНЫХ ИССЛЕДОВАНИЙ
| Наименование теста |
Предпочтительное время получения образца |
Ограничения по приему пищи |
Примечания |
|
Липидный спектр (общий холестерин, холестерин липопротеидов, триглицериды) |
По назначению врача |
Натощак | — |
| Гормональный профиль |
Утренние часы: 7.00–9.00 |
Натощак |
До приема лекарственных препаратов |
| Коагулограмма |
По назначению врача |
Натощак |
В соответствии с фармакодинамикой лекарственного препарата |
|
Ионы (железо, калий, натрий) |
Утренние часы: 7.00–9.00 |
Натощак | — |
|
Гликозилированный гемоглобин HbA1c, гомоцистеин |
В любое время по назначению врача |
Нет ограничений по времени приема пищи до исследования |
— |

