Механизмы исправления ошибок во время репликации ДНК и ее репарация вследствие повреждений на протяжении всего жизненного цикла клетки.
Основные моменты:
-
Клетки имеют различные механизмы предотвращения возникновения мутаций – необратимых изменений в ДНК
-
В процессе синтеза ДНК, большинство ДНК-полимераз «проверяют свою работу» и проводят замену бо́льшей части ошибочно вставленных нуклеотидов. Этот процесс можно назвать исправлением ошибок.
-
Сразу после синтеза ДНК любые оставшиеся ошибочные нуклеотиды обнаруживаются и заменяются в так называемом процессе репарации ошибочно спаренных нуклеотидов.
-
Если ДНК повреждена, она может быть восстановлена с помощью различных механизмов, например, путём прямой репарации, эксцизионной репарации или путём восстановления двухцепочечных разрывов
- пострепликативной репарации.
Введение
Как ДНК связана с раком? Рак возникает при неконтролируемом делении клеток, когда игнорируются клеточные «стоп»-сигналы, что приводит к образованию опухоли. Это неправильное поведение клеток вызвано накопившимися мутациями — необратимыми изменениями последовательности ДНК клетки.
На самом деле, ошибки в процессе репликации и повреждения ДНК возникают в клетках нашего тела постоянно. Однако в большинстве случаев они не приводят к раку и даже не вызывают мутаций, такие ошибки обычно обнаруживаются и исправляются в процессе репарации ДНК. Если же повреждение исправить не удаётся, то в клетке включается механизм самоуничтожения — (апоптоз), который предотвращает передачу поврежденной ДНК дочерним клеткам.
Мутации возникают и передаются дочерним клеткам только тогда, когда эти механизмы не справляются. В частности, рак возникает в случае накопившихся в одной клетке мутаций генов, связанных с делением.
В этой статье мы подробно рассмотрим механизмы, используемые клетками для исправления ошибок, которые возникают в процессе репликации. К ним относятся:
-
Исправление ошибок – процесс, который возникает во время репликации ДНК.
-
Репарация ошибочно спаренных нуклеотидов, которая происходит сразу же после репликации ДНК.
-
Механизмы репарации, которые выявляют и исправляют повреждения ДНК на протяжении всего клеточного цикла
Исправление ошибок
ДНК-полимеразы — это ферменты, участвующие в репликации ДНК. Во время копирования ДНК большинство ДНК-полимераз «проверяют», корректный ли нуклеотид они добавляют. Этот процесс называется исправлением ошибок. Если полимераза обнаружит, что был добавлен неправильный нуклеотид, она сразу же удалит и заменит его и только после этого продолжит синтез ДНКstart superscript, 1, end superscript.
Репарация ошибочно спаренных нуклеотидов
Процесс исправления избавляет от основной массы ошибок, но не от всех. После создания новой ДНК запускается механизм репарации ошибочно спаренных нуклеотидов — удаления и замены ошибочно спаренных нуклеотидов, оставшихся в результате репликации. Исправление несоответствий между парами оснований также может включать в себя исправление небольших вставок и делеций, возникающих вследствие «соскальзывания» полимеразы с исходной цепи squared.
Как происходит восстановление неправильно спаренных нуклеотидов? Во-первых, белковый комплекс распознаёт неправильно спаренный нуклеотид и связывается с ним. Другой комплекс разрезает ДНК в области несовпадения, а ещё одна группа ферментов отщепляет некорректный нуклеотид вместе с небольшим участком вокруг него. Затем ДНК-полимераза заполняет этот пробел правильными нуклеотидами, а фермент ДНК-лигаза сшивает разрывы в цепиsquared.
Удивительно: как белки, участвующие в восстановлении ДНК, определяют, «кто прав» во время репарации ошибочно спаренных нуклеотидов? То есть, когда два основания неправильно соединены (как G (гуанин) и T (тимин) на рисунке выше), какое из этих двух оснований должно быть удалено и заменено?
У бактерий можно отличить исходную и дочернюю цепи ДНК по метилированным основаниям. На исходной цепи ДНК есть метильные (minus, start text, C, H, end text, start subscript, 3, end subscript) группы, присоединенные к некоторым из ее оснований, а у дочерней цепи таких групп еще нетcubed.
У эукариот процессы, позволяющие идентифицировать исходную цепь при устранении несоответствий, включают распознавание одноцепочечных разрывов, которые обнаруживаются только у дочерней цепи cubed.
Механизмы репарации ДНК
С ДНК может что-нибудь случиться практически в любой момент жизни клетки, а не только во время репликации. Фактически, ДНК постоянно повреждается из-за воздействия внешних факторов: ультрафиолетового излучения и радиации, химических веществ, не говоря уже о спонтанных процессах, которые протекают даже без вмешательства окружающей среды!start superscript, 4, end superscript
К счастью, наши клетки имеют механизмы восстановления, с помощью которых они находят и исправляют большинство повреждений ДНК. Можно выделить несколько типов репарации:
-
Прямая репарация. Некоторые повреждения ДНК, вызванные химическими реакциями, могут быть «исправлены» находящимися в клетке ферментами.
-
Эксцизионная репарация. Повреждение одного или нескольких нуклеотидов ДНК часто исправляется удалением и заменой поврежденного участка. При эксцизионной репарации оснований удаляется только поврежденное основание. В случае эксцизионной репарации нуклеотидов, как и в случае репарации ошибочно спаренных нуклеотидов, которое мы рассмотрели выше, удаляются целиком нуклеотиды.
-
Репарация двухцепочечных разрывов: Существуют два основных способа: негомологичное соединение концов и гомологичная рекомбинация. Они используются для восстановления двухцепочечных разрывов ДНК (когда вся хромосома разделяется на две части).
Прямая репарация
В некоторых случаях клетка может исправить повреждение ДНК, обратив вызвавшую его реакцию. Дело в том, что «повреждение ДНК» — это, как правило, присоединение к ней лишней группы в результате химической реакции.
Например, гуанин (G) может подвергаться реакции с присоединением метильной (minus, start text, C, H, end text, start subscript, 3, end subscript) группы к атому кислорода в азотистом основании. Если это не исправить, метил-содержащий гуанин будет связываться с тимином (Т), а не с цитозином (С) во время репликации ДНК. К счастью, у людей и многих других организмов есть фермент, который может удалить метильную группу, обратив реакцию, и тем самым вернуть азотистое основание в нормальное состояниеstart superscript, 5, end superscript.
Эксцизионная репарация оснований
Эксцизионная репарация оснований — это механизм, используемый для обнаружения и удаления определенных типов поврежденных азотистых оснований. Ключевую роль в нем играет группа ферментов, называемых гликозилазами. Каждая гликозилаза обнаруживает и удаляет определенный вид поврежденных оснований.
Например, в процессе реакции дезаминирования цитозин может превратиться в урацил — основание, обычно встречающееся только в РНК. Во время репликации ДНК урацил будет соединяться с аденином, а не с гуанином (в отличие от цитозина), поэтому такое превращение может привести к возникновению мутацииstart superscript, 5, end superscript.
Для предотвращения подобных изменений гликозилаза, являющаяся частью сигнального пути эксцизионной репарации, обнаруживает и удаляет дезаминированные цитозины. После того, как основание было удалено, удаляется и оставшаяся часть нуклеотида, а другие ферменты заполняют пробелstart superscript, 6, end superscript.
Эксцизионная репарация нуклеотидов
Эксцизионная репарация нуклеотидов — это еще один способ удаления и замены поврежденных оснований. В результате нее обнаруживаются и корректируются повреждения, которые искажают форму двойной спирали ДНК. Например, азотистые основания могут измениться, присоединив к себе громоздкие группы атомов, в частности, в результате воздействия химических веществ, содержащихся в сигаретном дымеstart superscript, 7, end superscript.
Эксцизионная репарация нуклеотидов также используется для устранения повреждений, вызванных ультрафиолетовым излучением, например, при получении солнечного ожога. Под воздействием УФ-излучения цитозин и тимин могут вступать в реакцию с соседними основаниями, которые также являются цитозином или тимином, образуя при этом связи, изменяющие форму двойной спирали и вызывающие ошибки в процессе репликации ДНК. Наиболее распространенный тип таких связей — тиминовый димер — он состоит из двух тиминовых оснований, вступающих в реакцию друг с другом и образующих химическую связьstart superscript, 8, end superscript.
При эксцизионной репарации нуклеотидов поврежденные нуклеотиды удаляются вместе с соседними нуклеотидами. В этом процессе хеликаза (фермент, раскручивающий ДНК) раскрывает ДНК, образуя пузырь, а ферменты, разрезающие ДНК, отсекают поврежденную часть пузыря. Полимераза заполняет пробел, а лигаза сшивает разрыв в цепиstart superscript, 9, end superscript.
Репарация двухцепочечных разрывов
Некоторые факторы окружающей среды, например, радиация, могут вызывать разрывы обеих цепочек ДНК (разделение хромосомы на две части). Такие повреждения ДНК, если верить комиксам, ведут к появлению супергероев, но могут встречаться и после реальных катастроф, например, Чернобыльской.
Двухцепочечные разрывы опасны, потому что большие сегменты хромосом и сотни содержащихся в них генов могут быть потеряны, если разрыв не будет восстановлен. Существует два способа восстановления двухцепочечных разрывов ДНК: негомологичное соединение концов и гомологичная рекомбинация.
При негомологичном соединении концов два разорванных конца хромосомы просто склеиваются обратно. Этот механизм восстановления является «грубым» и неточным, в результате в месте разрыва, как правило, либо теряются нуклеотиды, либо добавляются лишние, что может привести к мутациям. Но это в любом случае лучше потери целого фрагмента хромосомыstart superscript, 10, end superscript.
При гомологичной рекомбинации для восстановления разрыва используется фрагмент из гомологичной хромосомы, который соответствует поврежденной хромосоме (или из сестринской хроматиды, если ДНК была реплицирована). В этом процессе две хромосомы объединяются, и неповрежденная область гомологичной хромосомы или хроматиды используется в качестве матрицы для замены поврежденной области. Гомологичная рекомбинация работает «чище», точнее, чем негомологичное соединение концов, и обычно не приводит к образованию мутацийstart superscript, 11, end superscript.
Репарация ДНК и заболевания человека
Доказательства важности механизмов репарации получены на основе генетических заболеваний человека. Во многих случаях мутации в генах, которые кодируют белки, участвующие в репарации, связаны с наследственным раком. Например:
-
Наследственный неполипозный колоректальный рак (также называемый синдромом Линча) вызван мутациями в генах, кодирующих белки, которые участвуют в репарации ошибочно спаренных нуклеотидовstart superscript, 12, comma, 13, end superscript. Поскольку такие нуклеотиды не восстанавливаются, у людей, страдающих этим синдромом, мутации накапливаются гораздо быстрее, чем у здоровых. Это может привести к развитию опухолей толстой кишки.
-
Люди с пигментной ксеродермой очень чувствительны к ультрафиолетовому излучению. Это вызвано мутациями в белках, участвующих в эксцизионной репарации нуклеотидов. Когда они не функционируют, димеры тимина и другие виды повреждений, вызванные ультрафиолетовым излучением, перестают восстанавливаться. У людей с пигментной ксеродермой после нескольких минут пребывания на солнце могут возникнуть сильные солнечные ожоги, и около половины из них заболевают раком кожи в возрасте до 10 лет, если только они не избегают солнечных лучейstart superscript, 14, end superscript.
Очевидно, что частые шибки при
воспроизведении генетической информации
в процессе репликации, могут подвергнуть
большому риску сохранность видов и их
жизнеспособность. Было установлено,
что частота ошибок при репликации не
превышает 1 ошибки на 109–1010
нуклеотидов. В то же время комплементарность
оснований может обеспечить лишь
существенно меньшую верность
воспроизведения — 1 ошибку на 104–105
оснований. Какие же дополнительные
механизмы повышают верность репликации
еще сто тысяч раз?
Выше уже было сказано, что ДНК-полимеразы
I и III кроме
полимеразной активности обладают еще
и 3-экзонуклеазной
активностью. Оказалось, что если
ДНК-полимераза встраивает неправильный
нуклеотид, она делает шаг назад, отщепляет
этот нуклеотид и повторно включает в
растущую цепь уже правильный нуклеотид.
Возможно, что существуют, особенно в
эукариотических клетках, и другие
механизмы исправления ошибок, возникающих
в процессе репликации.
Интересно, что некоторые эукариотические
ДНК-полимеразы не осуществляют такую
корректировку. По-видимому, в этом случае
точность процесса репликации обеспечивается
с помощью каких-то других средств.
1.2.Мутагенез
Молекулы ДНК живых организмов неизбежно
подвергаются действию различных
повреждающих факторов: химических
реагентов, ультрафиолетового излучения,
и более жесткой радиации (фонового
радиоактивного излучения горных пород,
космических лучей и техногенной
радиации). При этом возникают повреждения
в ДНК. Значительная часть таких повреждений
ДНК исправляется сразу по их возникновении
(см. Раздел 1.2.1,»). Неисправленные
повреждения, передающиеся по наследству,
называются мутациями.
Мутации могут быть нескольких видов.
Изменение одной пары оснований называют
точечной мутацией (замена одного
единственного основания называется
мутацией замещения). Подобная мутация
вызывает замену одной аминокислоты в
полипептиде, кодируемом данным геном.
Если такая замена происходит в вариабельной
части белка, то она мало или совсем не
сказывается на жизнедеятельности
клетки. Если же «неправильная» аминокислота
оказывается в активном центре фермента,
то это, как правило, приводит к потере
ферментом каталитической активности
и к гибели клетки. В редких случаях
полипептидный продукт, получаемый их
мутантного гена, оказывается лучше
приспособленным к выполнению своей
функции в тех новых условиях, в которые
попал организм. Такие мутации дают
потомству преимущества в борьбе за
существование, и серия соответствующих
мутаций может привести к появлению
нового вида.
Точечные мутации замещения составляют
лишь небольшую часть мутаций. Более
многочисленными и более опасными для
клеток мутациями являются мутации,
связанные с вставками и делециями
(вырезанием) нуклеотидов.
1.2.1.Репарация днк
Для исправления повреждений, возникающих
в одной из цепей ДНК, в клетке существует
большая группа ферментов репарации.
Наиболее распространенную стратегию
репарации мы рассмотрим на примере
исправления повреждений, возникающих
при действии такого сильного мутагена,
как азотистая кислота. Основным
результатом действия азотистой кислоты
является превращение цитозина в урацил.
В клетке есть специальный фермент,
урацил-ДНК-гликозидаза, который опознает
урацил и гидролизует гликозидную связь
между урацилом и остатком дезоксирибозы.
В результате в цепи ДНК появляется
дезоксирибозный остаток, не несущий
никакого основания. Появление такого
остатка служит сигналом специальной
эндонуклеазе к выщеплению этого остатка
из цепи ДНК. Образующаяся брешь
застраивается ДНК-полимеразой (специальный
фермент, работающий в системе репарации)
по информации, содержащейся в
противоположной цепи ДНК.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
При репликации
ДНК происходит важный процесс коррекции
вставляемых нуклеотидов (рис. 10). В
область синтеза ДНК поступают все четыре
нуклеотида (на рис. 10 они обозначены как
«претенденты нуклеотиды»). ДНК-полимераза
отбирает нужного предшественника путём
пробного спаривания его с нуклеотидом
ДНК-матрицы.
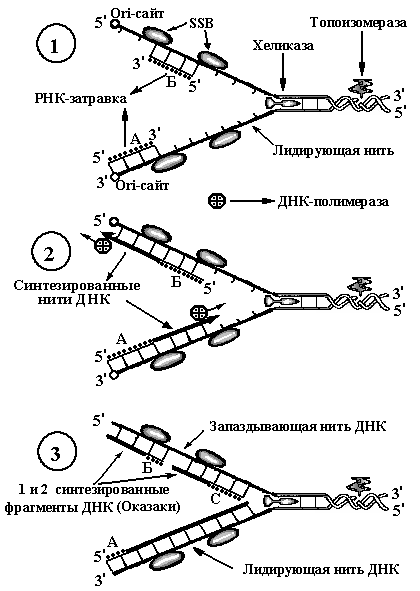
Рис. 7. Схемы
репликации ДНК
13
П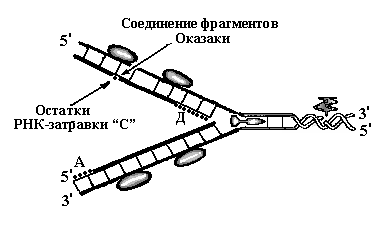 равильность
равильность
подобранного нуклеотида оценивается
по нескольким параметрам, два из которых
наиболее существенны. Во-первых,
подобранный нуклеотид должен формировать
столько же водородных связей, сколько
и нуклеотид на матричной нити.
Рис. 8. Схема
репликации ДНК – стадия элонгации. На
запаздывающей нити синтезировался
третий участок РНК-затравки – «Д».
РНК-затравки «Б» и «С» разрушены и
фрагменты Оказаки, синтезированные с
их концов соединены в единую нить. На
лидирующей цепочке синтез идёт непрерывно,
РНК-затравка «А» разрушается
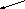


Ориджины
Лидирующая цепь












3’
5’


















5’
3’





Отстающая
цепь


Репликон



Движение
вилок Движение вилок
Рис. 9. Схема
осуществления синтеза ДНК в двух вилках
репликации
Во-вторых,
расстояние между сахарофосфатными
остовами должно быть постоянным и
соответствовать трём гетероциклическим
кольцам в двух основаниях (одно кольцо,
соответствующее пиримидиновому основанию
в одной нити, и два кольца, соответствующие
пуриновому основанию в другой нити).
Если же претендент нуклеотид и нуклеотид
в матрице будут содержать по два кольца
в молекуле или по одному, то соединение
не происходит.
Проверка правильного
включения нуклеотида в растущую цепь
производится дважды: один раз перед
включением его в состав растущей цепи
и второй раз перед включением следующего
нуклеотида.
14
После того как
прошла проверка на совместимость
нуклеиновых оснований, формируется
связь в сахарофосфатном остове.
-
Конвариантная
редупликация как основа мутационной
изменчивости
Этот термин ввёл
в научный обиход учёный-генетик
Тимофеев-Ресовский. Дословно конвариантная
редупликация означает самовоспроизведение
с изменением. Этот процесс лежит в основе
всего эволюционного процесса.
Несмотря на высокую
точность процессов репликации и
эффективно работающую систему коррекции,
во вновь синтезированных нитях ДНК
всегда имеются нарушения. Эти дефекты
чаще всего носят название «генные
мутации». Подсчёты показали, что они
происходят с частотой 1 ошибка на 1010
пар нуклеотидов. Редупликация,
происходящая с ошибками, носит название
конвариантная редупликация.
В основе нарушений
лежат самые различные причины. Например,
высокая или наоборот очень низкая
концентрация нуклеотидов в месте
синтеза, спонтанная потеря пуриновых
оснований (см. далее), дезаминирование
цитозина, который превращается при этом
в урацил под действием ультрафиолетового
облучения, присутствие в месте синтеза
химических мутагенов и т.д. Судьба
возникших ошибок неоднозначна. Они
могут быть исправлены репарационными
процессами (см. далее). Это наиболее
благоприятный для клетки вариант. В
некоторых случаях повреждение в молекуле
ДНК не устраняется. При этом возможны
два варианта разворачивания событий.
Если повреждение молекулы ДНК затронуло
функционально не активную область ДНК,
то фенотипически такая ошибка не будет
выявляться и, как правило, никаких
тяжёлых последствий наблюдаться не
будет. Иное дело, если ошибка спаривания
произошла в нуклеотидных последовательностях
какого-либо гена. В этом случае вероятность
появления фенотипических нарушений
увеличивается. Это может привести к
гибели клетки или целого организма. При
этом вместе с погибшей клеткой
элиминируется и дефект ДНК. И, наконец,
следует учитывать, что генные мутации
лежат в основе мутационной изменчивости.
А она приводит к возникновению
множественных аллелей, которые делают
генофонд популяций более пластичным.
5. Метилирование
ДНК
И в заключении
необходимо остановиться на важном
процессе, который происходит в момент
или сразу же после синтеза дочерних
цепей ДНК – метилирование вновь
синтезированных цепей. У человека
специальный фермент ДНК-метилаза
метилирует цитозин, присоединяя к нему
группы СН3.
Процесс метилирования скорее всего
необходим для формирования структуры
хромосом (упаковки ДНК) и регуляции
транскрипции генов. Кроме того,
метилирование спо-собствует инактивации
одной Х-хромосомы у млекопитающих. У
бактерий метилирование защищает ДНК
от разрезания своими собственными
ферментами.
15
Сахарофосфатный
остов


Водородные




связи



Т
А


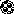










Г
Ц






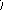



Дочерняя
цепь


ДНК



А
Т



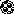
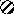
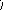






Ц









А
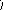




Г






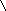

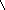





Ц



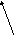
Матричная цепь
ДНК Т


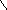


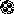




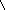

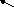

Претенденты
нуклеотиды
Рис. 10. Схема подбора
комплементарного основания к цитозиновому
нуклеотиду (Ц). Среди
претендентов с этим нуклеотидом совместим
только гуаниновый нуклеотид (Г), т.к. он
формирует три водородные связи и имеет
два кольца
6. Лекарственные
препараты и репликация
Процесс репликации
подвержен воздействию самых различных
факторов и, в частности, лекарственных
препаратов. Так, например, дауномицин
и другие противоопухолевые препараты
имеют в своей молекуле плоскую циклическую
структуру, которая встраивается
(интеркалируется) между парами оснований.
Это ведёт к локальному изменению
структуры ДНК, в результате чего ферменты
репликации прекращают свою работу.
Например, топоизомераза теряет
способность деспирализовывать ДНК в
месте интеркаляции. Такие алкилирующие
16
вещества, как
тиофосфамид и др., модифицируют основания
путём присоединения к ним алкильных
группировок. Если ферменты репликации
встречают это основание, их работа может
прекратиться.
Ингибитор
ДНК-топоизомеразы – новобиоцин,
вмешиваясь в работу фермента, прекращает
деспирализацию ДНК, а, следовательно,
и синтез РНК.
Резюме.
Репликация ДНК – процесс точной передачи
информации от ДНК на ДНК в результате
самовоспроизведения матричных молекул.
В репликации различают три периода.
1.
Инициация. Происходит образование
репликационной вилки и образование
РНК-затравки. Синтез начинается
одновременно на множестве участков
ДНК. Перед синтезом ДНК деспирализуется,
водородные связи разрываются и нити
отходят друг от друга.
2.
Элонгация. Синтез РНК начинается с
РНК-затравки и идёт одновременно на
обеих нитях материнской ДНК. На одной
нити синтез идёт непрерывно, на другой
– фрагментами (фрагменты Оказаки).
3.
Терминация. Синтез РНК заканчивается
при встрече репликационных вилок или
на конце молекулы ДНК.
РЕПАРАЦИЯ ДНК
1.Общее представление
о репарации
Процесс репарации
характерен для всех живых существ. Это
одно из основных свойств наследственного
материала, напрямую связанное с
интенсивностью процессов старения,
динамикой развития опухолевых заболеваний,
формированием врождённых пороков
развития, возникновением наследственной
патологии и др. Изменения ДНК, не
подвергшиеся репарации, сыграли (и
играют) важную роль в эволюционном
формировании новых адаптивных свойств
живого.
Остановимся на
трёх важных принципах, характерных для
процесса репарации.
1.
Ферменты репарации определяют место
большинства повреждений на молекуле
ДНК по её локальной денатурации в месте
повреждения.
Эффективность
любой репарационной системы, в первую
очередь, зависит от того насколько
быстро и точно ферменты обнаружат места
повреждений ДНК. Поскольку характер
последних чрезвычайно разнообразен,
то трудно представить существование
многочисленных ферментов, опознающих
«свои» специфические повреждения ДНК.
В действительности всё оказалось проще.
Любое нарушение первичной структуры
ДНК приводит к одинаковым последствиям
– сразу же возникает нарушение в
структуре второго, третьего и т.д.
порядка, т.е. в месте повреждения наступает
локальная денатурация ДНК. Возникшие
в ДНК участки денатурации (в отличие от
первичных повреждений) не специфичны.
Это позволяет специальным ферментам
быстро выявлять денатурированные
17
участки ДНК и
подключать для их восстановления
специфические репарационные системы.
2.
Повреждённый участок на одной нити ДНК
восстанавливается в соответствии с
неповреждённым оппозитным участком
второй нити. При повреждении двух нитей
в восстановлении повреждения участвуют
сестринские нити хроматид.
Отмечена
закономерность, что при воздействии на
ДНК мутагенных факторов, повреждения
в основном касаются одной нити ДНК.
Одновременное повреждение обеих нитей
случается не часто и они, как правило,
заканчиваются гибелью клетки. Восстановить
повреждённый участок не трудно, если
имеется план его первоначального (до
повреждения) строения. Такой план всегда
имеется – это последовательность
нуклеотидов на второй, оппозитной
цепочке ДНК, т.е. в нити ДНК, противоположной
месту повреждения. Здесь располагаются
нуклеотиды, комплементарно отражающие
последовательность нуклеотидов
повреждённого участка. Поэтому многие
репарационные системы «ремонтируют»
повреждённый участок, застраивая его
комплементарными нуклеотидами в
соответствии с планом оппозитного
участка.
Иное дело, если
повреждаются одновременно обе нити
ДНК. Это бывает, когда молекула ДНК с
повреждением вступает в период синтеза
ДНК. В этом случае на дефектной ДНК
происходит синтез дочерних нитей ДНК,
причём на повреждённой нити синтезируется
дефектная дочерняя нить. Но и в этом
случае план повреждённых участков
сохраняется в молекуле ДНК, которая
сформировалась в результате репликации
неповреждённой нити ДНК. При максимальном
сближении сестринских хроматид в профазе
мейоза и митоза происходит репарация
повреждённых нитей ДНК в соответствии
с неповреждёнными участками молекулы
ДНК сестринской хроматиды.
У диплоидных
организмов при репарации повреждённого
участка ДНК возможно использование
плана строения неповреждённого участка
ДНК гомологичной хромосомы.
3.
Энергия на процесс репарации черпается
в основном из АТФ. Но в некоторых случаях
используется энергия фотона света,
который активирует ферменты репарации.
Репарация ДНК –
энергозависимый процесс. В качестве
поставщика энергии используются
макроэргические соединения (например,
АТФ). Однако есть одно исключение – это
фотореактивация (световая репарация).
Фермент, осуществляющий эту реакцию,
использует энергию солнечного света,
а не аккумулированную в химических
связях АТФ. Называется этот фермент –
фотолиаза. Фермент репарирует повреждения,
связанные с образованием тиминовых
димеров (см. далее).
2.Виды репарации
Прежде всего, все
виды репарации (или реакции) делятся на
две большие группы – прямые и непрямые.
Прямые реакции отличаются простотой
и непо-
18
Сахарофосфатный
остов
Азотистые основания
Водородные



связи



Г Ц















УФ
Т А













Т А





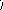
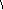






Г Ц








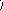

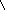



Рис. 11. Схема
образования тиминовых димеров под
действием УФ-облучения. Образовавшиеся
химические связи между тиминами одной
нити показаны пунктирными линиями
средственным
действием на повреждённый объект.
Никаких «предварительных работ» не
проводится. Практически все они
функционируют до периода синтеза ДНК.
К ним относится фотореактивация. При
непрямом типе репарации имеющееся
повреждение ДНК вначале вырезается. В
результате на одной из нитей формируется
брешь, которая застраивается специальными
ферментами в соответствии с планом
расположения нуклеотидов на противоположной
цепи. К этому типу репарации относится
эксцизионная репарация и ряд других.
Прямой тип репарации
Фотореактивация
Неоспоримым фактом
является то, что ультрафиолетовый свет
(УФ) повреждает уникальную молекулу
ДНК. Повреждения в основном касаются
пиримидиновых оснований – тимина и
цитозина. Под влиянием УФ света происходит
19
перераспределение
валентностей в пиримидиновых основаниях,
т.е. между нахо-
дящимися рядом на
одной нити двумя тиминами, двумя
цитозинами или тимином и цитозином.
Следствием этого является появление
необычной химической связи между
основаниями и возникновение димера
(два нуклеотида) – тиминового (тимин-тимин),
цитозинового (цитозин-цитозин) или
тимин-цитозинового. Водородная связь
между оппозитными нуклеотидами при
этом разрушается (рис.11). Есть данные о
том, что пиримидиновые димеры способны
активировать процессы, приводящие к
развитию опухолевых заболеваний.
Возникшая мутация
репарируется несколькими системами
репарации. Одна из них фотореактивация.
Основной фермент этой реакции белок
фотолиаза
имеет сложную
белковую структуру. На одном участке
молекулы находится светочувствительный
центр, воспринимающий фотоны синего
света и активирующий фермент. Фермент
в таком состоянии находит димеры в
молекуле ДНК, разрывает образованные
УФ связи между тиминами и восстанавливает
межнитевые водородные связи пиримидин
– пурин. По завершению цикла фермент
отходит от ДНК.
Следует отметить,
что при этом типе репарации фермент
непосредственно действует на повреждение,
восстанавливая его. Это классический
тип прямой репарации.
Непрямой тип
репарации
Эксцизионная
репарация
Надрез
Расширение бреши Застройка бреши
Сшивка

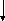
(Эндонуклеаза)
(Экзонуклеаза) (ДНК-полимераза)
(Лигаза)
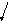



Тиминовый
димер
Рис. 12. Схема
эксцизионной репарации тиминовых
димеров
Тиминовые димеры
могут быть в силу ряда причин не
восстановлены системой фотореактивации.
В этом случае активируются ферменты
системы эксцизионной репарации. Этот
тип репарации позволяет исправить до
95% спонтанных мутаций. Существует
несколько типов реакций эксцизионной
репарации. Их объединяет то, что
повреждённое основание, нуклеотид или
неправильно спаренное основание
(мисмэтч) вначале полностью вырезается
из цепи, а затем вставляется новый
нуклеотид (или нуклеотиды), комплементарный
нуклеотиду противоположной цепочки.
Приведём в качестве примера эксцизионную
репара-
20
цию нуклеотидов
(тиминовых
димеров). Реакция состоит из нескольких
этапов. На первом этапе фермент
эндонуклеаза находит повреждённую нить
ДНК и делает надрез в месте повреждения.
Другой фермент, экзонуклеаза, расширяет
надрез, «откусывая» с обоих концов
надреза нуклеотиды вместе с тиминовым
димером. Образовавшаяся брешь застраивается
с одного конца нити ДНК специальным
ферментом ДНК-полимеразой. При этом
вставляемые нуклеотиды комплементарны
нуклеотидам неповреждённой нити ДНК.
Незастроенным остаётся небольшой
разрыв, который сшивается ДНК-лигазой
(рис.12).
ОБЩЕЕ ПРЕДСТАВЛЕНИЕ
О ТРАНСКРИПЦИИ
Экспрессия гена
– это реализация генетической информации,
закодированной в ДНК, путём её транскрипции
и трансляции.
Транскрипция – первый этап экспрессии
генов. Заключается она в переводе
информации, содержащейся в гене, на РНК
путём синтеза последней на одной нити
ДНК гена. В результате транскрипции
синтезируются все виды РНК – информационная
(иРНК), рибосомальная (рРНК), транспортная
(тРНК) и другие (регуляторные, малые
ядерные и пр.). Все они принимают участие
в экспрессии генов, но только иРНК
переносит информацию о строении белка
с нуклеотидного текста ДНК на аминокислотный
текст белка. Все остальные виды РНК
обеспечивают эффективное осуществление
этого процесса.
Суть транскрипции
заключается в следующем: специальные
ферменты подготавливают молекулу ДНК
в области гена к транскрипции (раскручивают
спираль ДНК, разрывают водородные связи
между нитями и т.д.). Фермент ДНК-зависимая
РНК-полимераза синтезирует РНК на
матричной нити ДНК от стартовой точки
до точки окончания транскрипции. Синтез
РНК заключается в последовательном
наращивании в ней нуклеотидов,
комплементарных матричной нити ДНК.
Исключение составляет урацил РНК,
который вставляется против аденина
матричной нити ДНК.
В транскрипции
принимает участие множество ферментов,
но непосредственно синтез РНК осуществляет
фермент ДНК-зависимая РНК-полимераза
(или просто РНК-полимераза). У прокариот
все виды РНК (иРНК, рРНК, тРНК) синтезируются
одной РНК-полимеразой, а у эукариот они
синтезируются тремя разными ферментами:
РНК-полимеразой I,
РНК-полимеразой II
и РНК-полимеразой III.
Информационные
РНК у
эукариот транскрибируются РНК-полимеразой
II.
Транскрипция –
это сложный многоэтапный процесс и одна
РНК-полимераза не в состоянии полностью
обеспечить его. На разных этапах
транскрипции к РНК-полимеразе
присоединяются и, наоборот, отщепляются
различные белковые субъединицы, которые
модифицируют её активность в соответствии
с требованиями данного этапа.
Транскрипция, как
и все процессы матричного синтеза у
про- и эукариот, состоит из трёх этапов
– инициации, элонгации и терминации.
В дальнейшем процесс транскрипции
будем рассматривать только у эукариот.
21
1. Периоды
транскрипции
Инициация
Инициация – это
подготовительный этап. В эту стадию
происходит множество синхронизированных
во времени процессов. Рассмотрим два
из них:
1. Формирование
инициаторного комплекса.
2. Образование
«транскрипционного глазка».
РНК-полимераза
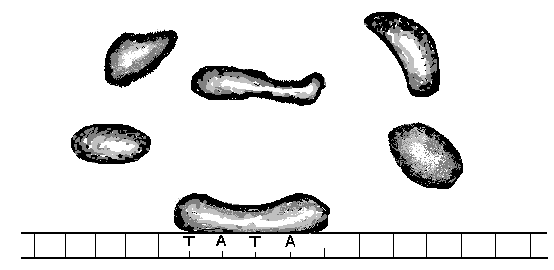





ТФ
ТФ
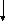


Специальный
белок

Промотор


Инициаторный
комплекс
Промотор
Т А Т А
Рис. 13.
Присоединение РНК-полимеразы и
транскрипционных
факторов к ТАТА-боксу
промотора у эукариот
Формирование
инициаторного комплекса происходит на
промоторе. Сама РНК-полимераза, как
правило, не может связаться с промотором.
Поэтому вначале специальный белок
взаимодействует со специфической
областью на промоторе. В этой области
располагается определённая
последовательность нуклеотидов. Эта
последовательность носит название бокс
Прибнова.
Эта
последовательность нуклеотидов богата
адениновыми и тиминовыми нуклеотидами–
ТАТА. Отсюда и другое название этого
участка промотора – ТАТА-бокс. К
специальному белку, осевшему на промоторе,
присоединяется РНК-полимераза и целый
ряд других белков, которые участвуют в
подготовке синтеза РНК. Таким образом,
на первом этапе на промоторе формируется
сложный комплекс, который состоит из
22
специального
белка, осевшего на промотор, РНК-полимеразы
и нескольких белков, которые носят
название транскрипционные факторы
(ТФ). Их несколько – ТФ1, ТФ2, ТФ3 и т.д.
(рис. 13). У эукариот этих факторов намного
больше, чем у прокариот. Совокупность,
состоящая из специального белка,
транскрипционных факторов и РНК-полимеразы
носит название инициаторный комплекс.
После его образования начинается
формирование вилки транскрипции.
Ферменты комплекса (ТФ1, ТФ2 и др.)
раскручивают спираль ДНК, разрывают
водородные связи между нитями. Нити
расходятся. В результате формируется
транскрипционный «глазок» с вилкой
транскрипции. Разошедшиеся нити этой
вилки прочно фиксируются специальными
белками (SSB),
которые могут не входить в инициаторный
комплекс (рис. 14).
Транскрипционный
«глазок»
Белки,
фиксирующие
разошедшиеся
нити

5’ Смысловая
нить
3’
3’ М атричная
атричная
нить
5’
5’
РНК-полимераза и
РНК
белки
Рис. 14. Транскрипционный
«глазок»
У прокариот
инициаторный комплекс состоит примерно
из пяти субъединиц-полипептидов и
называется голофермент (холофермент).
В комплексе имеется сигма-субъединица
(СС) или сигма-фактор. Это непостоянная
единица комплекса. Она может выходить
из комплекса, тогда комплекс называется
кор-фермент и вновь входить в него (рис.
15). Функция СС заключается в том, что она
первой связывается с промотором, затем
к ней присоединяется кор-фермент. Без
СС кор-фермент практически не
взаимодействует с промотором (или
взаимодействует очень слабо). Другая
функция СС заключается в том, что этот
белок приводит к стойким изменениям в
структуре других полипептидов
комплекса, в
результате чего голофермент приобретает
способность раскручивать спираль ДНК,
разрывать водородные связи между нитями
ДНК, т.е. формировать вилку транскрипции.
СС находится в голоферменте только на
этапе инициации. Обеспечив связывание
комплекса с промотором, она через
некоторое время после начала транскрипции
покидает комплекс и присоединяется к
новым кор-ферментам (см. далее).
У эукариот
инициаторный комплекс более сложный,
чем у прокариот. Помимо фермента
РНК-полимеразы в него входят более 10
полипептидных субъединиц. У них различная
функция. Часть из них, так же как и СС
прокари-
23

+
=



Рис. 15. РНК-полимераза
в зависимости от присоединения к ней
сигма- субъединицы будет иметь различную
структуру и функцию
от, связывается
с промотором. Затем на них осаждается
РНК-полимераза. Другие субъединицы
участвуют в формировании вилки
транскрипции и т.д.
Следует отметить,
что фермент РНК-полимераза про- и
эукариот имеет активный центр, который
контролирует связывание нуклеотидов
первичного транскрипта между собой. В
случае его блокады активность фермента
падает. Некоторые антибиотики, например
рифампицин и его производные, подавляют
инициацию транскрипции, специфически
связываясь с активным центром в
РНК-полимеразе. Интересно то, что
некоторые бактерии оказались не
чувствительны к антибиотику. Исследования
показали, что у таких бактерий
РНК-полимераза имеет небольшое изменение
в структуре. Это изменение не мешает
синтезировать олигонуклеотид, но не
даёт возможности соединиться с активным
центром антибиотику.
После образования
транскрипционного глазка начинается
следующий этап синтеза РНК – элонгация.
Элонгация
Чаще всего начинается
с присоединения к транскрипционному
комплексу специальных белков – факторов
элонгации, которые запускают процесс
синтеза РНК. Точка на ДНК, где начинается
синтез РНК, называется стартовой
точкой.
РНК-полимераза
вместе с белками двигается по нити ДНК,
последовательно раскручивая спираль.
После синтеза РНК нити ДНК вновь
воссоединяются. Деконденсированной
(свободной) в транскрипционном глазке
находится нить ДНК протяженностью около
20 нуклеотидов. Синтез молекулы РНК
идёт от 5’-конца
синтезированной РНК к 3’
–концу, т.е. при репликации (синтез ДНК)
и при транскрипции наращивание новых
нуклеотидов идёт с 3’-конца
синтезируемой цепи ДНК или РНК. Нить
ДНК, на которой синтезируется РНК,
называется плюс нитью, кодогенной,
антисмысловой, матричной цепью (рис.
16).
24
Скорость синтеза
РНК примерно 30 нуклеотидов в секунду.
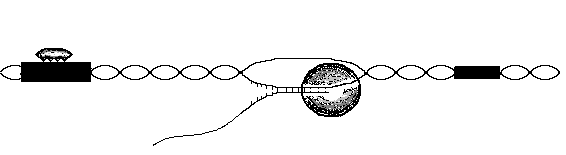
РНК-полимераза
Вилка транскрипции Терминатор
Б

 елок
елок

Направление
синтеза

Промотор
5’
конец РНК
3’
конец РНК
Рис. 16. Элонгация
Терминация
Несмотря на
многочисленные исследования последнего
этапа транскрипции, ясного представления
о его механизме пока не получено. Если
обобщить имеющиеся сведения, то можно
сделать вывод, что у большинства про- и
эукариот терминация осуществляется
несколькими способами. Сущность их одна
– в зоне терминатора располагаются
специальные элементы, которые останавливают
транскрипцию. Таких элементов в настоящее
время найдено несколько. Назовём только
наиболее исследованные. Их три.
1. В зоне терминации
располагается область, богатая ГЦ
парами.
Химические связи
этих нуклеотидов с комплементарными
нуклеотидами в транскрипте существенно
слабее, чем связи АТ. Это облегчает отрыв
синтезированной РНК от ДНК.
2. В терминаторе
имеются «шпильки ДНК».
Другой механизм
связан с имеющимися в области терминатора
последовательностями нуклеотидов,
которые носят название – инвертированные
повторы (см. рис. 17, А). Это два участка
молекулы ДНК, следующие друг за другом,
имеющие одинаковую последовательность
нуклеотидов, но расположенные в
противоположной (обратной) ориентации.
Так, например, последовательности,
представленные на рисунке 17, А, являются
инвертированными, так как при их чтении
от 5’ к 3’-концу они идентичны в обеих
цепях. Такое расположение нуклеотидов
в ДНК терминатора приводит к тому, что
при их считывании на РНК образуются
участки с комплементарными
последовательностями нуклеотидов (рис.
17, Б). Последние соединяются между собой
и формируют фигуру, которая носит
название «шпилька» (см. рис. 17, В). Эта
шпилька, сформированная на пути
РНК-полимеразы, прекращает её движение.
В некоторых случаях «шпильку» распознаёт
специальный белок, который движется по
вновь синтезированной цепочке РНК вслед
за РНК-полимеразой. Обнаружив шпильку,
белок прекращает движение фермента. У
прокариот инвертированные повторы
обнаруживаются
25
практически в
каждом терминаторе. В последнее время
появились данные о более сложных
механизмах терминации транскрипции у
эукариот.
-
Бессмысленные
(нонсенс) кодоны.
Они не кодируют
никакую аминокислоту. Предполагают,
что опознав их, РНК-полимераза прекращает
синтез РНК.
Последовательность
нуклеотидов в ДНК, которая находится
между стартовой точкой и терминатором
называется единицей транскрипции.
Транскрибируется, как правило, одна из
двух цепей ДНК. Могут, но редко,
транскрибироваться обе цепи одного
гена.
Формирующаяся РНК
на нити ДНК носит название транскрипт
или РНК-транскрипт.
2. Ошибки спаривания
при транскрипции.
Лекарственные
препараты и транскрипция
При транскрипции,
так же как и при любом матричном процессе,
происходят ошибки. Их называют ошибки
спаривания. Эти ошибки происходят с
частотой – одна ошибка на 2х104
включённых нуклеотидов. Как мы отмечали
при репликации ошибки возникают намного
реже – одна на 1010
включений.
При ошибках спаривания в растущую нить
РНК включаются «неправильные» основания.
Это может привести к изменению структуры
РНК. Если это касается рРНК или тРНК,
то, как правило, такие «дефектные» РНК
перестают выполнять свои функции –
формирование рибосом и транспорт
аминокислот. Но это практически не
отражается на здоровье человека, т.к.
появление одной «дефектной» молекулы
РНК приходится на несколько тысяч
нормальных молекул, к тому же ошибочное
спаривание очень редкое явление. Более
неблагоприятный прогноз бывает связан
с появлением ошибки спаривания в иРНК
– молекуле, несущей информацию об
аминокислотной последовательности
белка. В этом случае вероятность
реализации генетического дефекта в
фенотипический определяется характером
нуклеотида, образованного при ошибке
спаривания. Хорошо, если в результате
«вырожденности» третьего основания
триплета, новый кодон кодирует ту же
аминокислоту. Такая ошибка фенотипически
не проявляется (см. ранее). Подсчитано,
что в 67% случаев смысл кодона не меняется
при замене нуклеотида в третьем положении
кодона. Хуже когда сформированный на
основании ошибки спаривания кодон
меняет смысл и начинает кодировать
другую аминокислоту. Это приводит к
появлению в белке новой аминокислоты,
которая может изменить функциональные
свойства белка и последний выключится
из клеточного метаболизма. Но и в этом
случае новая аминокислота может по
физико-химическим свойствам (например,
растворимости) быть сравнима с заменённой.
Фенотипические последствия такой замены
менее опасны.
В целом необходимо
отметить, что ошибки спаривания на
уровне транскрипции менее опасны, чем
на уровне репликации.
Транскрипцию могут
ингибировать различные соединения.
Так, например, опасный шляпочный гриб
бледная поганка содержит токсин
альфа-аманитин.
26
Терминатор
Инвертированные
последовательности
А
А
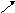
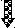
РНК-полимераза

РНК-полимераза
Б
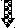
В
5’
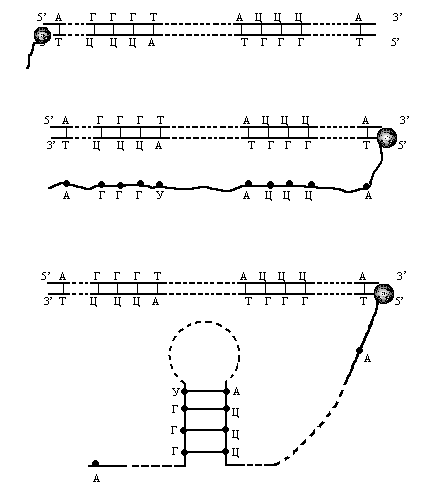
Рис. 17. Терминация.
Образование «шпильки» на РНК при
считывании инвертированных повторов
на матричной нити ДНК. А
– РНК-полимераза «подходит» к области
терминатора. У последнего имеется
инвертированный повтор. Б – РНК-полимераза
синтезировала РНК, в которой имеются
последовательности, комплементарные
инвертированному повтору на матричной
нити ДНК. В – нуклеотиды инвертированного
повтора на РНК сформировали связи, что
привело к образованию «шпильки».
Транскрипция прекратилась
Три характерных
признака этого гриба необходимо помнить
– бледный цвет, «юбочка» на ножке и
булавовидное утолщение в нижней части
ножки.
Этот токсин прочно
связывается с РНК-полимеразой II
у эукариот, которая транскрибирует
иРНК. В результате блокируется транскрипция
многих генов.
Другой токсин –
актиномицин Д является антибиотиком и
прочно связывается с ГЦ-богатыми
участками ДНК. А поскольку такими
участками обогаще-
27
ны рРНК и терминаторы
многих генов, то эти структуры страдают
в первую очередь.
Как мы отмечали
ранее, некоторые противоопухолевые
препараты, например дауномицин и
некоторые другие, содержат в своей
молекуле плоскую циклическую структуру,
которая встраивается (интеркалируется)
между парами оснований. Это ведёт к
локальному изменению структуры ДНК, в
результате чего ферменты транскрипции
прекращают свою работу.
Некоторые
алкилирующие вещества – тиофосфамид
и др. модифицируют основания в ДНК путём
присоединения к ним алкильных группировок.
Если ферменты транскрипции встречают
такие основания, их работа прекращается.
Ингибитор
ДНК-топоизомеразы – новобиоцин,
вмешиваясь в работу фермента, прекращает
деспирализацию ДНК, а, следовательно,
и синтез РНК.
Антибиотик
рифампицин ингибирует только РНК-полимеразу
бактерий, препятствуя инициации
транскрипции. Применяют его при различных
заболеваниях, так как он не действует
на ядерную РНК-полимеразу соматических
клеток человека. К сожалению, в последнее
время обнаружено действие рифампицина
на РНК- полимеразу митохондрий, где
также осуществляется транскрипция
митохондральных РНК. Это является ещё
одним подтверждением версии о том, что
митохондрии являются потомками
прокариотических или иных субмикроскопических
структур, внедрившихся в клетки эукариот
и адаптировавшихся к их метаболизму
так, что стали его полноправными
участниками.
Резюме.
Транскрипция – первый этап экспрессии
генов и заключается она в синтезе РНК
на одной нити ДНК ферментом ДНК-зависимой
РНК-полимеразой (РНК-полимеразой). Состоит
из трёх этапов – инициации, элонгации
и терминации. Во время инициации
формируется инициаторный комплекс,
состоящий из белка, прикреплённого к
промотору, РНК-полимеразы и нескольких
факторов инициации. Одновременно
формируется транскрипционный «глазок».
Во время элонгации происходит наращивание
нити РНК в соответствии с комплементарными
нуклеотидами на матричной (антисмысловой)
цепочке ДНК. Сигналом терминации является
определённая последовательность
нуклеотидов в матричной цепочке ДНК.
При транскрипции чаще, чем при репликации
возникают ошибки при спаривании
нуклеотидов.
3.Посттранскрипционные
процессы. Процессинг (созревание РНК)
Это совокупность
процессов, обеспечивающих превращение
синтезированной РНК (РНК-транскрипта)
в функционально активные РНК (зрелые
РНК), которые могут быть использованы
при синтезе белков. Сами РНК-транскрипты
функционально не активные.
В результате
процессинга изменяется структура и
химическая организация РНК. РНК-транскрипт
до образования зрелой РНК носит название
про-иРНК (или в зависимости от вида РНК
– про-тРНК, про-рРНК), т.е. предшественница
РНК. Практически все РНК-транскрипты
эукариот и прокариот (за
исключением
28
иРНК прокариот)
подвергаются процессингу. Превращение
РНК-транскрипта в зрелую РНК начинается
в ядре, когда синтез РНК ещё не закончен,
и она не отделилась от ДНК. В зависимости
от механизмов различают несколько
этапов созревания РНК:
-
Взаимодействие
про-иРНК с белком. -
Метилирование
про-иРНК. -
Кэпирование
5’-конца. -
Полиаденилирование.
-
Сплайсинг.
Графическая
последовательность этапов изображена
на рисунке 18. Следует отметить, что в
живых организмах все вышеперечисленные
процессы идут параллельно друг другу.
3.1.
Взаимодействие
про-иРНК с белком
У бактерий ещё до
окончания транскрипции 5’-конец
транскрипта сразу же соединяется с
рибосомой и иРНК включается в трансляцию.
Поэтому, для бактериальной иРНК
практически никакой модификации не
требуется. У эукариот синтезированный
транскрипт выходит из ядра, попадает в
цитоплазму и там соединяется с рибосомой.
На своём пути он должен быть ограждён
от случайных встреч с сильными реагентами
и в тоже время должен быть доступен
ферментам процессинга. Поэтому
РНК-транскрипт сразу же по мере удлинения
взаимодействует с белком. Здесь уместна
аналогия – РНК-транскрипт располагается
на белке как на операционном столе, он
фиксируется химическими связями,
одновременно в нём становятся доступными
места модификации. РНК, связанная с
белком, носит название рибонуклеопротеид
(информосома). В такой форме транскрипт
находится в ядре. При выходе из ядра
одни РНК продолжают оставаться в
соединении с белком, другие выходят из
комплекса и принимают участие в
трансляции.
3.2. Метилирование
про-иРНК
Чаще всего происходит
у бактерий, у которых имеется специальный
аппарат защиты от чужеродной ДНК
(фаговой). Этот аппарат состоит из целого
ряда ферментов, разрезающих чужеродную
ДНК или РНК в определённых сайтах, в
которых находится специфическая
последовательность нуклеотидов. Ферменты
носят название рестриктазы.
Понятно, что собственный, только что
синтезированный РНК-транскрипт, также
может быть подвергнут атаке рестриктаз.
Чтобы это не случилось, специальные
ферменты, называемые метилазами,
метилируют собственный РНК-транскрипт
в тех сайтах, которые могут быть разрезаны
рестриктазами. У эукариот РНК-транскрипт
метилируется в меньшей степени.
29
3.3. Кэпирование
5’-конца
Заключается в
химическом и конформационном изменении
5’-конца синтезированной РНК. Кэпирование
происходит в момент синтеза РНК, ещё до
её отделения. Процесс заключается в
присоединении к свободному концу про-РНК
специальных химических веществ, которые
изменяют конформацию концевого участка.
Кэпирование необходимо для инициации
процесса трансляции.


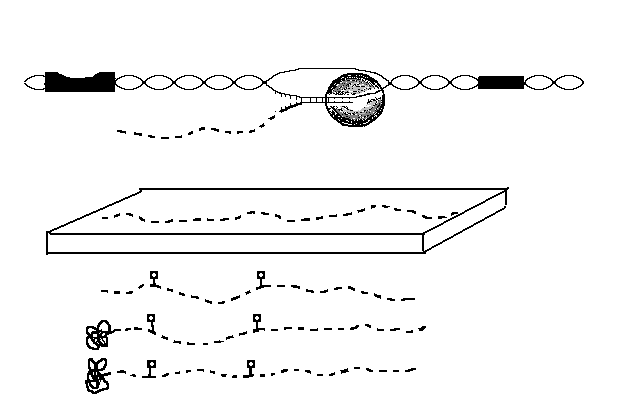
Промотор
Терминатор
Транскрипция

Про-иРНК

П ро-иРНК,
ро-иРНК,
фикси-
Белок
 рванная
рванная
на белке
М етилирование
етилирование
про-иРНК

К эпирование
эпирование
про-иРНК

П







 олиаденилирование
олиаденилирование
Сплайсинг
(см. далее)
Рис. 18. Схема
основных моментов процессинга
Специальные
ферменты присоединяют к 5’-концу про-иРНК
ГДФ (гуанозиндифосфат), а затем метилируют
его (рис. 19).
Функции КЭПа:
-
Инициирует
синтез белка. -
Предохраняет
про-иРНК от распада. -
Участвует в
удалении интронов.
3.4. Полиаденилирование
Это процесс
присоединения к 3’-концу про-иРНК 100 –
200 остатков адениловой кислоты (рис.
20).
30
ГДФ



5’
про-иРНК
СН3
КЭП
= ГДФ + СН3
Рис. 19. Структура
КЭПа на 5’-конце пре-иРНК эукариот
Эти остатки носят
название поли-А последовательности
(поли-А хвосты). Полиаденилированию
подвергаются не все про-иРНК. Например,
молекулы иРНК всех типов гистонов не
содержат поли-А последовательности.
Полиаденилирование предохраняет иРНК
от разрушения.
На растущей цепи
и-РНК имеется специальная последовательность
нуклеотидов (ААУААА). Особый фермент
(полиА-полимераза) находит это сочетание
нуклеотидов, разрезает про-иРНК в этом
месте и формирует полиадениловый
хвостик.
Значение поли-А
последовательностей:
-
Облегчают
выход иРНК из ядра в цитоплазму.
2.Предохраняют
иРНК от разрушения.
ГТФ
ПолиА —
последовательность




рАрАрАрАрАрАрАрА-ОН

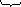
СН3
КЭП =
ГТФ + СН3
Рис. 20. Структура
КЭПа на 5’-конце про-иРНК эукариот и
полиадениловая последовательность на
3’-конце про -иРНК
Недавно было
выявлено ещё одно интересное свойство
поли-А последовательностей – они
участвуют в терминации синтеза про-иРНК.
РНК-полимераза, формируя последовательность
ААУААА в про-иРНК, получает сигнал о
завершении синтеза РНК-транскрипта. Но
синтез сразу не прекращается. Полная
остановка его наступает после того, как
РНК-полимераза встречает на матричной
нити ДНК специфическую последовательность
нуклеотидов (у разных генов она разная),
которая и даёт окончательный сигнал о
прекращении синтеза РНК.
31
3.5. Сплайсинг
В РНК-транскрипте
содержится определённое количество
нуклеотидных последовательностей,
которые были необходимы для успешного
завершения транскрипции и последующей
модификации транскрипта (кэпирования,
полиаденилирования и т.д.). Для выполнения
основной роли РНК в цитоплазме –
трансляции эти последовательности не
только не будут иметь функционального
значения, но могут помешать нормальному
течению синтеза белка. Поэтому в клетке
предусмотрен механизм освобождения
первичного транскрипта от целого ряда
последовательностей, не имеющих решающего
значения в трансляции.
К таким
последовательностям прежде всего
относят интроны.
Ген, с которого
транскрибировалась про-иРНК, содержит
кодирующие и некодирующие последовательности.
Кодирующие последовательности гена
определяют аминокислоты и их
последовательность в белке. Некодирующие
последовательности таким свойством не
обладают. Кодирующие и некодирующие
последовательности в гене чередуются,
и их количество зависит от индивидуальных
генов. В первичном транскрипте также
содержатся кодирующие и некодирующие
последовательности. Такая организация
генов и про-РНК характерна для эукариот.
Некодирующие последовательности
про-иРНК носят название интроны, а
кодирующие – экзоны. Длина интронов
может быть от 50 до 12000 нуклеотидов. Ген
начинается и заканчивается экзоном.
Чередующееся строение гена характерно
для большинства эукариот. Интроны могут
содержать все виды РНК – иРНК, тРНК,
рРНК.
Вся совокупность
экзонов (кодирующих участков) в геноме
человека занимает всего 1,1 – 1,4 %. Средний
ген человека содержит 9 интронов. По
мере упрощения организации организмов
совокупная величина их экзонов возрастает
(например, у бактерий она равна 86 %).
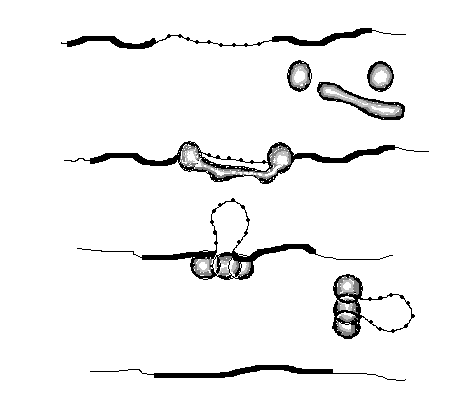
Экзон 1
Интрон Экзон 2
А 



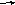
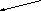
Д
Б

Е
В
Петля
интрона
вырезана
Г

Ж
Рис. 21. Схема
сплайсинга (объяснение в тексте)
32
В вырезании интронов
из РНК-транскрипта и сшивании оставшихся
экзонов принимает участие многокомпонентный
комплекс. Основными его составляющими
являются малые ядерные РНК (мяРНК) и
белки-ферменты.
В целом комплекс
носит название малые ядерные
рибонуклеопротеиды, мяРНП или сплайосома.
Сам процесс достаточно сложен и состоит
из нескольких этапов (см. рис. 21).
1. Формирование
сплайосомы. К началу и концу интрона
прикрепляются фрагменты белка и мяРНК
(рис. 21, Д), формируя сплайосому. Прикрепление
комплекса мяРНП (рис. 21, Е).
-
Сближение
соседних экзонов за счёт образования
петли интрона. Разрезание на границе
экзон-интрон и соединение соседних
(первого и второго) экзонов (рис. 21, В). -
Удаление и
разрушение петли и сплайосомы (рис. 21,
Г, Ж).
Необходимо отметить,
что при повреждении (мутации) интрона
сплайсинг может быть не закончен, интрон
не вырезан и конечный продукт – иРНК
будет нести несвойственные ей
последовательности нуклеотидов. Понятно,
что это может привести к нарушению
трансляции и выключению из метаболизма
опре-
делённого белка.
3.6. Альтернативный
сплайсинг
Такой тип сплайсинга
происходит при экспрессии одного и того
же гена в разных тканях. Сущность его в
том, что один и тот же участок гена в
разных тканях может выступать в качестве
интрона и экзона. Это приводит к
образованию разных иРНК, которые кодируют
белки с различной ферментативной
активностью.
Так в клетках
щитовидной железы синтезируется гормон
кальцитонин. Он тормозит высвобождение
кальция из костей.
Ген, контролирующий
синтез кальцитонина, состоит из 6
экзонов, первичный транскрипт этого
гена (про-иРНК) также состоит из 6 экзонов
(рис. 22). Из первичного транскрипта
формируется зрелая иРНК, содержащая 4
экзона – 1,2,3,4. Экзоны № 5 и 6 были прочитаны
как интроны и вырезаны. На основе такой
иРНК синтезируется кальцитонин. В
клетках головного мозга из первичного
транскрипта, содержащего 6 экзонов,
формируется зрелая иРНК, состоящая из
5 экзонов – 1,2,3,5,6. Четвёртый экзон был
вырезан как интрон. Такая иРНК контролирует
синтез кальцитонинподобного белка,
отвечающего за вкусовое восприятие.
Другой ген Icarus
(названный в честь легендарного Икара)
способен обеспечить за счёт альтернативного
сплайсинга синтез 6 различных полипептидов.
Кроме этого полипептиды образуют между
собой в клетке около 20 различных
ансамблей из одних и тех же полипептидов
или различных.
Нарушение механизма
сплайсинга может привести к патологическим
состояниям, которые носят общее название
талассемии. К ним относят заболевания,
связанные с частичным или полным
подавлением синтеза одной из цепей ге-
33
Ген,
контролирующий кальцитонин
э
и э и э и э и э и
э
Д





 НК
НК
1
2 3 4 5 6
э
и э и э и э и э и
э







про-иРНК
1
2 3 4 5 6


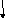
В щитовидной
железе В клетках головного
мозга























иРНК

1 2
3 4 1 2 3 5 6



Кальцитонин
Кальцитонинподобный
белок
Рис.22. Альтернативный
сплайсинг кальцитонина и кальцитонинподобного
белка
моглобина (α- или
β-цепи). Например, болезни, связанные с
недостатком синтеза β -цепи гемоглобина,
могут возникнуть в результате мутаций
в двух участках гена, кодирующего β-цепь
– в сайте, ответственном за полиаденилирование
и в одном из интронов. В первом случае
нарушается процесс формирования
полиаденилового хвостика и формируется
неполноценная β-цепь гемоглобина. Во
втором случае сплайосома не способна
вырезать повреждённый интрон и зрелая
иРНК β-цепи гемоглобина не образуется.
В любом случае нормальная функция
эритроцитов будет существенно нарушена.
Резюме.
Процессинг (или созревание РНК) –
это процесс
превращения только что синтезированной,
не активной РНК (про-иРНК) в функционально
активную РНК. Процесс связан со
структурными и химическими модификациями
про-иРНК. Он происходит в ядре до момента
выхода РНК в цитоплазму и состоит из
нескольких этапов: присоединение
про-иРНК к белку, метилирование некоторых
оснований, маркировка одного из концов,
полиаденилирование друго-
34
го (противоположного)
конца, вырезания интронов и сшивания
экзонов. Последние два процесса носят
название сплайсинг.
ТРАНСЛЯЦИЯ
-
Общее
представление о трансляции.
Материальное
обеспечение процесса
Трансляция – это
процесс переноса информации (декодирование
её) в рибосомах с иРНК в аминокислотную
последовательность белка. Это сложный
процесс, имеющий собственное сырьевое,
ферментативное и энергетическое
обеспечение.
В трансляции
задействованы следующие органические
соединения и органоиды:
-
иРНК.
-
тРНК.
-
рРНК.
-
Различные ферменты.
-
Рибосомы.
-
АТФ.
Рассмотрим их
подробнее.
1) иРНК.
В предыдущем
разделе мы описали как «созревает» иРНК
во время и после транскрипции. У эукариот
этот процесс идёт практически всё время
пока иРНК находится в ядре, где она
связана с белком и представляет собой
рибонуклеопротеид, называемый
информосомой. Переходя в цитоплазму,
иРНК выходит из комплекса с ядерным
белком и через ядерные поры попадает в
цитоплазму, где вновь связывается с
белком, формируя цитоплазматическую
информосому. В виде информосомы иРНК
может существовать в цитоплазме
достаточно долго.
Фактически это
выработанная в эволюции форма депонирования
иРНК в клетке. При необходимости, например
во время митоза, когда сильная компактизация
хромосом практически выключает синтез
всех видов РНК, информосомы распадаются
и освободившаяся иРНК включается в
трансляцию.
2) тРНК.
тРНК в ядре, также
как и иРНК, соединена с белком и
представляет собой рибонуклеопротеид.
Попадая в цитоплазму, она также соединяется
с белками. Основная функция тРНК –
доставка аминокислот к месту синтеза
белка.
Существует около
20 тРНК. Их пространственная структура
универсальна (см. рис. 23).
Отметим три
особенности в структуре тРНК.
1. Наличие в тРНК
минорных оснований. Эти основания
существенно отличаются по физико-химическим
параметрам от классических оснований,
имеющихся в иРНК и рРНК. Это придаёт
молекуле тРНК целый ряд свойств, которые
не характерны для других РНК. Например,
молекулы тРНК достаточно
35
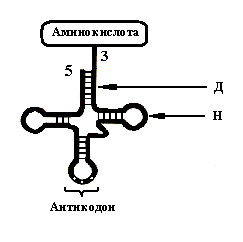
Рис. 23.
Пространственная структура тРНК
стойкие и не
подвергаются разрушительному действию
внутриклеточных нуклеаз.
2. В нити тРНК
выявлены участки, где имеются обратные
повторы нуклеотидов. Это приводит к
тому, что при сближении между собой
обратные повторы создают двунитчатые
структуры за счёт образования
комплементарных пар между основаниями
обратных повторов. На рисунке один такой
участок обозначен буквой «Д». Другие
участки тРНК из-за отсутствия
комплементарных повторов остаются
неспаренными. На этом же рисунке один
такой участок обозначен буквой «Н».
Наличие в нити тРНК участков с уникальной
последовательностью нуклеотидов и
обратными повторами создаёт своеобразную
вторичную структуру тРНК, называемую
«кленовым листом».
3. В структуре тРНК
имеются две области, значимые для
трансляции – область антикодона
и область
присоединения аминокислоты. Антикодон
– группа из трёх нуклеотидов,
располагающаяся примерно в середине
тРНК. Антикодон занимает фиксированное
положение и комплементарен кодону,
находящемуся в информационной РНК.
Другая область – 3’
–конец тРНК. К нему специальный фермент
присоединяет аминокислоту. Комплекс
тРНК с аминокислотой носит название
аминоацил-тРНК. Таким образом, в синтезе
белка принимают участие не свободные
аминокислоты, а аминокислоты в составе
аминоацил-тРНК.
Фермент, который
присоединяет аминокислоту к тРНК, имеет
два распознающих центра (рис.24). Один
центр определяет необходимую тРНК путём
взаимодействия с некоторыми специфическими
областями на её молекуле (петлями и в
некоторых случаях с антикодоном). Другой
центр распознаёт среди массы окружающих
его в цитоплазме аминокислот ту, которая
соответствует триплету в антикодоне.
После того как фермент определил
необходимую
36
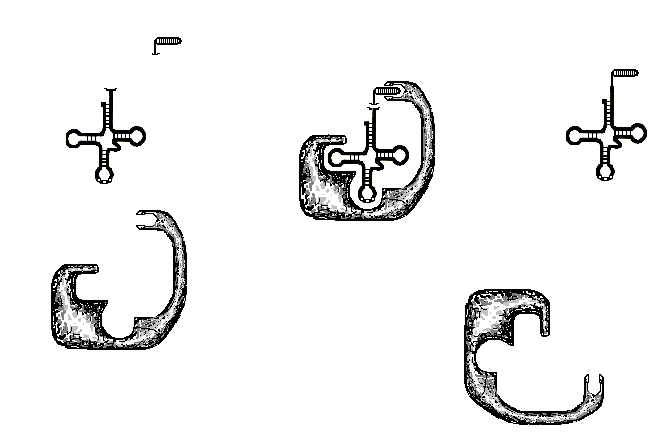

Аминокислота

Петля



тРНК


Фермент
А
Б
В
Рис.24. Схема
формирования аминоацил-тРНК. А
– компоненты– тРНК, аминокислота,
фермент; Б – фермент присоединяет
аминокислоту к тРНК в соответствии с
петлёй тРНК; В – после присоединения
фермент удаляется, а тРНК остаётся с
присоединённой аминокислотой
тРНК и аминокислоту
происходит присоединение аминокислоты
к 3’-концу
тРНК.
3) рРНК
рРНК синтезируются
на структурных генах и после процессинга
накапливаются в ядрышке ядра. В ядрышке
в зависимости от молекулярного веса
различают несколько типов рРНК. Все они
участвуют в строительстве рибосом,
являясь своеобразным каркасом, к которому
прикрепляется множество различных по
структуре и функции белков. Объединяет
белки то, что они являются участниками
различных этапов трансляции. Белки в
ядрышко поступают через ядерные поры
из цитоплазмы. Таким образом, в ядрышках
формируются «полуфабрикаты» малой и
большой субъединиц рибосом. В таком
виде они выходят через ядерные поры в
цитоплазму, где формирование малой и
большой субъединиц полностью заканчивается.
В полностью сформированной малой
субъединице расположена одна рРНК, в
большой – их несколько. рРНК, находясь
в рибосомах, выполняет несколько функций,
главные из которых следующие:
— рРНК является
каркасом для формирования белковой
основы рибосом,
— рРНК принимает
участие в формировании инициаторного
комплекса,
— рРНК обеспечивает
взаимодействие тРНК с мРНК.
В цитоплазме малая
и большая субъединицы находятся в
диспергированном состоянии (отдельно
друг от друга).
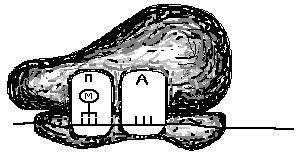
4) Рибосома.
Состоит из малой
и большой субъединиц. Важно отметить,
что в большой и малой субъединице имеются
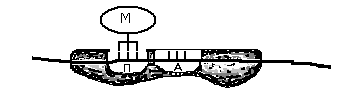
два функциональных центра: –
«П» (пептидильный) и «А» (аминоацильный),
объединяющиеся после соединения
субъединиц (рис. 25).
37
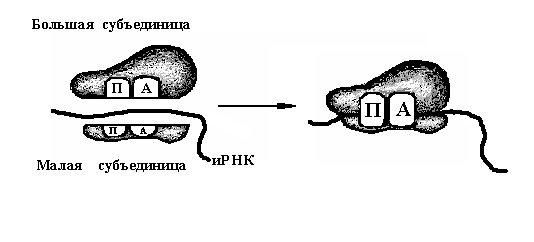
Рис. 25. Два
функциональных центра в рибосоме до
соединения субъединиц и после
Процесс трансляции,
как и любой процесс матричного синтеза,
состоит из трёх стадий – инициации,
элонгации и терминации.
2. Периоды
трансляции
Инициация
Рибосомы находятся
в цитоплазме в трёх состояниях:
— диспергированном,
когда большая и малая субъединицы
находятся отдельно друг от друга;
— в состоянии
комплекса, когда малая и большая
субъединицы объединены в один ансамбль,
а между ними проходит иРНК;
— в форме полирибосомы
(полисомы) – на одну нить иРНК «нанизаны»
несколько рибосомальных комплексов.
Каждый из них синтезирует белок.
Во время инициации
происходит процесс формирования
инициаторного комплекса. В него входит
три следующих друг за другом этапа.
1. Малая субъединица
рибосомы определяет 5’-конец
иРНК, содержащий «кэп», и присоединяется
к нему.
2. Скользя по иРНК,
малая субъединица «находит» расположенный
вблизи «кэпа» стартовый кодон. В этом
месте субъединица останавливается и
фиксируется на иРНК. Сформировалась
система, состоящая из двух элементов —
малой субъединицы и нити иРНК. Система
устроена таким образом, что в малой
субъединице располагается только 2
кодона, каждый из них занимает свою
активную область или центр, либо П-центр,
или А-центр. Стартовый кодон располагается
в функциональном центре «П» (рис. 26, А).
В другом функциональном центре (А)
располагается кодон первой аминокислоты,
входящей в белок. Ещё раз подчеркнём,
что два функциональных центра в малой
субъединице не активны. Они активируются
только при присоединении большой
субъединицы, в которой находятся
аналогичные центры П и А.
38

Кэп
Стартовый кодон



![]()
А
+
=
Малая
субъединица
иРНК
![]()
Б![]()
+ =
Метиониновая
Инициаторный
аминоацил-тРНК
комплекс
![]()

В
+
=
Большая
субъединица
Рис. 26. Схема
формирования инициаторного комплекса
и рибосомы. А
– малая субъединица рибосомы соединяется
с иРНК, Б – антикодон метиониновой-тРНК
соединяется с кодоном иРНК в участке
«П». Формируется инициаторный комплекс,
В – инициаторный комплекс соединяется
с большой субъединицей рибосомы.
Формируется рибосома
У многих организмов
стартовый кодон (или инициирующий кодон)
в иРНК содержит триплет, комплементарный
антикодону аминоацил-тРНК, несущей
метионин. С метионинового кодона, как
правило, начинается синтез белка.
3. К стартовому
кодону, находящемуся в «П» участке,
прикрепляется аминоацил-тРНК, несущая
аминокислоту метионин. Комплекс,
состоящий из малой субъединицы рибосомы,
иРНК, метиониновой-тРНК, называют
инициаторным комплексом (рис.26, Б).
Элонгация
Как только к
инициаторному комплексу присоединяется
большая субъединица рибосомы, начинается
этап элонгации. С присоединением большой
субъединицы в рибосоме формируется два
полноценных функциональных центра «П»
и «А». В обоих центрах размещаются только
два кодона иРНК. В центре «П» находится
метиониновая-тРНК, а к участку «А»,
который открыт в цитоплазму, пробуют
присоединиться аминоацил-тРНК, несущие
разные аминокислоты. Присоединяется
только та аминоацил-тРНК, антикодон
которой компле-
39
![]()

![]()
![]()
Инициаторный
комплекс
![]()
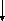
![]()
![]()
![]()
![]()


![]()
3’

![]()
![]()
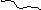
![]()
![]()
Б
А![]()

3’
3’
Г
В


3’
3’
Д
Е

3’
3’
Ж
З
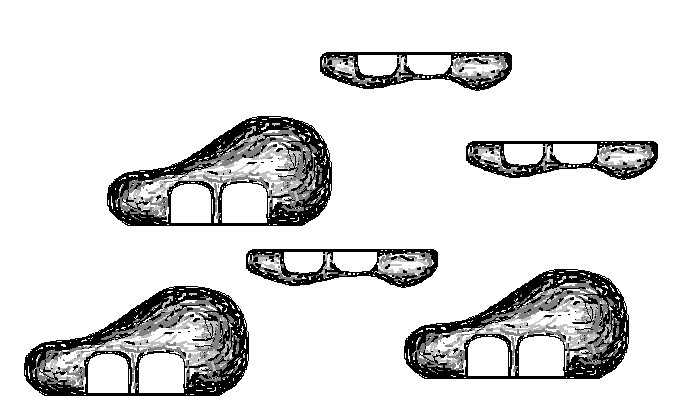
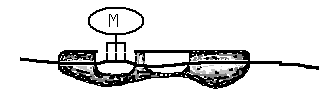
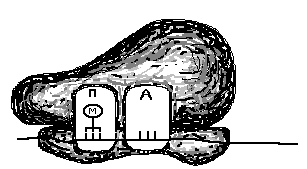
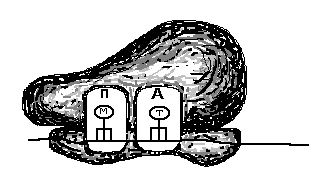
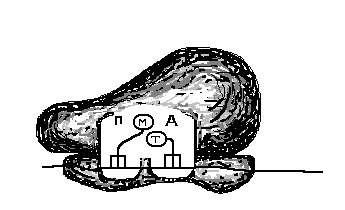
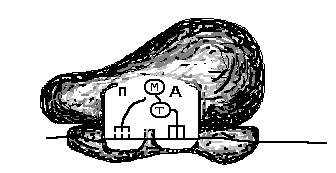
Рис. 27. Схема
трансляции. А
– компоненты аппарата трансляции
(малая, большая субъединицы рибосом,
иРНК, аминоацил-тРНК, тРНК и аминокислоты)
в цитоплазме перед началом синтеза
белка, Б – инициаторный комплекс, В –
начало элонгации. Большая и малая
субъединица соединены, в функциональном
центре «П» аминоацил-тРНК с метионином
(М), Г – в функциональном центре «А»
аминоацил-тРНК с триптофаном (Т), Д –
соединение аминокислот метионина и
триптофана в функциональном центре
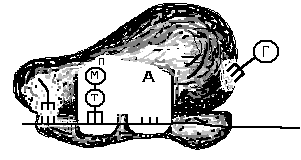
«А», Е – образовался дипептид, состоящий
из аминокислот метионина и триптофана,
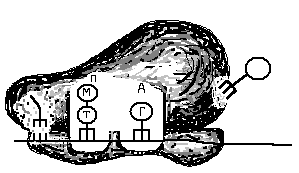
Ж – перемещение аминокислот вместе с
иРНК в центр «П», З – центр «А» заполнен
аминоацил-тРНК, которая несёт аминокислоту
глицин (Г).
ментарен кодону
иРНК, находящемуся в «А» участке. В
нашем случае в «А»участок попадает
триптофановая аминоацил-тРНК (Т) (рис.27,
В, Г).
Специальные
ферменты соединяют пептидной связью
две аминокислоты, находящиеся в
функциональных участках между собой
(рис. 27, Д). Одновремен-
но происходит
разрыв между тРНК и аминокислотой
метионином. Метионин ос-
40
таётся присоединённым
к триптофану в участке «А», а в участке
«П» находится освобождённая от
аминокислоты тРНК (рис. 27, Е). Специальный
фермент, используя энергию макроэргов
(АТФ) продвигает рибосому по иРНК на
один триплет (шаг) по направлению к 3’
-концу иРНК.
При этом из участка «П» тРНК освобождается
и выходит в цитоплазму, а её место
занимает аминоацил-тРНК, несущая
триптофан (Т) и прикреплённый к триптофану
метионин (М). «А» центр становится
свободным и на кодон, находящейся в нём
иРНК, начинают претендовать другие
цитоплазматические аминоацил-тРНК
(рис. 27, Ж). Присоединяется та аминокислота,
антикодон которой комплементарен кодону
иРНК «А» участка (рис. 27, З). Затем цикл
повторяется.
Функциональные
обязанности малой и большой субъединиц
рибосом различны. Малая субъединица
присоединяет аминоацил-тРНК (т.е.
декодирует информацию), а большая
субъединица отвечает за образование
пептидной связи между аминокислотами.
Терминация
Окончание трансляции
происходит тогда, когда в «А» участок
рибосомы попадает один из стоп-кодонов
(УАГ, УАА, УГА). Для них нет соответствующих
аминоацил- тРНК и процесс синтеза белка
останавливается.
К стоп-кодону
присоединяются факторы терминации
(белки), которые активируют ферменты,
находящиеся в рибосомах. Эти ферменты,
в свою очередь, осуществляют процесс
отщепления синтезированного белка от
тРНК и вызывают диссоциацию рибосомы
на субъединицы. Следует отметить
интересный феномен, наблюдаемый во
время терминации. Ранее мы отмечали (см
раздел «Процессинг»), что конец нити
иРНК, где располагается терминатор,
заканчивается полиадениловым «хвостиком»
–
поли-А. При окончании синтеза полипептида,
рибосома отсоединяется от нити иРНК,
«откусывая» при этом одно адениловое
основание от поли-А. Следующая рибосома,
завершив синтез, также отщепляет одно
основание и т.д. Как только все основания
будут утрачены, иРНК разрушается
ферментами. Таким образом, поли-А являются
своеобразными биологическими часами,
отмеряющими длительность существования
иРНК и количество синтезированных с
определённой иРНК белков. Чем длиннее
поли-А, тем больше молекул белка будет
синтезироваться с этой иРНК и наоборот.
Нарушение
трансляции
Трансляция, как и
другие процессы матричного синтеза,
может быть нарушена различными факторами
внутренней и внешней среды. Достаточно
часто такие нарушения связаны с
воздействием на процесс химических
агентов самой различной природы. В
медицинской практике нарушение трансляции
может происходить при употреблении
антибиотиков. В этом случае в основе
механизма повреждения ДНК чаще всего
лежат три феномена.
41
1. Антибиотик может
связаться с активным центром рибосомы
(например,
с «П» или «А»
центром) и блокировать взаимодействие
с этим центром участников процесса
трансляции. Так стрептомицин связывается
с «П», а тетрациклин с «А» центром рибосом
у микроорганизмов, полностью подавляя
их активность. Следует отметить, что в
рибосоме человека другая структура
этих центров, поэтому с ними эти
антибиотики не связываются. Однако
другой антибиотик – пуромицин связывается
с «А» центром рибосом человека и
прекращает трансляцию. Понятно, что в
качестве лекарственного препарата его
можно использовать с очень большой
осторожностью.
2. Другой механизм
действия веществ, нарушающих синтез
белка, заключается в присоединении их
к какому-либо ферменту-участнику синтеза.
В этом случае фермент выключается из
процесса. Так, дифтерийный токсин
инактивирует некоторые ферменты на
этапе элонгации.
3. Дистантный
механизм действия химических соединений
заключается в воздействии химического
агента не на сам процесс трансляции, а
на структуры, которые определяют его
течение. Такие структуры располагаются
в различных областях клетки. Ими могут
быть рецепторы, располагающиеся на
поверхности плазматической мембраны.
Химический агент, связываясь с рецептором,
индуцирует в цитоплазме цепочку
биохимических реакций, которые влияют
на интенсивность трансляции, вплоть до
её полного прекращения. Примерно так
действует интерферон.
Резюме.
Трансляция –
это перевод информации из полинуклеотидной
последовательности иРНК в аминокислотную
последовательность белка. Осуществляется
этот перевод путём синтеза белка на
матрице – иРНК. В трансляции принимают
участие рибосомы, тРНК, рРНК, различные
ферменты. Состоит из трёх этапов –
инициации, элонгации и терминации. На
стадии инициации образуется инициаторный
комплекс, который состоит из малой
субъединицы рибосомы, иРНК, тРНК, несущей
метионин. После присоединения к нему
большой субъединицы рибосомы наступает
стадия элонгации, которая заключается
в присоединении тРНК, несущих аминокислоты
к иРНК, и связывании аминокислот друг
с другом. Процесс происходит в двух
активных центрах, расположенных на
границе малой и большой субъединиц.
Трансляция заканчивается, когда в
рибосому попадает «бессмысленный»
кодон, не кодирующий аминокислоты.
3. Посттрансляционные
процессы. Фолдинг и модификация белка
После освобождения
синтезированной полипептидной цепи из
связи с рибосомой начинается фолдинг
– сворачивание полипептидной цепи в
определённую третичную структуру. В
этом процессе могут принимать участие
специальные соединения, находящиеся в
клетке. Небольшие полипептидные цепочки
приобретают третичную структуру
спонтанно. В укладке полипептидов с
высоким молекулярным весом принимают
участие специальные ферменты, например
42
шапероны и такие
ионы как кальций. Другой, не менее важный
процесс – модификация некоторых белков
заключается в присоединении к ним
углеводного или
другого компонента.
В результате формируются сложные белки,
например, гликопротеины.
ЭКСПРЕССИЯ ГЕНОВ.
ОСОБЕННОСТИ ЭКСПРЕССИИ ГЕНОВ
У ПРО- И ЭУКАРИОТ
Термин «экспрессия
гена» происходит от латинского слова
expression
– выражение. В зависимости от типа гена
его информация может быть выражена в
структуру какой-либо РНК (тРНК, рРНК или
мяРНК) или в структуру определённого
белка (белка-фермента, строительного
белка, сигнального белка, белка-регулятора
и т.д.). Поэтому существует несколько
определений экспрессии гена.
Мы рассмотрим
определение, характерное для генов,
несущих информацию о белке-ферменте.
Для них наиболее распространённым
понятием экспрессии является следующее:
экспрессия генов –
это совокупность процессов в клетке,
обеспечивающих реализацию информации
гена в признак.
1. Этапы экспрессии
генов у эукариот
В сформированном
организме эукариот экспрессия
структурных генов, несущих информацию
о структуре белка, состоит из нескольких
этапов: транскрипции – процессинга –
трансляции – фолдинга – биохимического
процесса, участником которого является
белок-фермент – физиологической реакции
и признака. Сразу же отметим, что мы
представили наиболее полную схему
экспрессии генов. На самом деле для
некоторых структурных генов, кодирующих
ферменты, этапы экспрессии могут быть
другие. Например, может отсутствовать
фолдинг, может отсутствовать физиологический
процесс и биохимический цикл может
сразу реализоваться в какой-либо признак
и т.д.
2. Особенности
экспрессии генов у прокариот
Последовательность
событий, приводящих к экспрессии генов
у прокариот, в целом сходны с таковыми
для эукариот. Однако есть и существенные
отличия. Приведём наиболее значимые из
них.
-
В реализации
генетической информации у прокариот
отсутствует процессинг. -
Поскольку в
прокариотической клетке отсутствует
пространственное разграничение ядра
и цитоплазмы, а так же по ряду других
причин у прокариот процессы транскрипции
иРНК и трансляции с этой иРНК информации
происходят одновременно.
Цепочка реализации
гена в признак у прокариот короче, т.к.
упрощён (или отстутствует) громоздкий
аппарат физиологических реакций.
43
3. Регуляция
экспрессии гена
Одно из замечательных
свойств про- и эукариот заключается в
их способ-
ности осуществлять
дифференциальную регуляцию экспрессии
генов. Это даёт возможность клеткам и
организмам приспосабливать свой фенотип
к определённым условиям внешней и
внутренней среды. А поскольку фенотипические
признаки клеток разных типов в различных
условиях зависят от количества и свойств
продуцируемых ими структурных,
каталитических и регуляторных белков,
то в основе большинства регуляторных
механизмов лежит регуляция одного или
нескольких этапов считывания информации
при синтезе этих белков. В настоящее
время известно достаточно большое
количество механизмов регуляции. Их
обычно рассматривают в зависимости от
того звена в экспрессии генов, которое
они регулируют – регуляция транскрипции
РНК (инициация, элонгация и терминация),
регулирование перехода РНК из ядра в
цитоплазму (у эукариот), регуляция
трансляции (инициация, элонгация и
терминация), фолдинга и т.д. Все эти этапы
у про- и эукариот контролируются
специфическими механизмами, однако
логика этих процессов в целом одинакова.
Не будем рассматривать все известные
в настоящее время механизмы регуляции
экспрессии генов. Их много. Остановимся
на регуляции одного этапа в экспрессии
генов – инициации транскрипции. Регуляция
активности генов на этом уровне широко
распространена среди организмов и
наиболее изучена.
3.1.Регуляция
экспрессии генов у прокариот на уровне
инициации
транскрипции
Этот тип регуляции
осуществляется несколькими способами.
Из них наиболее значимы два.
1. Регуляция
транскрипции путём изменения вторичной
структуры участка ДНК, на котором
фермент РНК-полимераза осуществляет
синтез РНК. Пространственную структуру
ДНК изменяют специальные ферменты. Эти
изменения могут быть самыми разнообразными,
например возможен такой вариант, когда
на кодирующей части ДНК формируются
изгибы или шпильки. Эти структуры
блокируют движение по ДНК ферментов,
обеспечивающих самый первый процесс
синтеза РНК – инициацию. В результате
не происходит деспирализации ДНК, не
разрываются водородные связи между
нитями ДНК, не отходят друг от друга
нити ДНК, т.е. не формируется вилка
транскрипции. Процесс транскрипции не
начинается.
2. Регуляция путём
взаимодействия специальных
белков-регуляторов с оператором.
Этот механизм был
предложен Ф. Жакобом и Ж. Моно в 1961 г.
Предложенная ими гипотеза регуляции в
настоящее время полностью подтверждена
и хорошо исследована. Этот тип регуляции
называется «Контроль синтеза белка на
уровне транскрипции» или просто «Теория
оперона».
44
Как мы уже писали
ранее, оперон прокариот состоит из
промотора, оператора и кодирующей части.
К промотору присоединяется РНК-полимераза,
которая «проходит» через оператор и
транскрибирует РНК с матричной цепи
ДНК. Промотор и оператор взаимно
перекрываются. К оператору присоединяются
два
типа белков-
регуляторов – активатор и репрессор.
Это генетические факторы регуляции.
Репрессор,
взаимодействуя
с оператором, перекрывает его и частично
промотор, создавая стерическое препятствие
для присоединения РНК-полимеразы к
промотору (рис. 28, Б). Такая регуляция
носит название негативный контроль.
Активатор взаимодействует с оператором
таким образом, что эта связь, не только
не нарушает движение РНК-полимеразы
через оператор (рис. 28, А), но и ускоряет
осаждение на промотор всё новых и новых
молекул РНК-полимераз. Это повышает
интенсивность транскрипции гена, что
приводит к существенному увеличению
синтеза РНК и синтеза белка. Этот тип
регуляции называется позитивным
контролем.
Важно отметить,
что без активатора связывание
РНК-полимеразы с промотором так же
происходит, но очень медленно.
Вышеописанный
механизм интегрирован и в более высокие
уровни регуляции экспрессии генов. Его
легко понять, если помнить, что на более
высоком уровне регуляции происходят
те же процессы, что и изложенные выше,
но к ним добавляется звено, которое
регулирует действие активаторов и
репрессоров. Эндогенные или экзогенные
факторы (ими могут быть физические
факторы или химические соединения)
могут активировать или инактивировать
активатор или репрессор. Если происходит
активация активатора и инактивация
репрессора, то интенсивность транскрипции
повысится, и наоборот, при активации
репрессора и инактивации активатора
интенсивность транскрипции снизится.
3.2. Регуляция
экспрессии генов у эукариот
Существует несколько
механизмов регуляции экспрессии генов
у эукариот. Они контролируют практически
все этапы экспрессии генов. Как и в
предыдущем разделе (см. раздел 11.1.)
рассмотрим механизмы регуляции только
на уровне транскрипции.
Механизмы
регуляции транскрипции
К наиболее изученным
механизмам регуляции относятся следующие.
1. Регуляция
транскрипции через формирование
инициирующего комплекса (ТИК). Этот
комплекс формируется следующим образом:
факторы транскрипции взаимодействуют
с сигнальными последовательностями
ДНК промотора, создавая прочный
белково-нуклеотидный комплекс. К нему
присоединяется РНК-полимераза,состоящая
примерно из 10 полипептидов. Этот
многоэтапный процесс образования ТИК
контролируется белками-регуляторами,
которые, взаимодействуя с различными
составляющими комплекса, могут ускорить
образование ТИК или, наоборот, затормозить
его формирование.
45
2. Дистантное
влияние на формирование ТИК.
У эукариот, как
известно, имеется промотор, часто лежащий
рядом с геном, но отсутствует оператор.
Вместо него имеются регуляторные
области, находящиеся в ДНК или рядом с
промотором или на расстоянии (иногда
значительном) от него. Эти регуляторные
последовательности состоят из
относитель-






Активация
транскрипции



А
ДНК
Активатор

Репрессор


Торможение
транскрипции



ДНК
Б




— РНК-полимераза,
— активатор, — репрессор
Промотор
Оператор Ген




Рис.28. Влияние
белков регуляторов (активатора и
репрессора) на связывание РНК-полимеразы
с промотором и модификация транскрипции.
А – активатор
связался с оператором и активировал
связывание РНК-полимеразы с промотором.
Синтез РНК увеличился. Б – репрессор
связался с оператором и частично с
промотором, препятствуя соединению
РНК-полимеразы с промотором. Транскрипция
не происходит
но коротких
последовательностей ДНК, с которыми
связываются белки-регуляторы. Эти
белки-регуляторы и влияют на формирование
ТИК, которое происходит в области
промотора. Пока не выяснено каким образом
этот белок-регулятор может влиять на
формирование ТИК, находящийся на
достаточном удалении от белка-регулятора.
Предполагают, что это связано с тем, что
молекула ДНК в ядре делает петлю, в
результате чего два участка (участок с
белком-регулятором и участок, где
формируется ТИК) сближаются. Это позволяет
белку-регулятору влиять на образование
ТИК (см. рис. 29). Считают, что именно таким
образом действуют белки-регуляторы,
связанные с энхансерами и сайлен-
46
серами – участками
ДНК размером 10 – 20 пар нуклеотидов.
Энхансеры увеличивают скорость
транскрипции, сайленсеры –
замедляют.
3. Плейотропность
в регуляции генов эукариот. Среди
белков-регуляторов у эукариот существует
своеобразная иерархия. Один главный
белок-регулятор контролирует транскрипцию
нескольких генов-регуляторов. Последние,
в свою очередь, контролируют активность
структурных генов.
Энхансер
Сайленсер Белок-регулятор
сайленсера

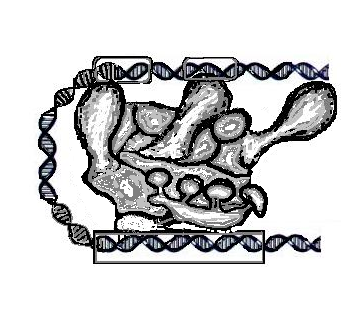
Белок-регулятор,
прикреплённый
к
энхансеру
П етля
етля
ДНК
Факторы



транскрипции


РНК-полимераза
Белок, связанный
с ДНК- промотором
Промотор
Рис.29. Петля ДНК.
Белки-регуляторы, осаждённые на энхансере
и сайленсере, взаимодействуют с факторами
инициации промотора
Механизмы
регуляции процессинга РНК у эукариот
Один из способов
регуляции экспрессии генов при созревании
мРНК – альтернативный сплайсинг. О нём
мы писали в разделе 7.5. Другой механизм
– редактирование ДНК, когда первичная
структура мРНК после транскрипции в
одних случаях сохраняется, а в других
изменяется в результате мутации. В
последнем случае про-иРНК может нести
другую функцию или вовсе её утратить.
Приведём пример.
Последовательности – УАА, УАГ и УГА
являются терминирующими кодонами. Они
располагаются в сайте терминации и
служат сигналом остановки РНК-полимеразы
и прекращения синтеза любой РНК. В
результате мутаций внутри гена может
происходить замена одного нуклеотида
на другой. Например, при дезаминировании
цитозин может превратиться в урацил.
В этом случае кодоны ЦАА, ЦАГ и ЦГА,
кодирующие аминокислоты (валин и аланин),
превратятся в бессмысленные кодоны
УАА, УАГ и УГА. Этот феномен превращения
смысловых кодонов в бессмысленные в
результате мутаций используется в живых
организмах в качестве регулирующего
механизма.
47
Так, у человека
имеется ген, кодирующий образование
липопротеинов, ответственных за обмен
жиров (в частности, транспортировку их
из кишечника в лимфу, а затем в кровь).
Этот ген имеется во всех клетках организма
человека, но функционирует он только в
дух органах – в печени и кишечнике. И в
печени и в кишечнике ген имеет одно и
тоже строение и один и тот же нуклеотидный
состав. В печени экспрессия гена
реализуется в полипептид апопротеин
В-100 (апо-В-100 или В-100), а в кишечнике
синтезируется апопротеин, содержащий
всего 48% аминокислот по сравнению с
В-100. Поэтому такой протеин назвали
апопротеин В-48 или просто В-48. Оказалось,
что в клетках кишечника, в середине
гена, кодирующего апопротеин, находился
(как и в клетках печени) триплет ЦАА, но
в результате дезаминирования цитозин
триплета превратился в урацил и триплет
приобрёл статус бессмысленного кодона
УАА. Понятно, что, подойдя к нему,
РНК-полимераза заканчивает транскрипцию
мРНК, в результате чего при трансляции
формируется не 100% белок В-100, а В-48. Однако
и белок В-100 и белок В-48 исправно несут
свои функции, хотя и отличающиеся друг
от друга.
Механизм регуляции
перехода мРНК из ядра в цитоплазму.
Для участия в
трансляции мРНК должна выйти из ядра
(места своего синтеза) через ядерные
поры в цитоплазму. Специальные ферменты
нуклеазы расщепляют мРНК при таком
переходе. Деградация приостанавливается,
если мРНК связана с белком. Понятно, что
в этом случае количественный выход мРНК
из ядра в цитоплазму зависит от двух
факторов: от количества ферментов,
расщепляющих иРНК, и количества белка,
способного связаться с мРНК. Синтез
нуклеаз и белка регулируется. Например,
если клетке необходимо синтезировать
большое количество гистонов (это бывает
в синтетическом периоде, когда идёт
интенсивный синтез ДНК и строительство
нуклеосом из гистонов), то усиливается
выработка белков, взаимодействующих с
гистоновой мРНК. Выход её в цитоплазму
увеличивается.
Существуют и
другие механизмы регуляции, о которых
мы только упомянем – регуляция
стабильности мРНК, регуляция скорости
трансляции, регуляция продолжительности
жизни молекул белка и др.
В заключении
необходимо отметить, что в изучении
регуляции экспрессии сейчас всё большее
значение придают химическим изменениям,
происходящим в определённых участках
генома. Наиболее известное из них –
метилирование, т.е. присоединение к
цитозину метильной группы (-СН3).
Такая модификация часто происходит в
ДНК рядом с геном и существенно сказывается
на его работе. Важным является то, что
метилирование не изменяет нуклеотидную
последовательность ДНК, т.е. это не
мутационная изменчивость. Не затрагивает
метилирование и информацию в гене. Это
не мутационная эпигенетическая
изменчивость. Сейчас изучение этой
изменчивости стало одним из важнейших
направлений в генетике – эпигеномикой
(от греческого «эпи» – рядом, около).
ХРАНЕНИЕ И РЕАЛИЗАЦИЯ
НАСЛЕДСТВЕННОЙ ИНФОРМАЦИИ
Редактор-корректор
Дудичева
Г.П.
Подписано в
печать……………..
Печать на ризографе.
Бумага офсетная.
Формат 60Х841/16.
Усл. печ. л. 2,79.
Тираж ……….. экз.
Заказ №…………
420012, Казань,
Бутлерова, 49, типография КГМУ
Репарация ошибочно спаренных нуклеотидов
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 19 февраля 2022 года; проверки требует 1 правка.
Репарация ошибочно спаренных нуклеотидов — система обнаружения и репарации вставок, пропусков и ошибочных спариваний нуклеотидов, возникающих в процессе репликации и рекомбинации ДНК, а также в результате некоторых типов повреждений ДНК[1][2].
Сам факт ошибочного спаривания не позволяет исправить ошибку, поскольку она может находиться на любой из двух составляющих ДНК ниток. Однако ошибки спаривания, как правило, локализуются только на одной (дочерней) нити ДНК, что позволяет избежать неоднозначности в интерпретации ошибки. В грам-положительных бактериях исходная нитка ДНК метилирована, а дочерняя нитка некоторое время остаётся неметилированной. Механизм распознавания исходной и дочерней ниток у других прокариот и эукариот в настоящее время неясен[3]. Предполагается, что у них дочерняя нить ДНК содержит разрезы, которые затем удаляются ДНК-лигазой.
Вероятность ошибки при репликации ДНК составляет 10–7—10–8. Система репарации ошибочно спаренных нуклеотидов снижает эту вероятность до 10–9[4].
Процесс репарации заключается в распознавании дефекта, определении исходной и дочерней нити ДНК, удалении ошибочно включённого нуклеотида и его замена правильным нуклеотидом. Удаляется обычно не только неправильный нуклеотид, но и часть нити ДНК вокруг него, после чего дочерняя нить восстанавливается, используя основную нить как матрицу[5].
Белки-репараторыПравить
Репарация ошибочно спаренных нуклеотидов — чрезвычайно консервативный процесс, практически без изменений унаследованный эукариотами от прокариот. Впервые этот тип репарации был обнаружен у S. pneumoniae (гены HexA и HexB). В дальнейшем исследования E. coli позволили обнаружить ряд генов, блокировка которых вызывает резкое повышение уровня мутаций. Белки, кодируемые этими генами, являются главными активными составляющими системы репарации и обозначаются префиксом «Mut»: MutS, MutH и MutL (MutS и MutL являются гомологами HexA и HexB соответственно).
MutS формирует димер (MutS2), который распознаёт неправильный нуклеотид на дочерней нити ДНК и связывается с дефектным участком ДНК. MutH связывается с полуметилированным участком ДНК, однако не совершает никаких действий, пока не будет активирован димером MutL (MutL2), который служит медиатором между MutS2 и MutH, активируя последний. Спираль ДНК расплетается в поисках ближайшей к дефекту метилированной группы GATC, которая может находиться на расстоянии 1000 нуклеотидов и более. MutH разрезает дочернюю нитку ДНК вблизи метилированной группы и активирует одну из хеликаз UvrABC, которая отделяет дочернюю нить от основной и отрезает её в районе дефекта, включая сам дефект и ближайшие к нему нуклеотиды. Используемая эндонуклеаза зависит от того, по какую сторону (3′ или 5′) от дефекта MutH разрезает нитку ДНК. Если разрез сделан на стороне 5′, используется RecJ или ExoVII, если на стороне 3′, то ExoI. Образовавшийся однониточный участок заполняется ДНК-полимеразой III, которая использует основную нитку в качестве образца, а затем разорванная нитка ДНК сшивается ДНК-лигазой и метилируется метилазой[5].
Гомологи MutSПравить
Связываясь с ДНК, MutS2 деформирует спираль и покрывает около 20 нуклеотидных пар. Он обладает слабыми аденозинтрифосфатазными свойствами и связывая АТФ формирует третичную структуру молекулы. Рентгеноструктурный анализ показывает, что структура молекулы MutS исключительно асимметричная, и хотя активной конфигурацией является димер, только один из мономеров взаимодействует с дефектным участком ДНК.
У эукариот в качестве гомологов MutS обнаружены два гетеродимера: Msh2/Msh6 (MutSα) и Msh2/Msh3 (MutSβ). MutSα используется для репарации нуклеотидных замен и небольших петель, возникших в результате вставки или делеции нуклеотидных цепочек. MutSβ удаляет только длинные петли (10 и более нуклеотидов)[6].
Гомологи MutLПравить
MutL также обладает слабыми аденозинтрифосфатазными свойствами (использует АТФ для движения вдоль нитки ДНК). Он образует с MutS и MutH комплекс, расширяя участок взаимодействия MutS с ДНК.
ПримечанияПравить
- ↑ Iyer R., Pluciennik A., Burdett V., Modrich P. DNA mismatch repair: functions and mechanisms (англ.) // Chem Rev (англ.) (рус. : journal. — 2006. — Vol. 106, no. 2. — P. 302—323. — doi:10.1021/cr0404794. — PMID 16464007.
- ↑ Larrea A. A., Lujan S. A., Kunkel T. A. DNA mismatch repair (англ.) // Cell. — Cell Press, 2010. — Vol. 141, no. 4. — P. 730. — doi:10.1016/j.cell.2010.05.002. — PMID 20478261.
- ↑ Modrich Paul. Strand-specific Mismatch Repair in Mammalian Cells (англ.) // Journal of Biological Chemistry. — 1997. — 3 October (vol. 272, no. 40). — P. 24727—24730. — ISSN 0021-9258. — doi:10.1074/jbc.272.40.24727. — PMID 9312062. [исправить]
- ↑
James A. Shapiro Evolution: A View from the 21st Century . FT Press Science, 2011, 254 р., ISBN 978-0-13-278093-3. - ↑ 1 2 Cline Susan D., Hanawalt Philip C. Who’s on first in the cellular response to DNA damage? (англ.) // Nature Reviews Molecular Cell Biology. — 2003. — May (vol. 4, no. 5). — P. 361—373. — ISSN 1471-0072. — doi:10.1038/nrm1101. — PMID 12728270. [исправить]
- ↑ MARRA Giancarlo, SCHÄR Primo. Recognition of DNA alterations by the mismatch repair system (англ.) // Biochemical Journal. — 1999. — 15 February (vol. 338, no. 1). — P. 1. — ISSN 0264-6021. — doi:10.1042/0264-6021:3380001. — PMID 9931291. [исправить]
См. такжеПравить
- en:Base excision repair
- Эксцизионная репарация нуклеотидов
СсылкиПравить
- Sung-Hoon Jun, Tae Gyun Kim, Changill Ban DNA mismatch repair system. Classical and fresh roles. FEBS Journal 273 (2006) 1609–1619, doi:10.1111/j.1742-4658.2006.05190.x.
- DNA Repair Архивная копия от 12 февраля 2018 на Wayback Machine
- MeSH DNA+Mismatch+Repair
- Hsieh P., Yamane K. DNA mismatch repair: Molecular mechanism, cancer, and ageing (англ.) // Mech Ageing Dev : journal. — 2008. — Vol. 129, no. 7—8. — P. 391—407. — doi:10.1016/j.mad.2008.02.012. — PMID 18406444. — PMC 2574955.
- Iyer R., Pluciennik A., Burdett V., Modrich P. DNA mismatch repair: functions and mechanisms (англ.) // Chem Rev (англ.) (рус. : journal. — 2006. — Vol. 106, no. 2. — P. 302—323. — doi:10.1021/cr0404794. — PMID 16464007.
- Joseph N., Duppatla V., Rao D. N. Prokaryotic DNA mismatch repair (неопр.) // Prog. Nucleic Acid Res. Mol. Biol.. — 2006. — Т. 81. — С. 1—49. — doi:10.1016/S0079-6603(06)81001-9. — PMID 16891168.
- Yang W. Structure and function of mismatch repair proteins (неопр.) // Mutation Research (англ.) (рус.. — Elsevier, 2000. — Т. 460, № 3—4. — С. 245—256. — PMID 10946232.
- Griffith, Wessler, Lewontin, Gelbart, Suzuki, Miller, Introduction to Genetic Analysis, 8th Edition, W.H. Freeman and Company, ISBN 0-7167-4939-4
- Thomas A.Kunkel and Dorothy A. Erie,(2005), DNA Mismatch Repair, Annu Rev.Biochem,74:681-710
- Errol C.Friedberg, Graham C. Walker, Wolfram Siede, Richard D. Wood, Roger A. Schultz, Tom Ellenberger, DNA repair and Mutagenesis, 2nd edition, ASM press, ISBN 1-55581-319-4
- Репарация ошибочно спаренных нуклеотидов (mismatch repair) на сайте «Биология человека».
- MutL белок на сайте «Биология человека».
- Глазер В.М. Конверсия гена на сайте «Научная сеть».
- Репарация на сайте «Химическая энциклопедия».
- Hsieh, P. Molecular mechanisms of DNA mismatch repair. Mutat. Res. 486, 71–87 (2001).
Исправление ошибок. ДНК-полимеразы могут выявлять и исправлять ошибки, тогда как РНК-полимеразы такой способностью, по-видимому, не обладают. Поскольку ошибка даже в одном основании как при репликации, так и при транскрипции может привести к ошибке в синтезе белка, можете ли вы дать биологическое объяснение этому поразительному различию [c.925]
З-Ю п. н. Оказывается, у всех организмов точность работы репликативной машины (включающей не только ДНК-полимеразы, но и другие белки см. ниже) как раз такова, чтобы обеспечить безошибочное воспроизведение всего генома или допустить лишь малое число ошибок. Так, у бактерий ошибки синтеза ДНК происходят не чаще чем один раз на много миллионов нуклеотидов. Молекулярные взаимодействия, на которых основаны ферментативные реакции, в частности синтез ДНК, не могут быть абсолютно надежными, кроме того, точность процесса связана с его скоростью. Для того чтобы обеспечить высокую точность наряду с высокой скоростью репликации, природе пришлось прибегнуть к специальным механизмам, один из которых — механизм коррекции. [c.47]
Смещение в комплементарности пар, или ошибка репликации может происходить по другой схеме [c.219]
Нормальное размножение клеток требует высокой точности копирования ДНК-матрицы. Генетический материал живых организмов имеет огромные размеры. Даже у бактерий ДНК-полимераза должна практически безошибочно скопировать молекулу ДНК длиной около 3-10 п. н. Оказывается, у всех организмов точность работы репликативной машины (включаюш.ей не только ДНК-полимеразы, но и другие белки см. ниже) как раз такова, чтобы обеспечить безошибочное воспроизведение всего генома или допустить лишь малое число ошибок. Так, у бактерий ошибки синтеза ДНК происходят не чаще чем один раз на много миллионов нуклеотидов. Молекулярные взаимодействия, на которых основаны ферментативные реакции, в частности синтез ДНК, не могут быть абсолютно надежными, кроме того, точность процесса связана с его скоростью. Для того чтобы обеспечить высокую точность наряду с высокой скоростью репликации, природе пришлось прибегнуть к специальным механизмам, один из которых — механизм коррекции. [c.47]
Очень важно отметить, что процесс репликации протекает со значительно более высокой степенью точности, чем процессы транскрипции и трансляции. Частые ошибки в репликации подвергли бы большому риску сохранность видов [c.908]
ДНК-полимеразы проверяют комплементарность каждого нуклеотида матрице дважды один раз перед включением его в состав растущей цепи и второй раз перед тем, как включить следующий нуклеотид. Очередная фосфодиэфирная связь образуется лишь в том случае, если последний (З -концевой) нуклеотид затравки комплементарен матрице. Если же на предыдущей стадии полимеризации произошла ошибка (например, из-за того, что нуклеотид в момент полимеризации находился в необычной таутомерной форме), то репликация останавливается до тех пор, пока неправильный нуклеотид не будет удален. Некоторые ДНК-полимеразы обладают не только полимеризующей, но и 3 -экзонуклеазной активностью, «Которая отщепляет не спаренный с матрицей нуклеотид затравки. После чего полимеризация восстанавливается, от механизм, коррекция, заметно увеличивает точность работы ДНК-полимераз. Мутации, нарушающие З -экзонуклеазную активность ДНК-полимеразы, существенно повышают частоту возникновения прочих мутаций. Напротив, мутации, приводящие к усилению экзонуклеазной актив- ности относительно полимеризующей, снижают темп мутирования Генетического материала. [c.47]
Спонтанные генные мутации определяются ошибками при репликации ДНК, возникающими вследствие теплового движе-иия атомов и молекул. Очевидно, что ошибки транскрипции и трансляции не наследуются. [c.283]
Процесс транскрипции находится в клетке под строгим контролем, поэтому имеет место как неодинаковое транскрибирование во времени разных участков ДНК (генов), так и неодинаковая скорость, с которой гены могут транскрибироваться. В результате количество молекул иРНК в клетке, комплементарных разным генам, сильно различается. Хотя в целом механизмы синтеза ДНК и РНК сходны, процесс транскрипции не обладает той степенью точности, которая характерна для репликации ДНК. Однако поскольку иРНК не способна к самовоспроизведению, возникающие при ее синтезе ошибки в последующих клеточных генерациях не воспроизводятся и, следовательно, не могут наследоваться. [c.142]
Если ошибка синтеза не устраняется системами репарации, то неизбежна деформация дуплекса и искажение генетической программы. Такие сохраняющиеся при репликации изменения ДНК носят название мутации. Они могут быть спонтанными и индуцированными. Частота спонтанных мутаций невелика и составляет всего 10 —10 на клетку. В основном имеют место мутации, обусловленные действием внешних факторов физических (радиация), биологических (вирусы) и чужеродных химических веществ на генетический аппарат клеток. Наиболее многочисленными и опасными являются мутагены окружающей среды. Загрязнение воды и воздуха различными химическими отходами промышленных предприятий, химическими средствами защиты растений отрицательно сказывается на генетической программе всех живых организмов. В последние годы установлено, что ряд пищевых красителей, стабилизаторов и вкусовых добавок обладает выраженной мутагенной активностью, что привело к значительному ужесточению требований, связанных с применением химических веществ в пищевой промышленности. Многие лекарственные вещества также воздействуют на генетический аппарат клеток и должны подвергаться специальным генетическим испытаниям. [c.455]
Химическое изменение оснований. Некоторые мутагенные вещества действуют путем химического изменения содержащихся в ДНК оснований, что приводит к ошибкам репликации. Вполне понятное изменение вызывает нитрит. Азотистая кислота дезаминирует аденин, гуанин или цитозин без разрыва или каких-либо других изменений полинуклеотидной цепи. В результате замещения аминогруппы гидроксильной группой аденин превращается в гипоксантин и спаривается с цитозином вместо тимина, что приводит к мутации АТ СС. Если цитозин дезаминируется в урацил, то он спаривается с аденином вместо гуанина, и это ведет к мутации СС -АТ. Будучи превращен в ксантин, гуанин по-прежнему спаривается с цитозином, т. е. дезаминирование С не вызывает мутации. Гидроксиламин вступает в реакцию главным образом с цитозином и изменяет его так, что тот спаривается с аденином значит, он тоже вызывает мутации СС ТА. [c.444]
Из уровня спонтанных мутаций у бактерий в расчете на одно поколение рассчитано, что вероятность одной репликационной ошибки при синтезе ДНК составляет порядка 10 . Эту величину можно рассматривать как отношение скоростей реакций правильной репликации [c.194]
ВЫВОД, ЧТО, по-видимому, код действительно является триплет-ным, причем кодирование начинается от определенной точки нуклеиновой кислоты. При этом большая часть трехбуквенных комбинаций соответствует определенным аминокислотам и лишь небольшая часть триплетов относится к бессмысленным. Число триплетов равно 4-4-4 = 64, т. е. значительно больше числа аминокислот. Некоторые из них, по-видимому, кодируют одну и ту же аминокислоту, т. е. код является вырожденным. Этот вывод согласуется с обнаружением в настоящее время двух и более типов растворимых РНК, специфичных к одной и той же аминокислоте. Вырожденность генетического кода может способствовать выживанию организма. Действительно, в случае невырожденного кода ошибка при репликации ДНК или при транскрипции должна скорее приводить к появлению бессмысленного триплета, чем в случае вырожденного кода. Следовательно, при невырожденном коде ошибки чаще вызывали бы прекращение синтеза соответствующего белка или образование незаконченных белковых цепей. Напротив, в случае вырожденного кода ошибки должны чаще приводить просто к замене одной аминокислоты на другую, что, как правило, не имеет серьезных последствий. [c.376]
Как в прокариотических, так и в эукариотических клетках содержатся ферментные системы, способные исправлять ошибки репликации и различные формы повреждения ДНК, вызываемые гидро- [c.990]
Г. Е. Фрадкин. После обработки фаговой популяции гидроксиламино.м последний при помощи диализа удалялся из вирусной суспензии. Следовательно, во время облучения гидроксиламин в среде отсутствовал. Предварительная модификация цитозиновых остатков в ДНК фага лямбда, вызываемая гидроксиламином (предположительно образование 4—5-дигидро-4-гидро-ксиламиноцитозина), действительно повышает радиочувствительность фаговой популяции в условиях преобладания непрямого эффекта излучения. Мы полагаем, что механизм повышения радиочувствительности сводится к нарушению специфического процесса комплементарного спаривания азотистых оснований во время репликации фаговой ДНК внутри клетки. В последних рабо тах Брауна, Филипса с соавторами химическими методами установлено, что цитозин, предварительно обработанный гидроксиламином, спаривается не с гуанином, а с аденином. Вследствие этого во вновь образованной ДНК происходят единичные замены гуанина на аденин. До тех пор, пока эти замены не выходят за пределы связанных серий однозначных кодонов, они не сказываются на информационных свойствах ДНК фага. Однако эти единичные замены понижают эффективность механизма, исправляющего ошибки включения, за счет уменьшения резерва однозначны кодонов или, иными словами, за счет уменьшения степени вырожденности структурного кода. Мы не видим большой сложности в этом объяснении, к которому мы сознательно прибегли для освещения возмол<ных молекулярных механизмов, лежащих в основе скрытых повреждений, связанных с тонкими сдвигами в величинах водородных сил в химически модифицированных азотистых основаниях. Как известно, сенсибилизация может обусловливаться уменьшением степени прочности первичной структуры ДНК вследствие лабилизации эфирно-фосфатных связей. Однако при использовании в качестве модифицирующего агента гидроксиламина этот второй механизм отсутствует, так как химическими исслг- [c.173]
Включение или утрата отдельных пар оснований. Профлавин и другие акридиновые красители действуют по-иному. Вероятно, молекула акридина внедряется между соседними основаниями цепи ДНК и увеличивает расстояние между ними (интеркаляция). Такое пространственное изменение при репликации ДНК может вызывать ошибки двух типов- [c.444]
НО редко, он может образовать пару не с аденином, а с гуанином. Это в свою очередь приведет к ошибке при включении или при репликации, заключающейся в замене пары А — Т на Г — Ц и наоборот. [c.218]
В 1959 г. Д. Пратт сумел показать, что большинство, если не все бромурациловые ревертанты г+, образуемые мутантами гП (которые были индуцированы аналогами оснований), возникают в виде гетерозигот гП/г» , которые позднее расщепляются на гомозиготные ревертанты г» «. Чтобы продемонстрировать это, к бактериям, зараженным мутантным фагом Т4гП, непосредственно перед окончанием скрытого периода внутриклеточного развития фага добавляли бромурацил и первые инфекционные частицы, появившиеся в клетках непосредственно после окончания скрытого периода, высвобождали путем искусственного лизиса клеток. Такая методика постановки опыта гарантировала, что все ревертанты / +, возникшие и извлеченные из фонда предшественников фаговой ДНК во время короткого воздействия мутагена, образовались исключительно в самом последнем цикле репликации. Ошибка копирования, восстановившая у них в соответствующем участке ДНК генетическую информацию дикого типа г+, произошла настолько поздно, что больше и и одного цикла репликации произойти уже не могло (а это значит, что не могло произойти и расщепления на гомозиготные мутантные структуры). Такого рода опыты показали, что свыше 80% всех ревертантов г, возникших в результате кратковременного контакта с бромурацилом, действительно представляет собой мутационные гетерозиготы, несущие как исходный аллель г, так и ревертировавщий к дикому типу аллель г» . Следовательно, в полном соответствии с механизмом Уотсона и Крика и вопреки механизмам, предусматривающим консервативное распределе- [c.325]
Нетрудно видеть, что в тонком механизме репликации и синтеза белков произвол в расположении частиц сведен к минимуму. Этот матричный процесс является низкоэнтропийным. Ошибки в размещении аминокислот в пептидных цепочках составляют по приблизительной оценке 1 на 10 . В то же время, если бы синтез белков происходил на примитивной матрице, на которой концентрация тех или иных компонентов и их относительное расположение в значительной мере определялись бы случайностями окружающей обстановки, нельзя было бы ожидать воспроизводимости синтеза того или иного белка и, в частности, того белка, от структуры ко- [c.393]
Репликаза фага Q способна in vitro синтезировать цепи, полностью комплементарные как плюс-, так и минус-молекулам вирусной РНК. Система, однако, специфична для вирусной РНК и не может копировать никаких других полинуклеотидов. Возможно, что для инициации процесса репликации нужно, чтобы на З -конце имелись определенные последовательности. В пробирке репликация протекает с ошибками, такими, в частности, как преждевременная терминация цепи и неправильное спаривание оснований. В результате происходит образование мутантных форм РНК, что дает возможность получать молекулы РНК, размеры которой будут значительно меньше, чем у вирусной РНК, и которые будут при этом легко реплицироваться репликазной системой фага Q . Была установлена нуклеотидная последовательность одного из таких фрагментов, включающего всего лишь 114 нуклеотидов . [c.245]
Разные аллели одного и того же Г. возникают благодаря мутациям-илслецуемьш изменениям в структуре исходного Г. В норме Г. чрезвычайно стабилен и при удвоении хромосом во время репликации ДНК воспроизводится совершенно точно вероятность ошибки не превышает 10″ . Мутации происходят редко и обычно влекут за собой неблагоприятные последствия для организма, т. к. нарушается его способность синтезировать нормальный белок. Однако в целом это явление играет положит, роль накопление редких полезных мутаций создает основу генетич. изменчивости, необходимой для эволюции. [c.517]
Особый класс М. составляют соед., представляющие собой аналоги оснований ДНК-5-галогенурацилы, 2-амино-и 6-метиламинопурины н др. Галогенурацилы включаются в ДНК при матричном синтезе вместо тимина, 2-амино-пурин-вместо аденина. Вследствие различий в положении кетоенольного равновесия у тимина и галогенурацилов (при включении последних в ДНК) увеличивается частота ошибочных спариваний оснований и возникают ошибки при репликации. [c.152]
Равновесие между созидательными возможностями выбора среди специфических оснований в ДНК (созидательные мутации) и точностью синтеза белков (поддерживающих жизнь организма) является основой эволюции. Ферменты, которые заряжают тРНК специфической аминокислотой, обладают очень низкой вероятностью ошибки, порядка 1 Ю» для гомологичных аминокислот. При репликации точность даже выше, и величина ошибки редко превышает 1 на 10. [c.212]
К настоящему времени у эукариот, как и у бактерий (см. ранее), открыто несколько ДНК-полимераз. В репликации ДНК эукариот участвуют два главных типа полимераз — а и б. Показано, что ДНК-полимераза а состоит из 4 субъединиц и является идентичной по структуре и свойствам во всех клетках млекопитающих, причем одна из субъединиц оказалась наделенной праймазной активностью. Самая крупная субъединица ДНК-полимеразы а (мол. масса 180000) катализирует реакцию полимеризации, преимущественно синтез отстающей цепи ДНК, являясь составной частью праймасомы. ДНК-полимераза б состоит из 2 субъединиц и преимущественно катализирует синтез ведущей цепи ДНК (см. далее). Открыта также ДНК-полимераза г, которая в ряде случаев заменяет б-фермент, в частности при репарации ДНК (исправление нарушений ДНК, вызванных ошибками репликации или повреждающими агентами). Следует отметить, что в эукариотических клетках открыты два белковых фактора репликации, обозначаемых RFA и RF . Фактор репликации А выполняет функцию белка—связывание одноцепочечной ДНК (наподобие белковых факторов связывания разъединенных цепей ДНК при [c.480]
Этап HI — терминация синтеза ДНК —наступает, скорее всего, когда исчерпана ДПК-матрица и трансферазные реакции прекращаются. Точность репликации ДНК чрезвычайно высока, возможна одна ошибка на 10 трансферазных реакций, однако подобная ошибка обычно легко исправляется за счет процессов репарации. [c.486]
Такие системы, достигшие определенного уровня сложности, наталкиваются на границу генетически переносимого количества информации. Оно составляет около 10 бит. Оптимальное значение ошибки при репликации нуклеиновой кислоты — 10 . Это — системно-обусловленная граница. Ее преодоление было достигнуто в нрироде созданием пола и геыегической рекомоина- [c.549]
Приближенная модель репликации ДНКизображена на рис. 2.11. Из приведенной схемы видно, что репликация точно воспроизводит прежнюю (исходную) структуру ДНК. Но если произошла ошибка в процессе копирования (мутация), то она будет с предельной точностью копироваться при последующих репликациях изменившейся ДНК. Показано, что участки ДНК, содержащие скопления нуклеотидов, обладают повышенной склонностью к спонтанным мутациям [22]. [c.94]
По происхождению мутации делятся на спонтанные (неконтролируемые) и индуцированные (контролируемые). Первые возникают в результате неконтролируемого влияния каких-то естественных факторов (радиация, температура и т. д.). Направленное использование мутагенов приводит к возникновению индуцированных мутаций. Многими экспериментами четко показано, что мутации возникают независимо от условий среды обитания, т. е. не направленно. Мутации возникают в основном как ошибки репликации ДНК. Выделяют следующие типы мутаций перестройка хромосом, перестройка генома клетки грибов и водорослей (полиплоидия, гаплоидия, гетероплоидия), внутригенные изменения (прямые мутации, реверсии, обратные мутации). [c.102]
Ошибка в одном основании при репликации ДНК, если она не исправлена, приведет к тому, что одна из двух дочерних клеток, а также все ее потомки будут содержать измененную хромосому. Ошибка в одном основании, совершенная РНК-полимеразой, повлечет за собой синтез некоторого количества неправильных копий одного белка. При этом, поскольку пул мРНК в клетке быстро обновляется, большинство молекул этого белка будет нормальным. Потомство такой клетки тоже будет нормальным. [c.1004]
Анализ приведенных выше результатов дает возможность написать для преобладающих таутомерных форм оснований нуклеиновых кислот формулы, изображенные на фиг. 55. Минорные таутомерные формы, возможно, играют существенную роль в возникновении спонтанных мутаций, поскольку спаривание несоответствующих оснований (см. гл. ХУП1) должно привести к ошибке при включении оснований и при последующей репликации цепи. Можно показать, что если скорость включения основания в цепь нуклеиновой кислоты меньше скорости перехода минорного таутомера в доминирующую форму, то скорость спонтанных мутаций, обусловленных данным основанием, приблизительно равна константе равновесия между минорным и доминирующим таутомерами. К сожалению, для азо- [c.308]
Если ДНК представляет собой генетический материал, то возникает весьма важный вопрос каким образом ДНК реплицируется столь точно, что при передаче генетических признаков очень редко возникают ошибки Так как количество ДНК, приходящееся на гаплоидный набор хромосом, есть величина постоянная, делящаяся клетка должна синтезировать ДНК- Для того чтобы наследственная информация, содерлсащаяс в ДНК, была передана без ошибок, вновь синтезированная ДНК должна представлять собой точную копию исходной. На фиг. 61 изображены схемы двух предполагаемых типов репликации ДНК консервативного и полуконсервативного. [c.327]
Задание 189. Напишите программу для моделирования самоорганизации ДНК в качестве примера самоорганизуюшихся систем. Используйте для этого следующую простую модель. Пусть имеется 100 молекул ДНК, состоящих из 12 нуклеотидов четырех видов (их обозначим буквами А, Т, С и G). Последовательность нуклеотидов в этих 100 молекулах ДНК случайная. Назовем одну из последовательностей идеальной она имеет некоторые преимущества перед остальными. Из 100 молекул ДНК в результате репликации получается еще 100 молекул. Однако при репликации встречаются ошибки (мутации), например в количестве 1%. Теперь из 200 молекул 100 погибает. При этом имеет значение преимущество, которым обладают молекулы с последовательностью нуклеотидов, похожей на идеальную . (Например, при каждом совпадении нуклеотида и его положения в цепи с идеальной последовательностью вероятность гибели уменьшается в два раза.) Процессы репликации и гибели протекают очень быстро. В конце концов все молекулы ДНК должны получить идеальную последовательность нуклеотидов, хотя вероятность ее образования в результате случайного процесса составляет 1 16777216. Что будет, если мутации будут возникать чаще или реже [c.330]
Нетрудно видеть, что в тонком механизме репликации и синтеза белков произвол в расположении частиц сведен к минимуму. Этот матричный процесс является низкоэнтропийным. Ошибки в размещении аминокислот в пептидных цепочках составляют по приблизительной оценке 1 на 10 . В то же время, если бы синтез белков происходил на примитивной матрице, на которой концентрация тех или иных компонентов и их относительное расположение в значительной мере определялись бы случайностями окружающей обстановки, нельзя было бы ожидать воспроизводимости синтеза того или иного белка и, в частности, того белка, от структуры которого зависят жизненно важные свойства системы. Здесь кодирование матричного синтеза обусловлено целым рядом низших кодов кодом, отвечающим соответствию т-РНК и аминокислоты кодом, соответствующим отношению между т-РНК, рибосомой и м-РНК кодом ферментов, производящих замыкание пептидных связей, и т. д. Это — кодированный перенос массы, обусловливающий возникновение структуры, обладающей исключительными свойствами их исключительность состоит в том, что они необходимы для стабилизации синтеза этой же структуры на уровне всех не только низших, но и многих высших кодов, которые возникнут, когда белки сложатся в клетки, клетки в органы, а органы в организм. [c.205]
