Индикаторные погрешности титрования
При титровании возможны случайные и
систематические погрешности. Случайные
погрешности связаны с измерением объема
и массы навески, но и значительную часть
погрешности титрования составляют
систематические погрешности, в частности,
индикаторная.
Случайные погрешности обрабатываются
по законам математической статистики.
Индикаторные погрешности связаны с
тем, что pT индикатора не
совпадает со значением pH
в ТЭ. Конечная точка титрования с данным
индикатором не совпадает с ТЭ.
При недотитровывании:
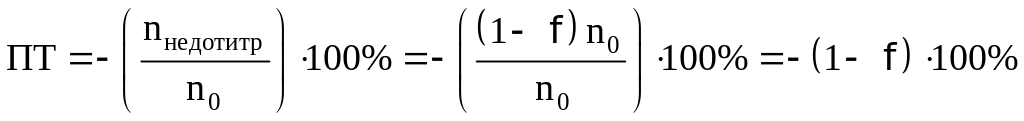
При перетитровывании:
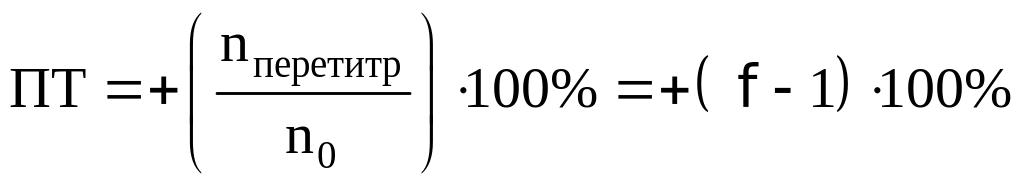
Возьмем индикаторы хризоидин (pT=5,50)
и хлорфеноловый красный (pT
= 5,80). В данном случае в КТТ pH
будет больше, чем pH в ТЭ
(pH = 5,28), а, следовательно,
в растворе будет неотитрованное
основание. Эта погрешность, обусловленная
содержанием неоттитрованного основания,
называется щелочной, будет определяться
уравнением
![]()
.
На данном этапе титрования pH
будет определяться по формуле
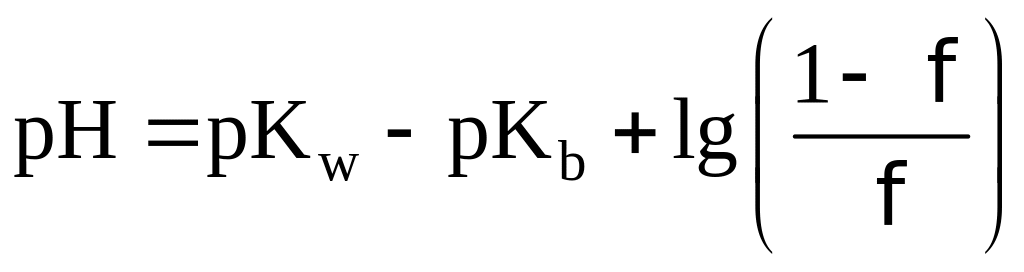
.
В КТТ pH раствора равен
pT. Следовательно, можно
найти и f
в КТТ:
![]()
.
Отсюда,

.
Посчитаем ПТ для данных индикаторов:
хризоидин:
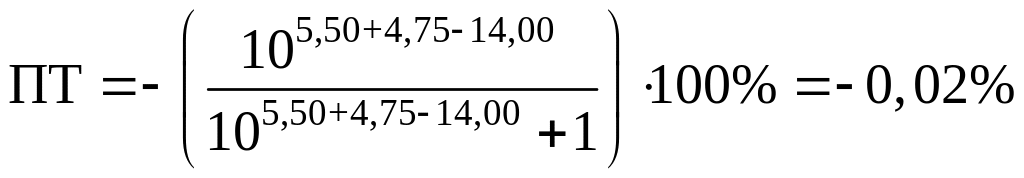
хлорфеноловый красный:
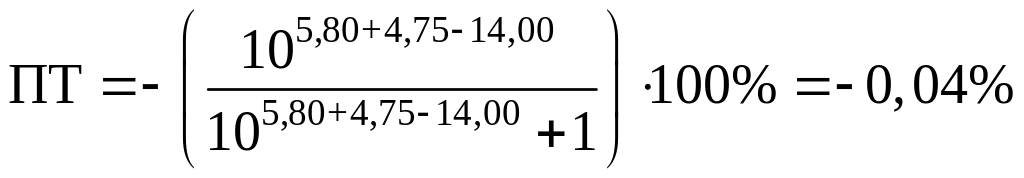
Оба эти индикатора подойдут для нашего
титрования. Рассмотрим ПТ для индикатора
розоловая кислота (pT=7,1).
По данной формуле получается ПТ=–0,70%,
что превышает обычно задаваемое значение
погрешности (±0,2%).
Рассмотрим же теперь случай, когда мы
используем индикаторы с pT
меньшим, чем pH в ТЭ. В КТТ
раствор будет перетитрован, и pH
будет определяться концентрацией
сильной кислоты (водородная погрешность),
и в нашей задаче определяться уравнением
.
Погрешность будет определяться по
формуле
![]()
Возьмем для примера индикаторы лакмоид
(pT=5,20), ализариновый красный
C (pT=4,45) и
бромфеноловый синий (pT=3,80).
pH раствора в КТТ равен
pT:
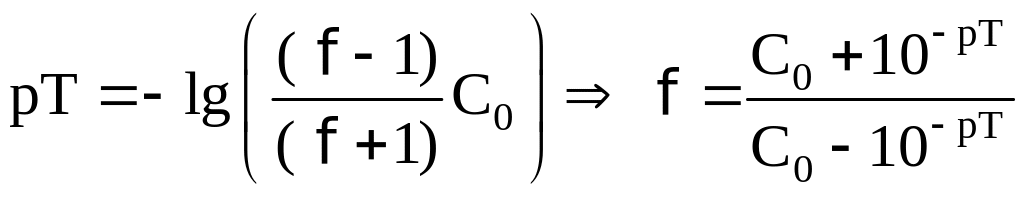
.
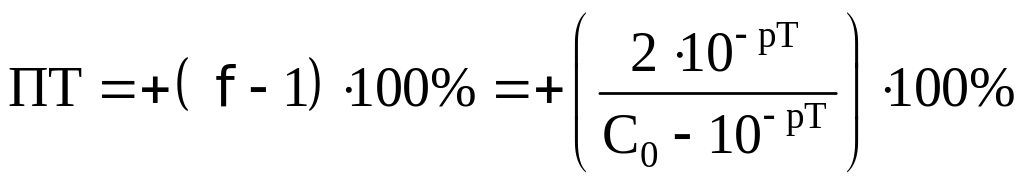
.
Рассчитаем ПТ для наших индикаторов:
Лакмоид:

Ализариновый красный C:
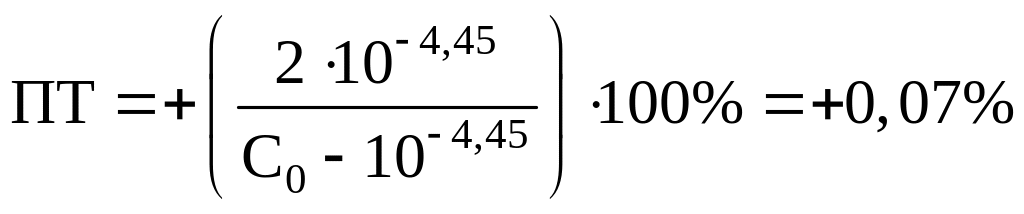
Бромфеноловый синий:

Вполне очевидно, что из двух предложенных
индикаторов наиболее подходящим является
ализариновый красный C.
Учитывая все расчеты, приходим к выводу,
что самыми подходящими для нашего опыта
индикаторами являются хризоидин (с
интервалом перехода 4,0 – 7,0, оранжевая
– желтая) и лакмоид (4,0 – 6,4, красная –
синяя).
Выводы
По кривой титрования аммиака можно
сделать ряд выводов.
В ходе титрования заметно плавное
уменьшение pH и заметен
скачок в области точки эквивалентности.
Скачок титрования полностью находится
в кислой области.
Точка эквивалентности расположена при
pH 5,28 и, очевидно, не
совпадает с точкой нейтральности. Скачок
титрования 0,1 М аммиака в пределах ±0,1%
от точки эквивалентности находится в
пределах pH от 6,25 до 4,30 и
составляет примерно 2 единицы pH,
что намного меньше скачка сильной щелочи
(6 единиц pH). С уменьшением
концентрации и увеличением температуры
скачок уменьшается.
В нашем случае одними из самых подходящих
являются лакмоид и хризоидин.
Окислительно-восстановительное титрование
Метод основан на реакциях
окисления-восстановления. Их называют
по применяемому тированному раствору
реагента, например: перманганатометрия,
йодометрия, бихроматометрия. В этих
методах в качестве титрантов применяют,
соответственно, KMnO4,
I2, K2Cr2O7.
В основе метода лежит изменение
окислительно-восстановительного
потенциала, обусловленного протеканием
окислительно-восстановительной реакции
между титрантом и определяемым веществом.
![]()
В процессе титрования происходит
изменение концентраций окисленной и
восстановленной форм, а, следовательно,
изменяется окислительно-восстановительный
потенциал титруемого раствора, включающей
две редоксопары.
В соответствии с уравнением Нернста
окислительно-восстановительный потенциал
для любой редоксопары:
![]()
Для каждого отдельного метода
окислительно-восстановительного
титрования используются свои стандартные
растворы.
Рассмотрим наш случай – перманганатометрия.
Рабочим раствором этого метода является
раствор перманганата калия KMnO4,
он неустойчив из-за реакции с водой,
катализируемый диоксидом марганца и
на свету:
![]()
Поэтому растворы перманганата калия
следует готовить, используя чистую воду
(органические примеси в воде могут
реагировать с
![]()
и давать MnO2, ускоряющий
разложение реагента), отфильтровать от
диоксида марганца и хранить в темных
склянках; раствор следует выдержать
несколько недель для окончания протекания
всех процессов. Очевидно, что раствор
следует стандартизировать, для чего
используют оксалат натрия и другие
восстановители. Реакция
![]()
катализируется ионами Mn2+.
Первые капли перманганата даже в горячем
растворе обесцвечиваются очень медленно.
В ходе титрования концентрация ионов
Mn2+ возрастает и
скорость реакции увеличивается: реакция
автокаталитическая.
Титр перманганата калия можно установить
также по оксиду мышьяка(III)
или металлическому железу.
В перманганатометрии применяют также
растворы восстановителей – слои Fe(II),
щавелевую кислоту и некоторые другие
– для определения окислителей методом
обратного титрования. Соединения Fe(II)
на воздухе медленно окисляются, особенно
в нейтральном растворе. Подкисление
замедляет процесс окисления, однако
обычно рекомендуется перед применением
раствора Fe(II)
в анализе проверить его титр. Оксалаты
и щавелевая кислота в растворе медленно
разлагаются. Этот процесс ускоряется
на свету, поэтому растворы оксалатов
рекомендуется хранить в темных склянках.
Подкисленные растворы оксалатов более
устойчивы, чем нейтральные или щелочные.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Чтобы окраска окислительно-восстановительного индикатора изменялась при титровании резко и индикаторная ошибка титрования была незначительной, интервал перехода индикатора должен находиться в пределах скачка потенциалов на кривой титрования. [c.369]
И. М. Кольтгоф, В. А. Стенгер. Объемный анализ. Госхимиздат, 1950, (т. I. 376 стр.) и 1952, (т. И, 444 стр.). В т. I рассматриваются теоретические основы объемного анализа. Изложена теория методов нейтрализации и соединения ионов, приведены кривые титрования для различных случаев метода нейтрализации. Отдельные главы содержат материал ио теории методов окисления-восстановления, теории индикаторов, по ошибкам титрования. Рассмотрены явления адсорбции и соосаждения, катализа и индукции, применение объемных методов в органическом анализе описаны теоретические положения, касающиеся применения физико-химических методов для определения точки эквивалентности. В т. 11 книги изложено практическое применение методов нейтрализации, осаждения и комплексообразования. В томе 111 (840 стр., 1961 г.) описано применение окислительно-восстановительных методов объемного анализа. [c.486]
Инцикаторы в окислительно-восстановительном титровании. Индикаторные ошибки титрования [c.132]
Ошибка титрования близка нулю, если потенциал перехода окраски индикатора равен потенциалу в точке эквивалентности. Практически допустимой считают относительную ошибку в10 или 0,1 7о, благодаря чему возможен широкий выбор окислительно-восстановительных индикаторов. При титровании восстановителя 2 окислителем 1 предельные значения потенциа-.лов (в вольтах) получают из следующих уравнений [c.170]
Кривые титрования хлоридов нитратом серебра в расплавленных солях получаются такими же, как кривые титрования в водных растворах для экзотермических процессов. Относительная ошибка титрования для указанных выше концентраций приближалась к 4%. Применение метода ограничено в связи с трудностью достаточно точного измерения повышения температуры, происходящего в результате реакции. Необходимо, чтобы изменение температуры окружающей среды было на несколько порядков меньше, чем изменение температуры, происходящее в результате рассматриваемой реакции. Теоретически в среде расплавленных солей возможно проводить любые реакции осаждения, комплексообразования или окислительно-восстановительные реакции, однако практически сложность прибора, который требуется для этого, ограничивает применимость расплавленных солей в качестве растворителей. [c.110]
На практике расчет потенциала при помощи такого уравнения, как правило, связан с ошибкой, хотя во многих случаях эта ошибка невелика и полученное значение потенциала является полезным для предсказания возможности проведения того или иного титрования. Во всех окислительно-восстановительных системах, включающих ионы водорода, потенциал обычно зависит от концентрации этих ионов, однако степень такой зависимости может значительно отличаться от величины, полученной по уравнению. Такая же картина иногда наблюдается и для зависимости потенциала от концентрации окисленной и (или) восстановленной формы вещества. [c.353]
Разница в объемах постоянна для всех выбранных на кривой точек, до которых проводилось титрование, и является, вероятно, приборной ошибкой. Результаты титрования до заданного потенциала показывают, что при помощи автотитратора можно приготавливать растворы с заранее заданными величинами окислительно-восстановительного потенциала или pH, что позволяет автоматизировать процесс подготовки проб к дальнейшему анализу при серийных определениях. [c.136]
Для окислительно-восстановительного титрования перманганата применяют также другие восстановители, в том числе соединения Си, Sn , W», U , V [17], однако преимущества применения этих восстановителей не очевидны. Сравнительно простой окислительно-восстановительный метод основан на взаимодействии перманганата с кислым раствором KI и последующем титровании выделившегося иода стандартным раствором тиосульфата. Избирательность определения часто достигается применением маскировки. Например, в указанном выше методе перманганат (или хромат) можно определять в присутствии железа (III), которое маскируют гексаметафосфатом [18]. При определении 13—65 мг марганца (в виде MnO ) в присутствии 10—340 мг Fe + ошибка составляет 0,3%. [c.159]
В Присутствии восстановителей-абсорбентов в ячейке для поглощения. Осуществить такое определение с хлор- или бромсеребряными электродами не представляется возможным, так как они дают ошибку, связанную с возникновением на них окислительно-восстановительного потенциала. Сжигание проводится обычным способом, потенциометрическое титрование идет в 50%-ном диоксане. Титруют 0,02 М раствором нитрата серебра. Вблизи конечной точки титрант вводят равными порциями по 0,02 мл. Конечную точку определяют как максимальное значение Д /Д . [c.62]
Амперометрическое титрование применимо для многих окислительно-восстановительных реакций, реакций комплексообразования и осаждения. По сути этот метод обладает более высокой точностью, чем соответствующий прямой полярографический метод, так как каждое определение включает ряд отдельных измерений, для которых исключаются случайные ошибки. [c.359]
Преимущество флуоресцентных окислительно-восстановительных индикаторов по сравнению с цветными состоит в том, что с их применением можно значительно уменьшить ошибки титрования, связанные с расходом титранта на окисление индикатора. Кроме того, возможно титрование в окрашенных и мутных средах . [c.120]
Окислительно-восстановительные реакции в большинстве случаев протекают в сильно кислой среде небольшие изменения электропроводности за счет реакции окисления-восстановления на фоне высокой проводимости среды обусловливают нерезкие перегибы кривой титрования в конечной точке. Это приводит к значительным ошибкам в определении конечной точки. В работе [69] систематизированы реакции этого типа в наглядной таблице для целей кондуктометрического титрования. Эта таблица может быть использована при разработке методов ВЧ-титрования окислителей и восстановителей. [c.156]
Последние соотнощения показывают, что в состоянии равновесия концентрация Мп2+ будет превыщать концентрацию МпО в 1025 раз . р g процесс восстановления ионов МпО в Мп2+ пройдет с исчерпывающей для практической цели полнотой. Поэтому можно считать, что ощибка титрования, обусловленная образованием равновесной системы, будет равна нулю (такое количественное течение процесса вообще характерно для большинства окислительно-восстановительных реакций). Ввиду этого ошибки, допускаемые при перманганатометрических определениях, должны быть отнесены лишь за счет капельной ошибки, неточностей при отсчетах и взвешиваниях, а также необходимости введения некоторого избытка перманганата, позволяющего установить конец реакции по появлению окраски раствора. [c.85]
Практикум содержит 47 лабораторных заданий. Многие задания оригинальны по постановке и рассчитаны на получение количественных результатов. Некоторые из задач могут быть использованы как факультативные. Новые работы посвящены методам очистки веществ ионитами и зонной плавкой, определению термодинамических характеристик процесса растворения бензойной кислоты и процесса восстановления ионов меди цинком, определению координационного числа методами криоскопии и титрования, кинетике окислительно-восстановительных реакций и изучению поверхностно-активных веществ. Заново написано задание по определению тепловых эффектов. В новом издании практикума лабораторным заданиям предпослано введение, где рассказывается о научном эксперименте и его роли в познании, и глава о работе с экспериментальными данными, в которой идет речь о записи результатов, вычислениях, ошибках эксперимента, выражении результатов в виде графиков и формул и о написании отчета. Остальные задания практикума подверглись значительной переработке. В приложении появился ряд новых таблиц. [c.3]
В книге на современном уровне кратко изложены теоретические основы гравиметрии и титриметрии — образование и свойства осадков, типы химических равновесий в гомогенных и гетерогенных растворах описаны кривые титрования проанализированы ошибки в кислотно-основном, осацительном, комплексимет-рическом и окислительно-восстановительном титровании. Подробно рассмотрены аппаратура и техника проведения всех операций в количественном химическом анализе. Все расчеты проведены с учетом новых данных о величинах констант, стандартных потенциалов и т.п. [c.2]
Окислительно-восстановительный потенциал аскорбиновой кислоты при pH 7 составляет — -0,19 в. Аскорбинометрическое определение железа является одним из лучших методов, так как не мешают нитраты и фосфаты присутствие фторидов вызывает незначительную ошибку. Недостатком является малая устойчивость титрованного раствора аскорбиновой кислоты при хранении. [c.193]
Кинетическое окислительно-восстановительное титрование Sb(lII). Реакционную смесь титруют раствором окислителя (КВгОз, Ja, e(S04)2, K rjO,, KJO3) в строго определенных условиях (pH, температура, объем) при постоянной скорости подачи титранта с потенциометрическим, фотометрическим или визуальным (индикаторы ксиленоловый оранжевый, ферроин) установлением конечной точки. По продолжительности титрования, которое прямо пропорционально содержанию Sb, находят ее содержание. Метод позволяет определять Sb в растворах с ее концентрацией 8-10 —1,2-10 с ошибкой 2—5% [953, 1326]. [c.98]
Эрдеи и Ради [938] титровали Au(III) аскорбиновой кислотой при pH 1—3 и 50—60° С. При температуре > 80° С получаются заниженные результаты. Не мешают Hg(II), u, Fe(III) (в присутствии НэР04), 150-кратные количества NOJ, 1 г-ион л С мешают ионы со стандартным окислительно-восстановительным потенциалом > — — 1,39 в [Pt(IV), Вг , S N и N ]. Ошибка определения золота в 0,001—0,01 N растворах 1%. При титровании в среде ледяной уксусной кислоты [937] вид кривой титрования похож на кривую титрования в водных растворах, если перед титрованием в безводной уксусной кислоте ввести безводный Ha OONa. В точке эквивалентности наблюдается отчетливый скачок потенциала. Аналогично золоту ведут себя другие окислители. [c.130]
ВОЗМОЖНОЙ благодаря снижению окислительно-восстановительного потенциала пары Fe +/Fe + за счет образования устойчивых пирофосфатных комплексов Ее(П1) при pH 9, а в начале титрования — при pH 12 [915]. Титрование ведут 0,01 JV раствором ЕеЗОд в инертной атмосфере с обязательным добавлением в анализируемый раствор бромид-иона, препятствующего диспропорцио-нированию гипобромит-иона. 1 —10 мг ВгО определяют этим методом с ошибкой -< 0,5%. Примеси BrOJ (до 16%), 10-кратное количество ионов СГ или J , 10-кратный избыток сульфат-иона и 150-кратный нитрат-иона не мешают анализу. [c.129]
При прямом титровании фосфатов раствором соли свинца [1172] при рн 2—3 в качестве индикатора применяют хлороформный раствор дитизона. Титруют до перехода зеленой окраски в фиолетовую. Метод применяют для определения фосфора в фосфатных удобрениях [1174]. В качестве индикатора применяют также эриох-ром черный Т (растворяют 0,2 г эриохрома черного Т в 5 мл С2Н5ОН и 15 мл триэтаНоламина) [950]. Титруют до появления красной окраски. Метод применяют для определения микроколичеств фосфора в органических веществах. Для определения микроколичеств фосфора применяют также титрование нитратом свинца в присутствии 2-азо-4-резорцина [1018]. Титруют до появления красного окрашивания. При содержании фосфора 20— 400 мкг средняя абсолютная ошибка определения составляет 2—3 мкг Р. При косвенном определении фосфатов с помощью нитрата свинца применяют окислительно-восстановительные индикаторы [732, 733]. Метод основан на осаждении РО/ в виде РЬз(Р04)2 нитратом свинца, избыток которого оттитровывают К4[Ге(СК)б1 в присутствии вариаминового синего и Кз[Ге(СК)б] в качестве индикатора. Титруют до перехода фиолетовой окраски в бледно-желтую. [c.37]
Предложен интересный метод окислительно-восстановительного титрования, основанный на применении гидрохинона [20]. Метод позволяет определять 10—130 мг перманганата в присутствии других окислителей, например, бихромата, гексацианоферрата (III) и хлорамина Т. При определении 13—130 мг КМПО4 в присутствии 20—2000 мг других окислителей относительная ошибка оп-)еделения не превышает 1,8%. Определению мешает ванадий (V). Метод длителен сначала перманганат восстанавливают до диоксида марганца с помощью формиата натрия в щелочном растворе. Осадок гидратированного диоксида марганца фильтруют, промывают, растворяют в ЫагНгРгОу и образующийся пирофосфат марганца (III) титруют стандартным раствором гидрохинона. [c.159]
Хотя растворы бихромата окрашены в оранжевый цвет, интенсивность окраски недостаточна для определения конечной точки. Отличным индикатором при титровании бихроматом является дифениламиносульфокислота (гл. 15) с переходом окраски от зеленой (ионы хрома(1П)) до фиолетовой (окисленная форма индикатора). Холостой опыт в присутствии индикатора идет плохо, поскольку в отсутствие других окислительно-восстановительных систем бихромат очень медленно окисляет индикатор. Но ошибка, возникающая за счет того, что холостой опыт не проведен, обычно пренебрежимо мала. Реакция окисления дифениламиносульфокис-лоты обратима, поэтому можно проводить обратное титрование очень малых количеств бихромата железом (II). В присутствии больших количеств окислителя при низкой кислотности (рН>2) раствора индикатор необратимо окисляется до соединений желтого или красного цвета. [c.386]
Метод определения конечной точки. Как уже отмечалось, перманганат-ион имеет настолько интенсивный цвет, что сам по себе может служить индикатором. Опыты показали, что при титровании мышьяковистой кислоты перманганатом концентрация иона МпОГ. равная б-10 моль/л, легко обнаруживается вблизи точки эквивалентности. В расчетах, проведенных для одного из опытов титрования, мы показали, что при введении 0,1% избытка титранта концентрация МпОГ составляет 8-10 моль/л. Таким образом, ясно, что при использовании цвета избыточного Мп04 для установления точки эквивалентности вводится ошибка менее 0,1 %. Однако можно подобрать окислительно-восстановительный индикатор, при применении которого конечная точка еще точнее соответствовала бы точке эквивалентности. В рассматриваемом случае важнее даже то, что при использовании индикатора конечную точку можно обнаружить еще в тот момент, когда концентрация МпОГ слишком низка, чтобы окислить хлорид-ионы, присутствующие в растворе. Один из таких индикаторов — о-фенаитролиповый комплекс желе-за П), с которым могут происходить следующие превращения [c.235]
Работа установки проверялась не только титрованием в кислотно основных и окислительно-восстановительных сис темах, но также пу тем определения миллиграммовых количеств галогенид ионов их осаждением ионами серебра, г енерированнымн электрохимически. Определения проводят в бюксе на 75 мл, анодом служит серебро вы сокой чистоты или платина, покрытая серебром, катодом — платиновая спираль, снабженная чехлом. В качестве индикаторного электрода используют серебряную или платиновую проволоку, потенциал ко торой измеряется относительно каломельного электрода сравнения, причем для устранения загрязнения хлоридом последний под.-оединя-н.т с помощью агарового солевого мостика- с 0,1 М раствором а. 0,. При определении хлорида, бромида и иодида в количествах 0,2 — 10 средняя ошибка составляет 0,005 мг. [c.86]
1.
Окислительно-восстановительное
титрование
1
2.
Mэкв(X) = fэкв · М(X)
f = 1/z
z – число электронов, принимающих участие в
окислительно-восстановительной реакции
2
3.
10FeSO4 + 2KMnO4 + 8H2SO4 2MnSO4 +
5Fe2(SO4)3 + K2SO4 + 8H2O
MnO4 + 8H+ + 5ē Mn2+ + 4H2O
2Fe2+ 2ē Fe23+
3
4.
10FeSO4 + 2KMnO4 + 8H2SO4 2MnSO4 +
5Fe2(SO4)3 + K2SO4 + 8H2O
MnO4 + 8H+ + 5ē Mn2+ + 4H2O
2Fe2+ 2ē Fe23+
fэкв(KMnO4) = 1/5,
M(1/5KMnO4) = M(KMnO4) /5;
fэкв(FeSO4) = 1
M(FeSO4) = M(FeSO4)/1
4
5.
I2 + 2Na2S2O3 2NaI + Na2S4O6
I2 + 2ē 2I
2S2O32 2ē S4O62
5
6.
I2 + 2Na2S2O3 2NaI + Na2S4O6
I2 + 2ē 2I
2S2O32 2ē S4O62
fэкв(I2) = 1/2
M(1/2 I2) = M(I2)/2;
fэкв(Na2S2O3) = 1
M(Na2S2O3) = M(Na2S2O3)/1
6
7.
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3 +
K2SO4 + 7H2O
Cr2O72 + 14H+ + 6ē Cr23+ + 7H2O
2I 2ē I2
7
8.
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3 +
K2SO4 + 7H2O
Cr2O72 + 14H+ + 6ē Cr23+ + 7H2O
2I 2ē I2
fэкв(K2Cr2O7) = 1/6
Mэкв(K2Cr2O7) = M(K2Cr2O7)/6
fэкв(KI) = 1
M(KI) = M(KI)/1
8
9.
H2SO4
CH4
CH3—CH2OH
CH3OH
H
HCOH
H
H
CH3—COOH
H
H
H
9
10.
–4
–2
CH4
CH3OH
–3
–1
CH3—CH2OH
+1
HCOH
–3
-1
+3
CH3—COOH
10
11.
O O
OH OH
H
+1
H +2
+1
O
O
+2
CHOH
O
CHOH
CH2OH
CH2OH
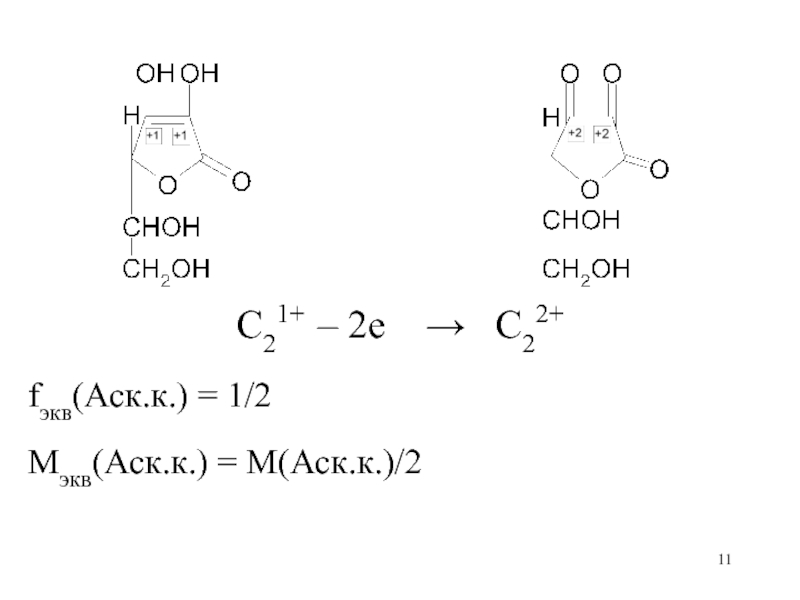
C21+ – 2е
O
C22+
fэкв(Аск.к.) = 1/2
Mэкв(Аск.к.) = M(Аск.к.)/2
11
12.
Перманганатометрия
Титрант – 0,02 М или 0,1 М (1/5 KMnO4) или
0,1 н. раствор KMnO4
По точной навеске приготовить нельзя, т.к.
сильный окислитель.
Готовят раствор приблизительно нужной концентрации, выдерживают 7-10 дней или
кипятят 10 минут для окисления восстановителей, содержащихся в воде
Фильтруют через стеклянный фильтр.
12
13.
Стандартизацию проводят по щавелевой кислоте H2C2O4 2H2O, оксалату натрия Na2C2O4,
оксиду мышьяка (III) As2O3, металлическому
железу.
Стандартизацию проводят только в сернокислой
среде.
16HCl + 2KMnO4 5Cl2 + 2MnCl2 + 2KCl +8H2O
Индикатор – сам титрант.
13
14.
Стандартизация 0,1 н. по щавелевой кислоте
60-70 0С
5H2C2O4 + 2KMnO4 + 3H2SO4 2MnSO4 +
10CO2 + K2SO4 + 8H2O
C2O42– – 2е 2CO2
14
15.
Этикетка:
0,02 М или 0,1 М (1/5KMnO4) или 0,1 н.
К = 0,9972
Хранят в темном месте, в склянках темного
стекла
свет
4KMnO4 + 2H2O 4MnO2 + 4 KOH + 3H2O
По ГФ XIII стандартизация по тиосульфату
натрия
15
16.
Применение:
прямая перманганатометрия
Железа (II) сульфат:
10FeSO4 + 2KMnO4 + 8H2SO4 5Fe2(SO4)3 +
K2SO4 + 2MnSO4 + 8H2O
2Fe2+ – 2е Fe23+
Сэкв(KMnO4)·Mэкв(FeSO4)
Т(KMnO4/FeSO4) = ————————————
1000
16
17.
m(FeSO4) = V(KMnO4)·K·T(KMnO4/FeSO4)
V(KMnO4)·K·T(KMnO4/FeSO4)·100
(FeSO4) = ——————————————, %
а(FeSO4)
17
18.
Перекись водорода:
5H2O2 + 2KMnO4 + 3H2SO4 5O2 + K2SO4 +
2MnSO4 + 8H2O
O22– – 2е O2
Сэкв(KMnO4)·Mэкв(H2O2)
Т(KMnO4/H2O2) = ————————————
1000
18
19.
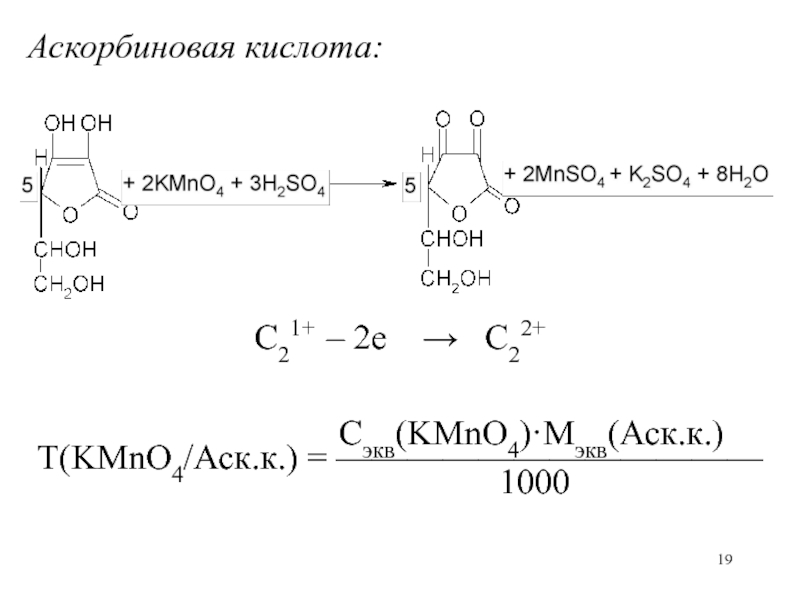
Аскорбиновая кислота:
O O
OH OH
H
H
5
+ 2KMnO4 + 3H2SO4
O
5
CHOH
O
CHOH
CH2OH
CH2OH
O
C21+ – 2е
+ 2MnSO4 + K2SO4 + 8H2O
O
C22+
Сэкв(KMnO4)·Mэкв(Аск.к.)
Т(KMnO4/Аск.к.) = ————————————
1000
19
20.
обратная перманганатометрия
Натрия нитрит:
5NaNO2 + 2KMnO4(изб.) + 3H2SO4 5NaNO3 +
2MnSO4 + K2SO4 + 3H2O
2KMnO4(ост.) + 10KI + 8H2SO4 2MnSO4 + 5I2
+ 6K2SO4 + 8H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6
20
21.
(VKMnO4 K VNa2S2O3 K) Т(Na2S2O3/NaNO2) 100
(NaNO2)= (%)
а (NaNO2)
Сэкв(Na2S2O3) Мэкв(NaNO2)
Т(Na2S2O3/NaNO2) =
1000
NO2– + H2O – 2е
N3+ – 2е
NO3– + 2H+
N5+
21
22.
5NaNO2 + 2KMnO4(изб.) + 3H2SO4 5NaNO3 +
2MnSO4 + K2SO4 + 3H2O
NO2– + H2O – 2е NO3– + 2H+
| 5
MnO4– + 8H+ + 5е Mn2+ + 4H2O | 2
5NO2– + 2MnO4– + 16H+ + 5H2O
5NO3– + 10H+ + 2Mn2+ + 8H2O
или
5NO2– + 2MnO4– + 6H+ 5NO3– + 2Mn2+ + 3H2O
22
23.
Кривые окислительно-восстановительного
титрования
Выражают зависимость величины потенциала
от концентрации титранта
23
24.
Задача. Рассчитать и построить кривую титрования соли Fe (II) раствором перманганата
калия, если
Eo (Fe3+/Fe2+) = + 0,77 B;
Eo (MnO4–/Mn2+) = + 1,51 B
Какой из индикаторов можно использовать в
данном случае?
24
25.
2,2 – Дипиридил (комплекс с рутением)
Ео = 1,33 В
Дифениламин-2,2 –дикарбоновая кислота
Ео = 1,26 В
Комплекс 1,10-фенантролина с Fe (II)
Ео = 1,14 В
Фенилантраниловая кислота Ео = 1,08 В
Дифениламин
Ео = 0,76 В
Метиленовый голубой
Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
25
26.
5Fe2+ + MnO4– + 8H+ 5Fe3+ + Mn2+ + 4H2O
В начале титрования и до т.э. в растворе будут:
Fe2+, Fe3+ ,Mn2+
Потенциал системы будет определяться парой
восстановителя Fe3+/Fe2+
Величина потенциала может быть вычислена по
уравнения Нернста:
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
26
27.
В точке эквивалентности:
E = (mEoв-ля + nEoок-ля )/(m + n)
27
28.
5Fe2+ + MnO4– + 8H+ 5Fe3+ + Mn2+ + 4H2O
за т. э. в растворе будут:
Fe3+, MnO4– и Mn2+
Потенциал будет определяться парой
окислителя MnO4– /Mn2+
Величина потенциала вычисляется по
уравнению Нернста:
E = Eo + 0,059/5 lg[MnO4–][H+]8/[Mn2+]
28
29.
Пусть концентрация ионов водорода равна 1 М
Доб-но
От-но
KMnO4–
в%
[Fe3+]
———
[Fe2+]
9
9
9/91 10-1
-1
0,77–0,059=0,71В
50
50
50/50=1
0
0,77 В
99
99
99/1 102
2
0,77+0,059 2=0,89В
3
0,77+0,059 3=0,95В
99,9
100
99,9 99,9/0,1 103
[Fe3+]
lg ———
[Fe2+]
E=Eo +0,059/1
lg [Fe3+]/[Fe2+]
E = (mEoв-ля+nEoок-ля )/(m+n)=(1 0,77+5 1,51)/(1+5)
=1,39 29B
30.
Доб-но
Изб-к
KMnO4–
в%
100,1
0,1
[MnO4–][H+]8
————— lgдроби E=Eo +0,059/5lgдр
[Mn2+]
0,1/100 10-3 -3
1,51+(0,059/5) (-3) =
1,475 B
101
1
1/100=10-2
-2
1,51+(0,059/5) (-2)
= 1,486 B
110
10
10/100=10-1
-1
1,51+(0,059/5) (-1)
= 1,498 B
30
31.
Скачок от 0,95 В до 1,475 В
2,2 – Дипиридил (комплекс с рутением)
Ео = 1,33 В
Дифениламин-2,2 –дикарбоновая кислота
Ео = 1,26 В
Комплекс 1,10-фенантролина с Fe (II)
Ео = 1,14 В
Фенилантраниловая кислота Ео = 1,08 В
Дифениламин Ео = 0,76 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
31
32.
Интервал изменения окраски индикаторов
Ind(ок) + ne Ind(вос)
0,059
[Ind(ок)]
E = Eo + ——— lg ————
n
[Ind(вос)]
[Ind(ок)]
———— = 10 – наблюдаем окраску окисленной
[Ind(вос)]
формы
E = Eo + 0,059/n lg10 = Eo + 0,059/n
32
33.
[Ind(ок)]
——— = 0,1 – наблюдаем окраску восстановл.
[Ind(вос)]
формы
E = Eo + 0,059/n lg 0,1 = Eo – 0,059/n
E = Eo ± 0,059/n
33
34.
Индикаторы окислительно-восстановительного
титрования
1. Специфические – индикаторы, которые взаимодействуют с одной из форм окислительновосстановительной пары с изменением
окраски (крахмал)
2. Редокс-индикаторы — вещества, которые при
определенном потенциале раствора окисляются или восстанавливаются с изменением
окраски
34
35.
Редокс-индикаторы:
1. Обратимые
E = Eo ± 0,059/n
Дифениламин Ео = 0,76 В
бесцветный – фиолетовый
м.р. в воде, готовят 1% р-р в концентр. H2SO4
Ферроин – комплекс Fe(II) с о-фенантролином
Ео = 1,14 В
[FeL3]2+ – e [FeL3]3+
красная
бледно-голубая
Фенилантраниловая кислота (Ео = 1,08 В) и др.
35
36.
2. Необратимые
Метиловый оранжевый
Метиловый красный,
Нейтральный красный
При окислении необратимо исчезает окраска
раствора
36
37.
Индикаторные ошибки окислительновосстановительного титрования
Индикаторная ошибка рассчитывается по
формуле:
n’(X)
Х = ———— · 100
n(X)
n’(X) – количество неоттитрованного вещества
(или избыточно прибавленного титранта)
n(X) – количество вещества, взятого для
титрования
37
38.
Задача. Рассчитать ошибку титрования железа
сульфата (II) раствором KMnO4 в сернокислой
среде при [H+] = 1 моль/л с индикатором
дифениламином (Ео = 0,76 В).
Потенциал системы в т.э.:
E = (mEoв-ля+nEoок-ля )/(m+n)=(1 0,77+5 1,51)/(1+5)
=1,39 B
38
39.
Таким образом,
Изменение окраски произойдет при 0,76 В
Т.э. наступит при 1,39 В, следовательно,
раствор недотитрован.
Потенциал системы рассчитывался по паре
[Fe3+]/[Fe2+] (Eo = 0,77 В) и закончили
титровать при 0,76 В
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
0,76 = 0,77 + 0,059/1 lg[Fe3+]/[Fe2+]
39
40.
lg[Fe3+]/[Fe2+] = – 0,169
[Fe3+]
0,68
———— = 0,68 = ———
[Fe2+]
1
n’(X)
Х = ———— · 100
n(X)
n’(X) = 1 (количество неоттитрованного в-ва)
n(X) = 1 + 0,68 (количество вещества, взятого
для титрования)
40
41.
Ошибка титрования составит:
1
Х = ———— · 100 = 59,5 %
1 + 0,68
Индикаторная ошибка д.б. не более 0,1 %.
41
42.
Задача. Рассчитать и построить кривую
титрования соли олова (II) раствором соли
железа (III), если Eo (Fe3+/Fe2+) = + 0,77 B и
Eo (Sn4+/Sn2+) = + 0,15 B.
Какой из индикаторов вы выберете?
Дифениламин Ео = 0,76 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
Нейтральный красный Ео = 0,24 В
Рассчитать ошибку титрования с индикатором –
метиленовый голубой
42
43.
Sn2+ + 2Fe3+ Sn4+ + 2Fe2+
В начале титрования и до т.э. в растворе будут:
Sn2+, Sn4+, Fe2+
Потенциал системы будет определяться парой
восстановителя Sn4+/Sn2+,
Величина потенциала вычисляется по
уравнению Нернста:
E = Eo + 0,059/2 lg[Sn4+]/[Sn2+]
43
44.
В точке эквивалентности:
E = (mEoв-ля + nEoок-ля )/(m + n)
E = (2 · 0,15 + 1· 0,77) / 3 = 0,36 B
44
45.
Sn2+ + 2Fe3+ Sn4+ + 2Fe2+
за т. э. в растворе будут:
Fe3+, Sn4+, Fe2+
Потенциал будет определяться парой
окислителя Fe3+/Fe2+
Величина потенциала вычисляется по
уравнению Нернста:
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
45
46.
Доб-но
Fe3+
От-но
в%
[Sn4+]
———
[Sn2+]
[Sn4+]
lg ———
[Sn2+]
E
9
9
9/91 10-1
-1
0,12 В
50
50
50/50 1
0
0,15 В
90
90
90/10 101
1
0,18 В
99
99
99/1 102
2
0,21 В
99,9
99,9
99,9/0,1 103
3
0,24 В
100
0,36 B
46
47.
Доб-но
Fe3+
Изб-к
в%
100,1
0,1
0,1/100 10-3
-3
0,59 B
101
1
1/100=10-2
-2
0,65 B
110
10
10/100=10-1
-1
0,71 B
[Fe3+]
———
[Fe2+]
[Fe3+]
lg ———
[Fe2+]
E
Скачок от 0,24 В до 0,59 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
Нейтральный красный Ео = 0,24 В
47
48.
Изменение окраски произойдет при 0,53 В
Т.э. наступит при 0,36 В, следовательно,
раствор перетитрован.
Потенциал системы рассчитывался по паре
окислителя [Fe3+]/[Fe2+] (Eo = 0,77 В)
Закончили титровать при 0,53 В
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
0,53 = 0,77 + 0,059/1 lg[Fe3+]/[Fe2+]
48
49.
lg[Fe3+]/[Fe2+] = – 6,949
[Fe3+]
1·10–7
———— = 1·10–7 = ———
[Fe2+]
1
1·10–7
Х = ——— · 100 = 1·10–5 %
1
n’(X) = 1·10–7 (количество избыточно прибавленного титранта)
n(X) = 1 + 1·10–7 1 (количество вещества,
взятого для титрования)
49
50.
Дихроматометрия
Титрант – 0,0167 М или 0,1 М (1/6 K2Cr2O7)
или 0,1 н. раствор K2Cr2O7
Стандартный раствор можно приготовить по
точной навеске
Cr2O72 + 14H+ + 6ē 2Cr3+ + 7H2O
fэкв(K2Cr2O7) = 1/6
Mэкв(K2Cr2O7) = M(K2Cr2O7)/6
50
51.
K2Cr2O7 – оранжевая окраска
Cr3+ – зеленоватая окраска, однако
интенсивности цвета не хватает для фиксации
конечной точки титрования
Ind – дифениламин, дифениламинсульфоновая
кислота и др.
51
52.
а(K2Cr2O7)теор=Сэкв(K2Cr2O7)·Mэкв(K2Cr2O7)·V (л)
а(K2Cr2O7)прак
Сэкв(K2Cr2O7)прак = —————————
Mэкв(K2Cr2O7) · V(л)
Сэкв(K2Cr2O7)прак
K = ————————
Сэкв(K2Cr2O7)теор
52
53.
Применение:
прямая дихроматометрия
Железа (II) сульфат:
6FeSO4 + K2Cr2O7 + 7H2SO4 3Fe2(SO4)3 +
Cr2(SO4)3 + K2SO4 + 7H2O
2Fe2+ – 2е Fe23+
Сэкв(K2Cr2O7)·Mэкв(FeSO4)
Т(K2Cr2O7/FeSO4) = ———————————
1000
53
54.
Расчет массы и массовой доли (%)
m(FeSO4) = V(K2Cr2O7)·K·T(K2Cr2O7/FeSO4)
V(K2Cr2O7)·K·T(K2Cr2O7/FeSO4)·100
(FeSO4) = ——————————————, %
а(FeSO4)
54
55.
Калия иодид:
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3 +
4K2SO4 + 7H2O
2I– – 2е I2
Сэкв(K2Cr2O7)·Mэкв(KI)
Т(K2Cr2O7/KI) = ——————————
1000
55
56.
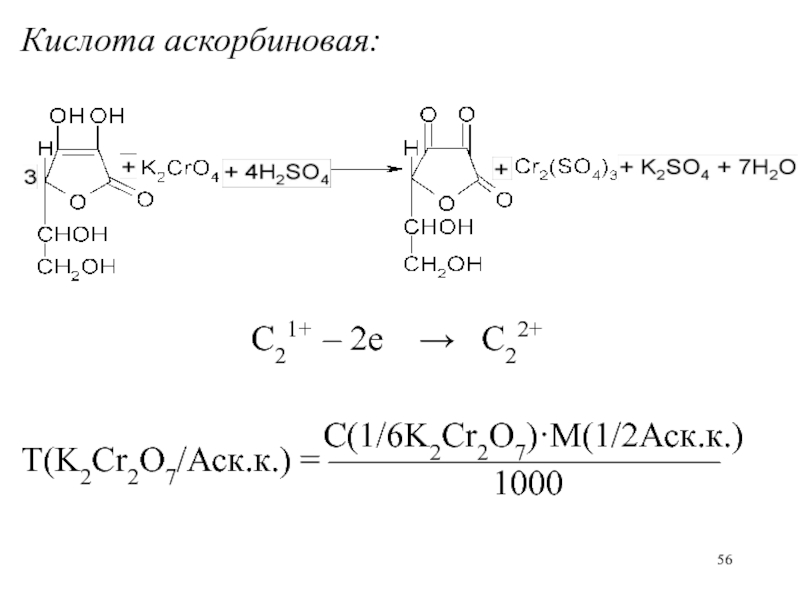
Кислота аскорбиновая:
O O
OH OH
H
3
O
+ K2CrO4 + 4H SO
2
4
O
H
CHOH
O
CHOH
CH2OH
CH2OH
C21+ – 2е
+ Cr2(SO4)3 + K2SO4 + 7H2O
O
C22+
С(1/6K2Cr2O7)·M(1/2Аск.к.)
Т(K2Cr2O7/Аск.к.) = ———————————
1000
56
57.
Обратная дихроматометрия применяется для
определения спирта этилового:
3CH3CH2OH + 2K2Cr2O7 + 8H2SO4
избыток
3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
K2Cr2O7 + 6KI + 7H2SO4 3I2 + Cr2(SO4)3 +
остаток
4K2SO4 + 7H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6
57
58.
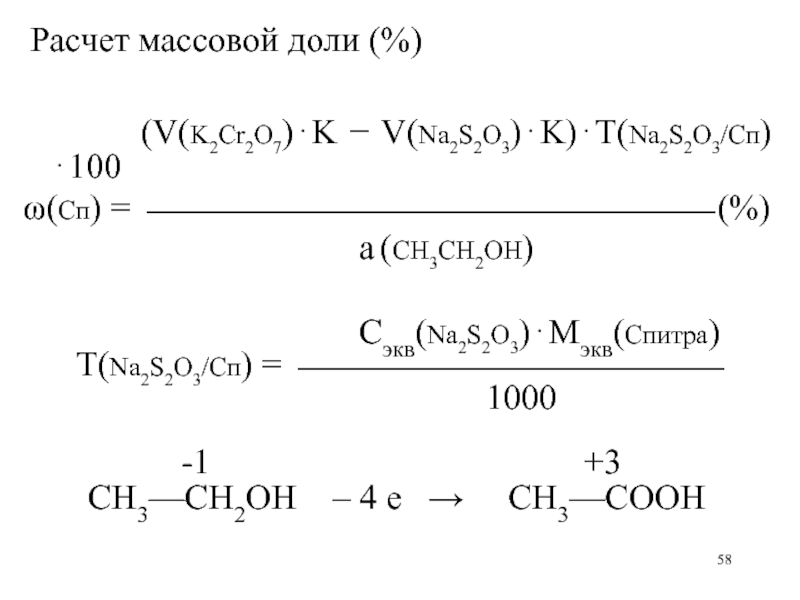
Расчет массовой доли (%)
(V(K2Cr2O7) K V(Na2S2O3) K) Т(Na2S2O3/Сп) 100
(Сп) = (%)
а (CH3CH2OH)
Сэкв(Na2S2O3) Мэкв(Спитра)
Т(Na2S2O3/Сп) =
1000
-1
CH3—CH2OH – 4 е
+3
CH3—COOH
58
59.
Преимущества дихроматометрии перед
перманганатометрией
1. Титрант можно приготовить по точной
навеске
2. Титрование можно проводить в присутствии
HCl
Eo(Cr2O72–/2Cr3+) = 1,33 B
Eo(Cl2/2Cl–) = 1,33 B
При титровании Cl– не окисляются Cr2O72–ионами
59
Слайд 1
Окислительно-восстановительное
титрование

Слайд 2
Mэкв(X) = fэкв · М(X)
f = 1/z
z – число электронов,
принимающих участие в окислительно-восстановительной реакции

Слайд 3
10FeSO4 + 2KMnO4 + 8H2SO4 2MnSO4 +
5Fe2(SO4)3 +
K2SO4 + 8H2O
MnO4 + 8H+ + 5ē Mn2+ +
4H2O
2Fe2+ 2ē Fe23+
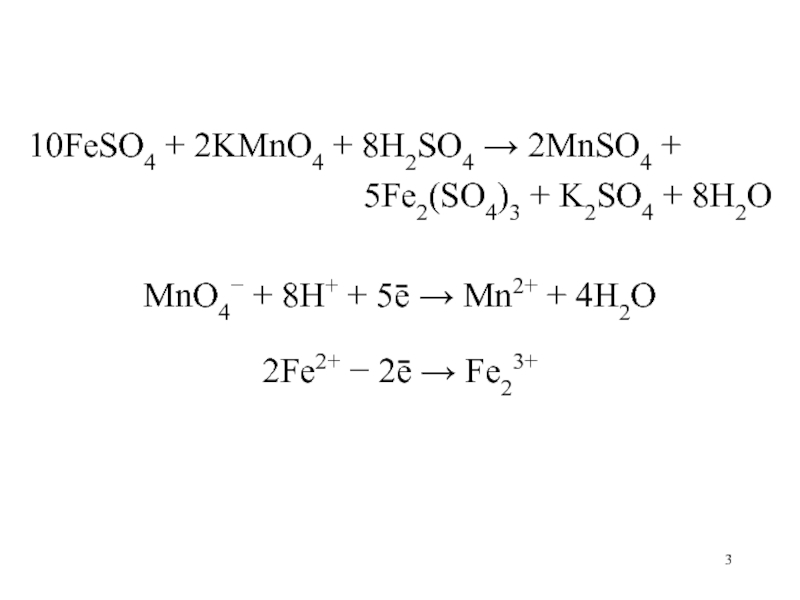
Слайд 4
10FeSO4 + 2KMnO4 + 8H2SO4 2MnSO4 +
5Fe2(SO4)3 +
K2SO4 + 8H2O
MnO4 + 8H+ + 5ē Mn2+ +
4H2O
2Fe2+ 2ē Fe23+
fэкв(KMnO4) = 1/5,
M(1/5KMnO4) = M(KMnO4) /5;
fэкв(FeSO4) = 1
M(FeSO4) = M(FeSO4)/1
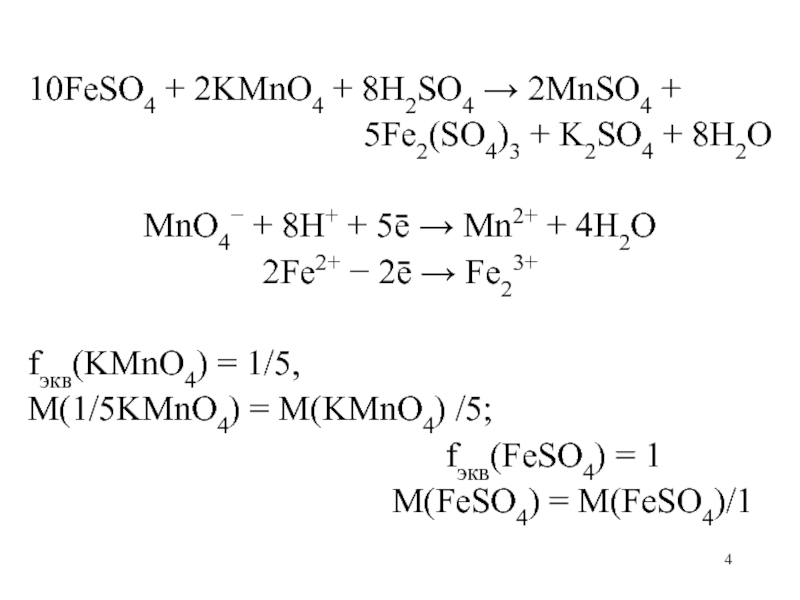
Слайд 5
I2 + 2Na2S2O3 2NaI + Na2S4O6
I2 + 2ē
2I
2S2O32 2ē S4O62
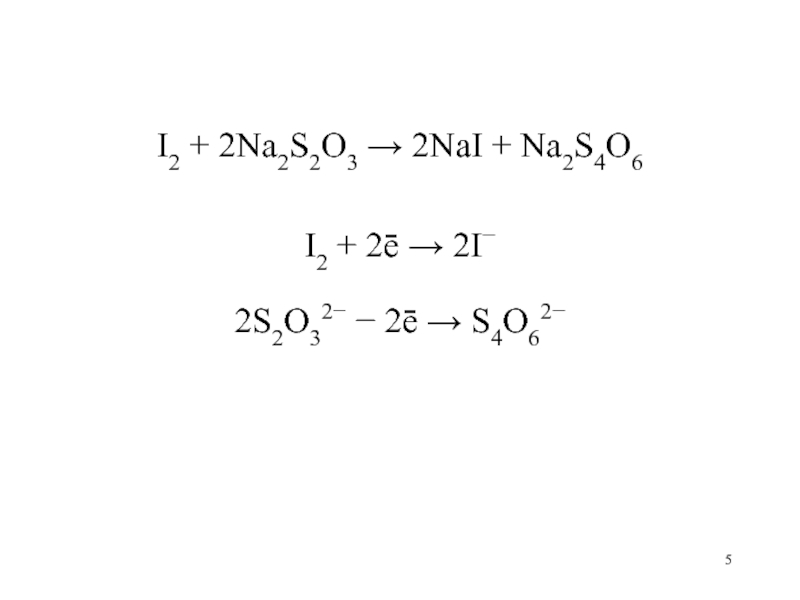
Слайд 6
I2 + 2Na2S2O3 2NaI + Na2S4O6
I2 + 2ē
2I
2S2O32 2ē S4O62
fэкв(I2) = 1/2
M(1/2 I2) = M(I2)/2;
fэкв(Na2S2O3) = 1 M(Na2S2O3) = M(Na2S2O3)/1
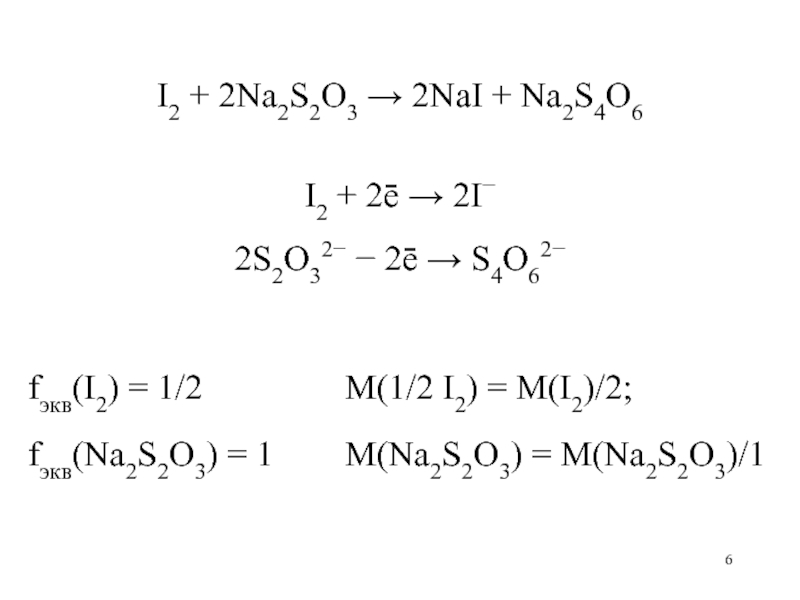
Слайд 7
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3 +
K2SO4 + 7H2O
Cr2O72 + 14H+ + 6ē Cr23+ +
7H2O
2I 2ē I2
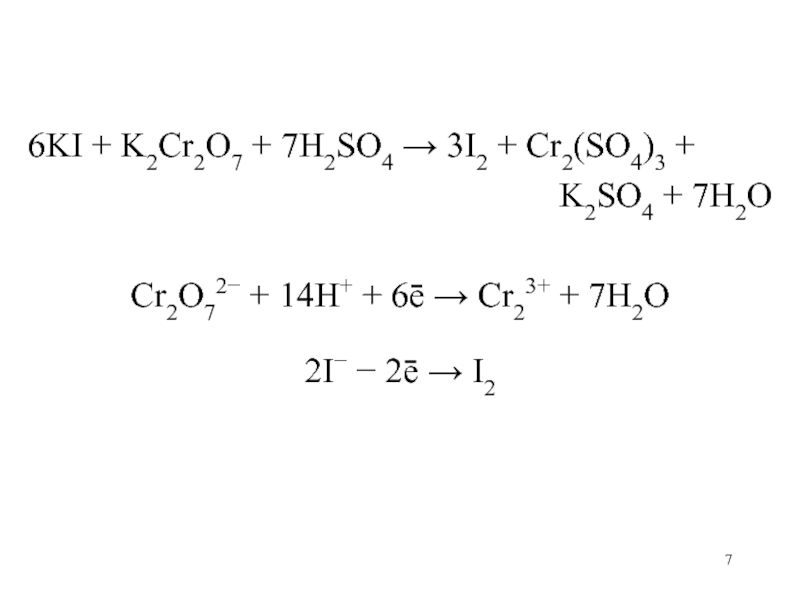
Слайд 8
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3 +
K2SO4 + 7H2O
Cr2O72 + 14H+ + 6ē Cr23+ +
7H2O
2I 2ē I2
fэкв(K2Cr2O7) = 1/6
Mэкв(K2Cr2O7) = M(K2Cr2O7)/6
fэкв(KI) = 1
M(KI) = M(KI)/1
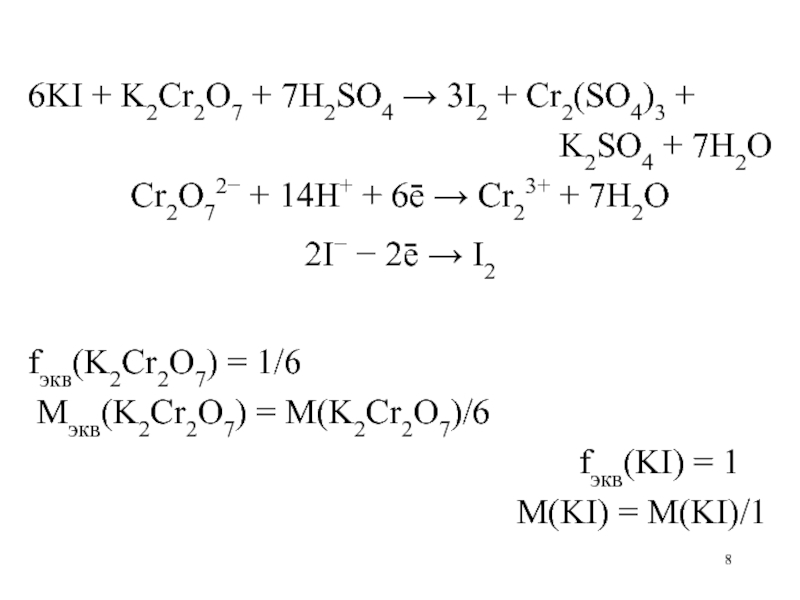
Слайд 9
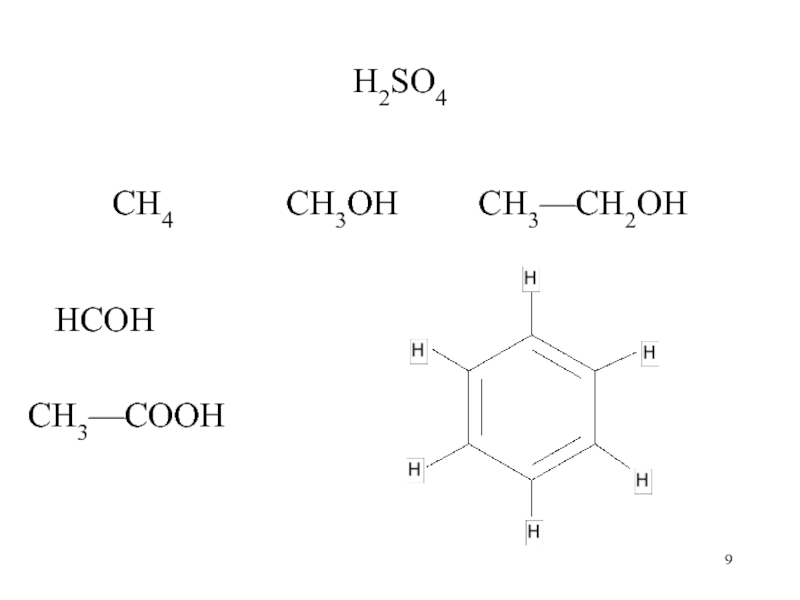
H2SO4
CH4 CH3OH
CH3—CH2OH
HCOH
CH3—COOH
Слайд 10
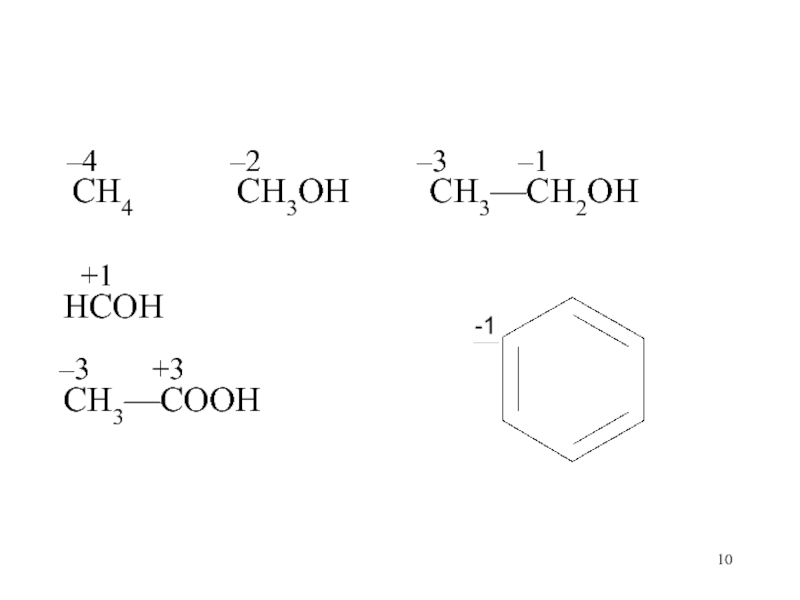
–4
–2
–3 –1
CH4 CH3OH CH3—CH2OH
+1
HCOH
–3 +3
CH3—COOH
Слайд 11
C21+ – 2е C22+
fэкв(Аск.к.) = 1/2
Mэкв(Аск.к.)
= M(Аск.к.)/2
Слайд 12Перманганатометрия
Титрант – 0,02 М или 0,1 М (1/5 KMnO4) или
0,1 н. раствор KMnO4
По точной навеске приготовить нельзя, т.к.
сильный окислитель.
Готовят раствор приблизительно нужной кон-центрации, выдерживают 7-10 дней или кипятят 10 минут для окисления восстанови-телей, содержащихся в воде
Фильтруют через стеклянный фильтр.

Слайд 13
Стандартизацию проводят по щавелевой кисло-те H2C2O42H2O, оксалату натрия Na2C2O4, оксиду
мышьяка (III) As2O3, металлическому железу.
Стандартизацию проводят только в сернокислой
среде.
16HCl + 2KMnO4 5Cl2 + 2MnCl2 + 2KCl +8H2O
Индикатор – сам титрант.

Слайд 14
Стандартизация 0,1 н. по щавелевой кислоте
60-70 0С
5H2C2O4 + 2KMnO4
+ 3H2SO4 2MnSO4 +
10CO2 + K2SO4 +
8H2O
C2O42– – 2е 2CO2

Слайд 15Этикетка:
0,02 М или 0,1 М (1/5KMnO4) или 0,1 н.
К =
0,9972
Хранят в темном месте, в склянках темного стекла
свет
4KMnO4 + 2H2O 4MnO2 + 4 KOH + 3H2O
По ГФ XIII стандартизация по тиосульфату натрия

Слайд 16Применение:
прямая перманганатометрия
Железа (II) сульфат:
10FeSO4 + 2KMnO4 + 8H2SO4
5Fe2(SO4)3 +
K2SO4 + 2MnSO4 + 8H2O
2Fe2+ – 2е
Fe23+
Сэкв(KMnO4)·Mэкв(FeSO4)
Т(KMnO4/FeSO4) = ————————————
1000

Слайд 17
m(FeSO4) = V(KMnO4)·K·T(KMnO4/FeSO4)
V(KMnO4)·K·T(KMnO4/FeSO4)·100
(FeSO4) = ——————————————, %
а(FeSO4)
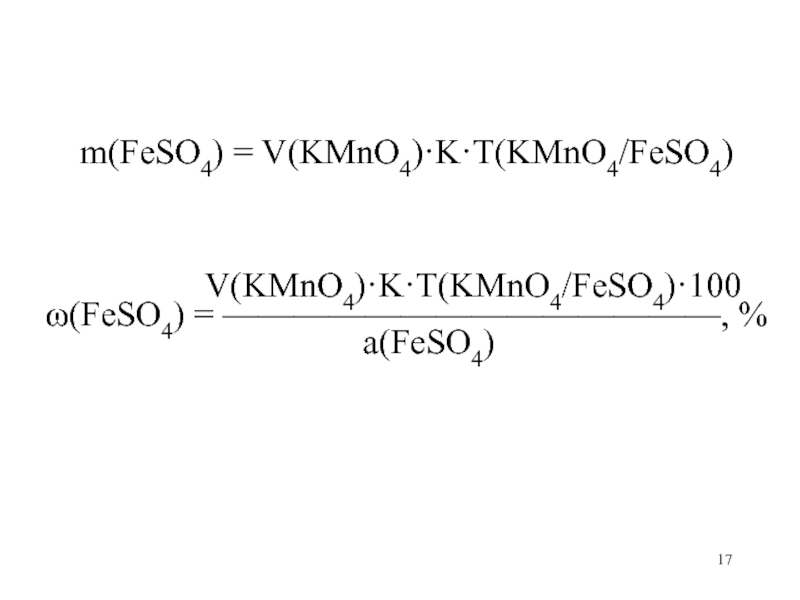
Слайд 18Перекись водорода:
5H2O2 + 2KMnO4 + 3H2SO4 5O2 + K2SO4
+
2MnSO4 + 8H2O
O22– – 2е O2
Сэкв(KMnO4)·Mэкв(H2O2)
Т(KMnO4/H2O2) = ————————————
1000
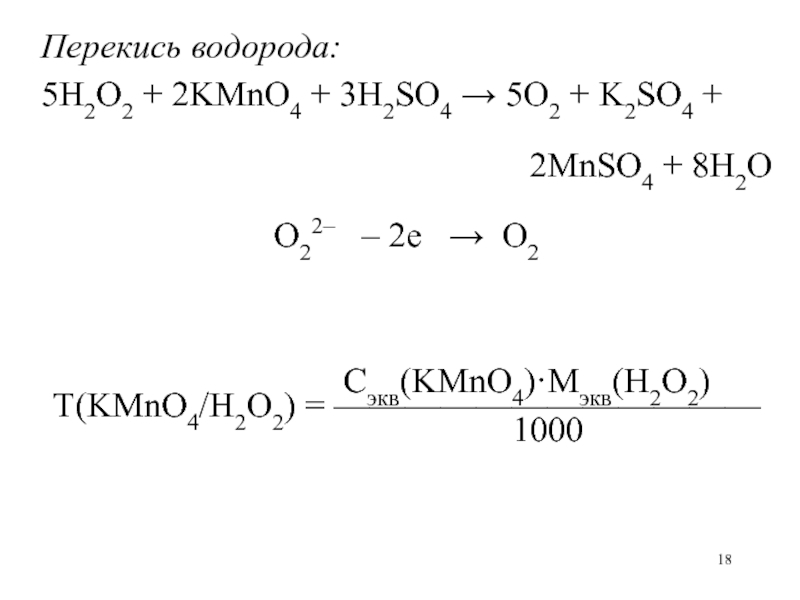
Слайд 19Аскорбиновая кислота:
C21+ – 2е C22+
Сэкв(KMnO4)·Mэкв(Аск.к.)
Т(KMnO4/Аск.к.) = ————————————
1000
Слайд 20обратная перманганатометрия
Натрия нитрит:
5NaNO2 + 2KMnO4(изб.) + 3H2SO4 5NaNO3 +
2MnSO4 + K2SO4 + 3H2O
2KMnO4(ост.) + 10KI + 8H2SO4
2MnSO4 + 5I2
+ 6K2SO4 + 8H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6

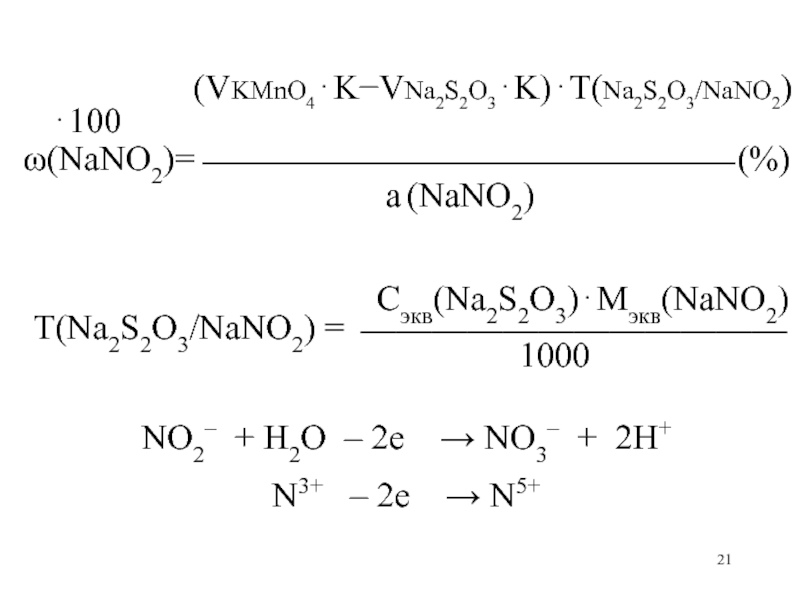
Слайд 21
(VKMnO4KVNa2S2O3K)Т(Na2S2O3/NaNO2)100
(NaNO2)= (%)
а (NaNO2)
Сэкв(Na2S2O3)Мэкв(NaNO2)
Т(Na2S2O3/NaNO2) =
1000
NO2– + H2O – 2е NO3– + 2H+
N3+ – 2е N5+
Слайд 225NaNO2 + 2KMnO4(изб.) + 3H2SO4 5NaNO3 +
2MnSO4 +
K2SO4 + 3H2O
NO2– + H2O – 2е
NO3– + 2H+ | 5
MnO4– + 8H+ + 5е Mn2+ + 4H2O | 2
5NO2– + 2MnO4– + 16H+ + 5H2O
5NO3– + 10H+ + 2Mn2+ + 8H2O
или
5NO2– + 2MnO4– + 6H+ 5NO3– + 2Mn2+ + 3H2O
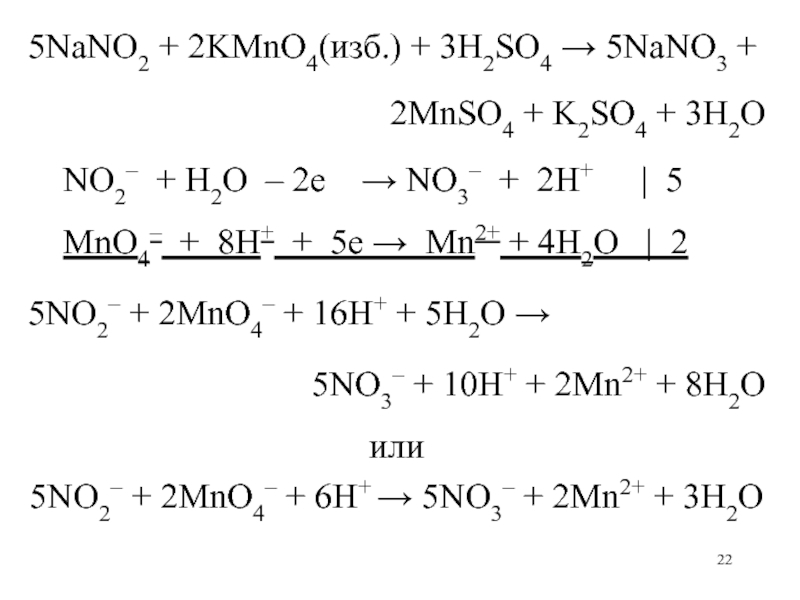
Слайд 23
Кривые окислительно-восстановительного титрования
Выражают зависимость величины потенциала от концентрации титранта

Слайд 24
Задача. Рассчитать и построить кривую титрова-ния соли Fe (II) раствором
перманганата калия, если
Eo (Fe3+/Fe2+) = + 0,77 B;
Eo (MnO4–/Mn2+) = + 1,51 B
Какой из индикаторов можно использовать в данном случае?

Слайд 252,2 – Дипиридил (комплекс с рутением)
Ео = 1,33 В
Дифениламин-2,2
–дикарбоновая кислота
Ео = 1,26 В
Комплекс 1,10-фенантролина с Fe (II)
Ео = 1,14 В
Фенилантраниловая кислота Ео = 1,08 В
Дифениламин Ео = 0,76 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В

Слайд 26
5Fe2+ + MnO4– + 8H+ 5Fe3+ + Mn2+ +
4H2O
В начале титрования и до т.э. в растворе будут: Fe2+,
Fe3+ ,Mn2+
Потенциал системы будет определяться парой восстановителя Fe3+/Fe2+
Величина потенциала может быть вычислена по уравнения Нернста:
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]

Слайд 27
В точке эквивалентности:
E = (mEoв-ля + nEoок-ля )/(m +

Слайд 285Fe2+ + MnO4– + 8H+ 5Fe3+ + Mn2+ +
4H2O
за т. э. в растворе будут:
Fe3+, MnO4– и Mn2+
Потенциал будет определяться парой
окислителя MnO4– /Mn2+
Величина потенциала вычисляется по уравнению Нернста:
E = Eo + 0,059/5 lg[MnO4–][H+]8/[Mn2+]

Слайд 29 Пусть концентрация ионов водорода равна 1 М
Доб-но
От-но [Fe3+] [Fe3+]
——— lg ——— E=Eo +0,059/1
KMnO4– в % [Fe2+] [Fe2+] lg [Fe3+]/[Fe2+]
9 9 9/9110-1 -1 0,77–0,059=0,71В
50 50 50/50=1 0 0,77 В
99 99 99/1102 2 0,77+0,0592=0,89В
99,9 99,9 99,9/0,1103 3 0,77+0,0593=0,95В
100 E = (mEoв-ля+nEoок-ля )/(m+n)=(10,77+51,51)/(1+5)
=1,39 B
![1
Окислительно-восстановительное
титрование Пусть концентрация ионов водорода равна 1 М Доб-но От-но [Fe3+] Пусть концентрация ионов водорода равна 1 М Доб-но От-но [Fe3+]](https://theslide.ru/img/thumbs/1de0cf9c84cc626a6231efe70e038a90-800x.jpg)
Слайд 30
Доб-но Изб-к [MnO4–][H+]8
————— lgдроби E=Eo +0,059/5lgдр
KMnO4– в % [Mn2+]
100,1 0,1 0,1/10010-3 -3 1,51+(0,059/5)(-3) = 1,475 B
101 1 1/100=10-2 -2 1,51+(0,059/5)(-2)
= 1,486 B
110 10 10/100=10-1 -1 1,51+(0,059/5)(-1)
= 1,498 B
![1
Окислительно-восстановительное
титрование Доб-но Изб-к [MnO4–][H+]8 Доб-но Изб-к [MnO4–][H+]8](https://theslide.ru/img/thumbs/91107d2dba1e887f0b2a8f7932d34e0f-800x.jpg)
Слайд 31
Скачок от 0,95 В до 1,475 В
2,2 – Дипиридил
(комплекс с рутением)
Ео = 1,33 В
Дифениламин-2,2 –дикарбоновая кислота
Ео
= 1,26 В
Комплекс 1,10-фенантролина с Fe (II)
Ео = 1,14 В
Фенилантраниловая кислота Ео = 1,08 В
Дифениламин Ео = 0,76 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В

Слайд 32Интервал изменения окраски индикаторов
Ind(ок) + ne
Ind(вос)
0,059 [Ind(ок)]
E = Eo + ——— lg ————
n [Ind(вос)]
[Ind(ок)]
———— = 10 – наблюдаем окраску окисленной
[Ind(вос)] формы
E = Eo + 0,059/n lg10 = Eo + 0,059/n

Слайд 33
[Ind(ок)]
——— = 0,1 – наблюдаем окраску восстановл.
[Ind(вос)]
формы
E = Eo + 0,059/n lg 0,1 = Eo – 0,059/n
E = Eo ± 0,059/n
![1
Окислительно-восстановительное
титрование [Ind(ок)] ——— = 0,1 – наблюдаем окраску восстановл. [Ind(вос)] [Ind(ок)] ——— = 0,1 – наблюдаем окраску восстановл. [Ind(вос)]](https://theslide.ru/img/thumbs/4bd741a5a91052d7e68ed2907ee51096-800x.jpg)
Слайд 34
Индикаторы окислительно-восстановительного титрования
1. Специфические – индикаторы, которые вза-имодействуют с одной
из форм окислительно-восстановительной пары с изменением окраски (крахмал)
2. Редокс-индикаторы —
вещества, которые при определенном потенциале раствора окисля-ются или восстанавливаются с изменением окраски

Слайд 35Редокс-индикаторы:
1. Обратимые E = Eo ± 0,059/n
Дифениламин Ео = 0,76 В
бесцветный – фиолетовый
м.р. в воде, готовят 1% р-р в концентр. H2SO4
Ферроин – комплекс Fe(II) с о-фенантролином
Ео = 1,14 В
[FeL3]2+ – e [FeL3]3+
красная бледно-голубая
Фенилантраниловая кислота (Ео = 1,08 В) и др.

Слайд 36
2. Необратимые
Метиловый оранжевый
Метиловый красный,
Нейтральный красный
При окислении необратимо исчезает окраска
раствора

Слайд 37Индикаторные ошибки окислительно-восстановительного титрования
Индикаторная ошибка рассчитывается по формуле:
n’(X)
Х = ———— · 100
n(X)
n’(X) – количество неоттитрованного вещества (или избыточно прибавленного титранта)
n(X) – количество вещества, взятого для титрования

Слайд 38Задача. Рассчитать ошибку титрования железа сульфата (II) раствором KMnO4 в
сернокислой среде при [H+] = 1 моль/л с индикатором дифениламином
(Ео = 0,76 В).
Потенциал системы в т.э.:
E = (mEoв-ля+nEoок-ля )/(m+n)=(10,77+51,51)/(1+5)
=1,39 B
![1
Окислительно-восстановительное
титрование Задача. Рассчитать ошибку титрования железа сульфата (II) раствором KMnO4 в сернокислой Задача. Рассчитать ошибку титрования железа сульфата (II) раствором KMnO4 в сернокислой среде при [H+] = 1 моль/л](https://theslide.ru/img/thumbs/4a64fb8f9e307d0b1f73aee93268dbae-800x.jpg)
Слайд 39Таким образом,
Изменение окраски произойдет при 0,76 В
Т.э. наступит при 1,39
В, следовательно,
раствор недотитрован.
Потенциал системы рассчитывался по паре [Fe3+]/[Fe2+] (Eo =
0,77 В) и закончили титровать при 0,76 В
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
0,76 = 0,77 + 0,059/1 lg[Fe3+]/[Fe2+]

Слайд 40lg[Fe3+]/[Fe2+] = – 0,169
[Fe3+]
0,68
———— = 0,68 = ———
[Fe2+] 1
n’(X)
Х = ———— · 100
n(X)
n’(X) = 1 (количество неоттитрованного в-ва)
n(X) = 1 + 0,68 (количество вещества, взятого для титрования)
![1
Окислительно-восстановительное
титрование lg[Fe3+]/[Fe2+] = – 0,169 [Fe3+] lg[Fe3+]/[Fe2+] = – 0,169 [Fe3+]](https://theslide.ru/img/thumbs/0f9d3200acb1bf321ff96c8d3537d748-800x.jpg)
Слайд 41
Ошибка титрования составит:
1
Х =
———— · 100 = 59,5 %
1 + 0,68
Индикаторная ошибка д.б. не более 0,1 %.

Слайд 42Задача. Рассчитать и построить кривую титрования соли олова (II) раствором
соли железа (III), если Eo (Fe3+/Fe2+) = + 0,77 B
и
Eo (Sn4+/Sn2+) = + 0,15 B.
Какой из индикаторов вы выберете?
Дифениламин Ео = 0,76 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
Нейтральный красный Ео = 0,24 В
Рассчитать ошибку титрования с индикатором – метиленовый голубой

Слайд 43
Sn2+ + 2Fe3+ Sn4+ + 2Fe2+
В начале титрования
и до т.э. в растворе будут: Sn2+, Sn4+, Fe2+
Потенциал системы будет определяться парой восстановителя Sn4+/Sn2+,
Величина потенциала вычисляется по уравнению Нернста:
E = Eo + 0,059/2 lg[Sn4+]/[Sn2+]

Слайд 44
В точке эквивалентности:
E = (mEoв-ля + nEoок-ля )/(m +
n)
E = (2 · 0,15 + 1· 0,77) /
3 = 0,36 B

Слайд 45
Sn2+ + 2Fe3+ Sn4+ + 2Fe2+
за т. э. в
растворе будут:
Fe3+, Sn4+, Fe2+
Потенциал будет определяться парой
окислителя Fe3+/Fe2+
Величина
потенциала вычисляется по уравнению Нернста:
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]

Слайд 46
Доб-но От-но
[Sn4+] [Sn4+]
——— lg ——— E
Fe3+ в % [Sn2+] [Sn2+]
9 9 9/9110-1 -1 0,12 В
50 50 50/50 1 0 0,15 В
90 90 90/10101 1 0,18 В
99 99 99/1102 2 0,21 В
99,9 99,9 99,9/0,1103 3 0,24 В
100 0,36 B
![1
Окислительно-восстановительное
титрование Доб-но От-но [Sn4+] [Sn4+] Доб-но От-но [Sn4+]](https://theslide.ru/img/thumbs/8d39817e9293b8f84eb7ab246791cd14-800x.jpg)
Слайд 47
Доб-но Изб-к
[Fe3+] [Fe3+]
——— lg ——— E
Fe3+ в % [Fe2+] [Fe2+]
100,1 0,1 0,1/10010-3 -3 0,59 B
101 1 1/100=10-2 -2 0,65 B
110 10 10/100=10-1 -1 0,71 B
Скачок от 0,24 В до 0,59 В
Метиленовый голубой Ео = 0,53 В
Индиготетрасульфоновая кислота Ео = 0,36 В
Нейтральный красный Ео = 0,24 В
![1
Окислительно-восстановительное
титрование Доб-но Изб-к [Fe3+] [Fe3+] Доб-но Изб-к [Fe3+]](https://theslide.ru/img/thumbs/5a5ed037c7e0a6c8cdb51ccd492b06f3-800x.jpg)
Слайд 48
Изменение окраски произойдет при 0,53 В
Т.э. наступит при 0,36 В,
следовательно,
раствор перетитрован.
Потенциал системы рассчитывался по паре окислителя [Fe3+]/[Fe2+] (Eo =
0,77 В) Закончили титровать при 0,53 В
E = Eo + 0,059/1 lg[Fe3+]/[Fe2+]
0,53 = 0,77 + 0,059/1 lg[Fe3+]/[Fe2+]

Слайд 49lg[Fe3+]/[Fe2+] = – 6,949
[Fe3+]
1·10–7
———— = 1·10–7 = ———
[Fe2+] 1
1·10–7
Х = ——— · 100 = 1·10–5 %
1
n’(X) = 1·10–7 (количество избыточно прибавлен-
ного титранта)
n(X) = 1 + 1·10–7 1 (количество вещества,
взятого для титрования)
![1
Окислительно-восстановительное
титрование lg[Fe3+]/[Fe2+] = – 6,949 [Fe3+] lg[Fe3+]/[Fe2+] = – 6,949 [Fe3+]](https://theslide.ru/img/thumbs/8d0c6e038e4600cf82f139280b064980-800x.jpg)
Слайд 50Дихроматометрия
Титрант – 0,0167 М или 0,1 М (1/6 K2Cr2O7) или
0,1 н. раствор K2Cr2O7
Стандартный раствор можно приготовить по точной
навеске
Cr2O72 + 14H+ + 6ē 2Cr3+ + 7H2O
fэкв(K2Cr2O7) = 1/6
Mэкв(K2Cr2O7) = M(K2Cr2O7)/6

Слайд 51
K2Cr2O7 – оранжевая окраска
Cr3+ – зеленоватая окраска, однако интенсивности
цвета не хватает для фиксации конечной точки титрования
Ind –
дифениламин, дифениламинсульфоновая кислота и др.

Слайд 52
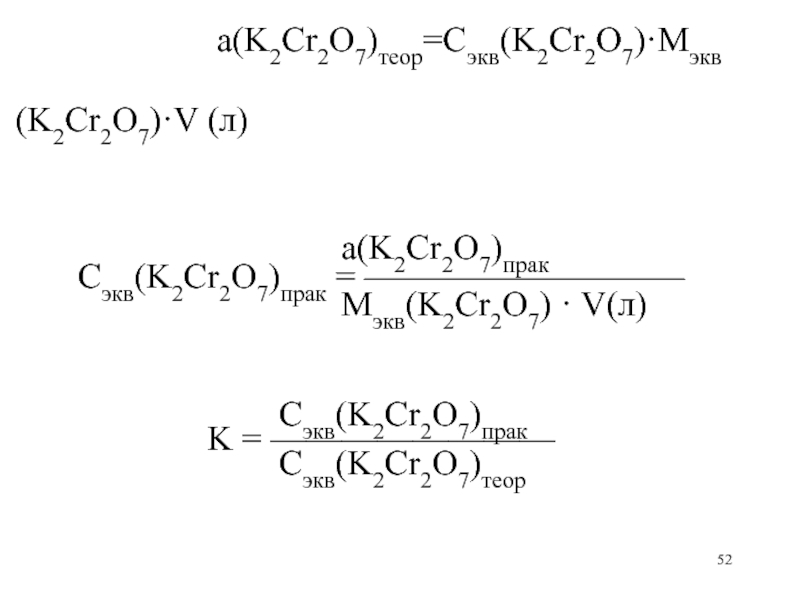
а(K2Cr2O7)теор=Сэкв(K2Cr2O7)·Mэкв(K2Cr2O7)·V (л)
а(K2Cr2O7)прак
Сэкв(K2Cr2O7)прак = —————————
Mэкв(K2Cr2O7) · V(л)
Сэкв(K2Cr2O7)прак
K = ————————
Сэкв(K2Cr2O7)теор
Слайд 53Применение:
прямая дихроматометрия
Железа (II) сульфат:
6FeSO4 + K2Cr2O7 + 7H2SO4 3Fe2(SO4)3
+
Cr2(SO4)3 + K2SO4 + 7H2O
2Fe2+ – 2е
Fe23+
Сэкв(K2Cr2O7)·Mэкв(FeSO4)
Т(K2Cr2O7/FeSO4) = ———————————
1000

Слайд 54
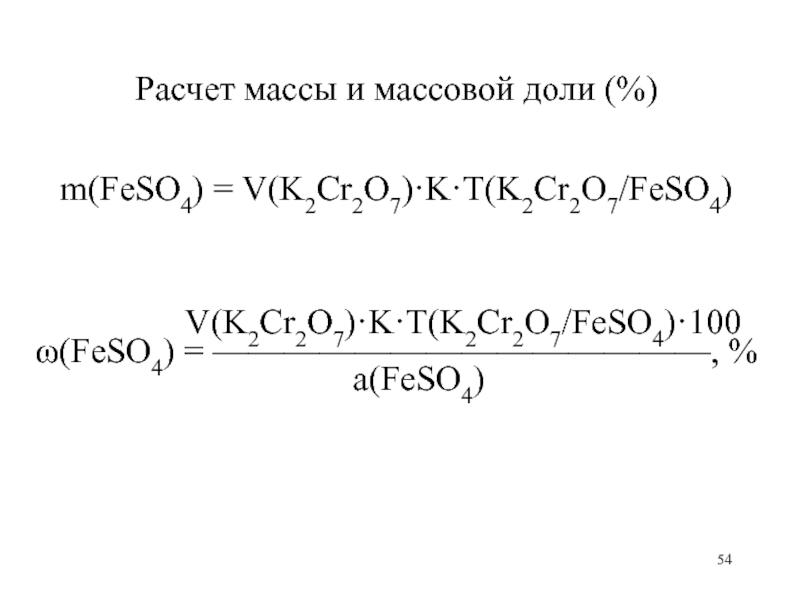
Расчет массы и массовой доли (%)
m(FeSO4) = V(K2Cr2O7)·K·T(K2Cr2O7/FeSO4)
V(K2Cr2O7)·K·T(K2Cr2O7/FeSO4)·100
(FeSO4) = ——————————————, %
а(FeSO4)
Слайд 55Калия иодид:
6KI + K2Cr2O7 + 7H2SO4 3I2 + Cr2(SO4)3
+
4K2SO4 + 7H2O
2I– – 2е I2
Сэкв(K2Cr2O7)·Mэкв(KI)
Т(K2Cr2O7/KI) = ——————————
1000
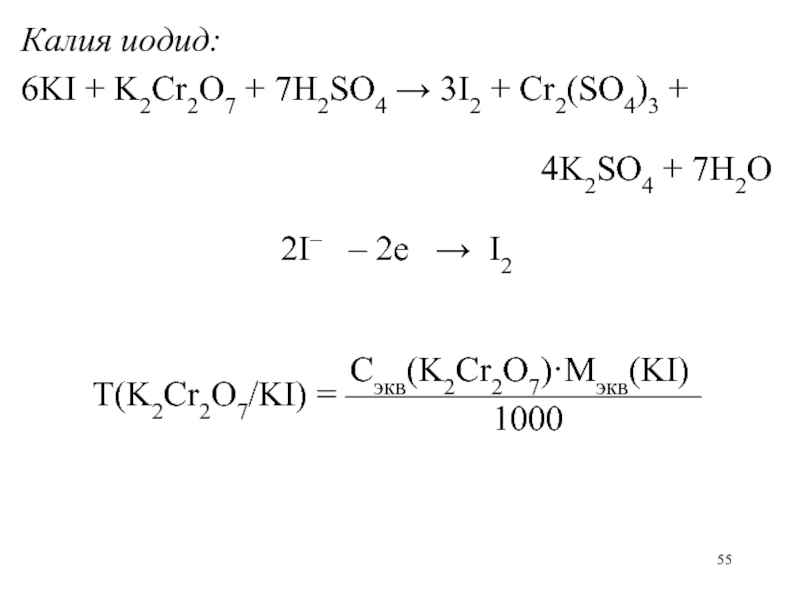
Слайд 56Кислота аскорбиновая:
C21+ – 2е C22+
С(1/6K2Cr2O7)·M(1/2Аск.к.)
Т(K2Cr2O7/Аск.к.) = ———————————
1000
Слайд 57Обратная дихроматометрия применяется для определения спирта этилового:
3CH3CH2OH + 2K2Cr2O7 +
8H2SO4
избыток
3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O
K2Cr2O7 + 6KI + 7H2SO4 3I2 + Cr2(SO4)3 +
остаток 4K2SO4 + 7H2O
I2 + 2Na2S2O3 2NaI + Na2S4O6

Слайд 58 Расчет массовой доли (%)
(V(K2Cr2O7)K
V(Na2S2O3)K)Т(Na2S2O3/Сп)100
(Сп) = (%)
а (CH3CH2OH)
Сэкв(Na2S2O3)Мэкв(Спитра)
Т(Na2S2O3/Сп) =
1000
-1 +3
CH3—CH2OH – 4 е CH3—COOH
Слайд 59Преимущества дихроматометрии перед перманганатометрией
1. Титрант можно приготовить по точной навеске
2.
Титрование можно проводить в присутствии
HCl
Eo(Cr2O72–/2Cr3+) = 1,33 B
Eo(Cl2/2Cl–) =
1,33 B
При титровании Cl– не окисляются Cr2O72–-
ионами

